㉔말단비대증 첫 경구용 SST2 작용제 '팔투소틴'
- 최병철 박사
- 2026-03-20 06:00:55
-
가
- 가
- 가
- 가
- 가
- 가
- 최병철 박사의 노벨드럭 인사이트
- 기존 주사제와 달리 경구 투여 강점
- 장기적 안전성 자료 필요...환자 선택 기준 확립 과제
- PR
- 전국 지역별 의원·약국 매출&상권&입지를 무료로 검색하세요!!
- 데일리팜맵 바로가기

팔소니파이(PalsonifyⓇ, 성분명: 팔투소틴 paltusotine, Crinetics Pharmaceuticals)는 최초의 1일 1회 경구 선택적 소마토스타틴 수용체 2형(somatostatin receptor type 2, SST2) 비펩타이드 작용제다. 작년 9월 미국 FDA에서 수술에 대한 반응이 불충분하거나 수술이 불가능한 성인 말단비대증(acromegaly) 환자의 치료제로 승인되었다.
말단비대증은 뇌하수체 전엽에서 성장호르몬(growth hormone, GH)이 과다 분비되어 대사 및 신체 발달 이상을 초래하는 질환이다. 환자에서는 만성적으로 성장호르몬(GH)과 인슐린유사성장인자-1(insulin-like growth factor-1, IGF-I,, IGF-1) 수치가 상승되어 있으며, 이로 인해 이마 돌출, 턱 비대, 손발 비대, 피부 비후 등 과도한 조직 성장 등이 나타난다.
말단비대증의 약물 치료는 GH 및 IGF-1의 과다 분비를 억제하거나 그 작용을 차단하는 것을 목표로 하며, 이에는 도파민 작용제(dopamine agonists), 소마토스타틴 유사체(somatostatin analogs), 성장호르몬 수용체 길항제(growth hormone receptor antagonists)가 있다.
팔소니파이는 경구용 소마토스타틴 수용체 작용제로, 소마토스타틴 수용체 2형(SSTR2)에 선택적으로 작용하여 성장호르몬(GH) 분비를 억제하고 IGF-1 생성을 감소시킨다.
팔소니파이의 승인은 PATHFNDR-1 및 PATHFNDR-2 3상 임상시험 결과를 기반으로 이루어졌다. 해당 연구에서는 이전 치료 경험이 있는 환자와 치료 경험이 없는 환자를 포함한 성인 말단비대증 환자를 대상으로 약물의 유효성과 안전성이 평가되었다.
두 연구의 주요 평가 변수는 위약군과 비교하여 IGF-1 수치가 정상 상한치(ULN)의 1.0배 이하에 도달한 환자의 비율이었다.
PATHFNDR-1 연구는 주사형 소마토스타틴 유사체(SRL) 치료에서 전환한 말단비대증 환자 58명을 대상으로 수행된 무작위 배정, 이중맹검, 위약 대조 임상시험이다. 연구 대상자는 36주 동안 팔투소틴 또는 위약을 투여받았으며, 이후 선택적 공개 라벨 연장 연구가 진행되었다. 36주 평가 결과, 팔투소틴 투여군의 83%가 IGF-1 수치를 정상 상한치의 1.0배 이하로 유지한 반면, 위약군에서는 4%만이 해당 기준을 충족하였다.
PATHFNDR-2 연구는 약물 치료 경험이 없거나 조절되지 않은 말단비대증 환자 111명을 대상으로 수행된 무작위 배정, 이중맹검, 위약 대조 임상시험이다. 연구는 24주 치료 기간으로 구성되었으며, 이후 선택적 공개 라벨 연장 연구가 포함되었다. 24주 평가 결과, 팔투소틴 투여군의 56%가 IGF-1 수치를 정상 상한치의 1.0배 이하로 달성한 반면, 위약군에서는 5%만이 해당 기준을 달성하였다.
또한 말단비대증 증상 일기(Acromegaly Symptom Diary, ASD)를 통한 평가에서 질환 관련 징후 및 증상이 유의하게 개선된 것으로 나타났다.
임상시험 기간 동안 보고된 흔한 이상반응으로는 설사, 복통, 메스꺼움, 식욕 감소, 동성 서맥, 고혈당, 심계항진, 위장염 등이 있었다.
말단거대증(Acromegaly)이란 무엇인가?
말단비대증은 뇌하수체 전엽의 이상으로 성장호르몬(growth hormone, GH)이 과다 분비되어 발생하는 내분비 질환이다. 정상적인 생리 상태에서 GH 분비는 시상하부와 뇌하수체 간의 정교한 조절 기전에 의해 유지된다.
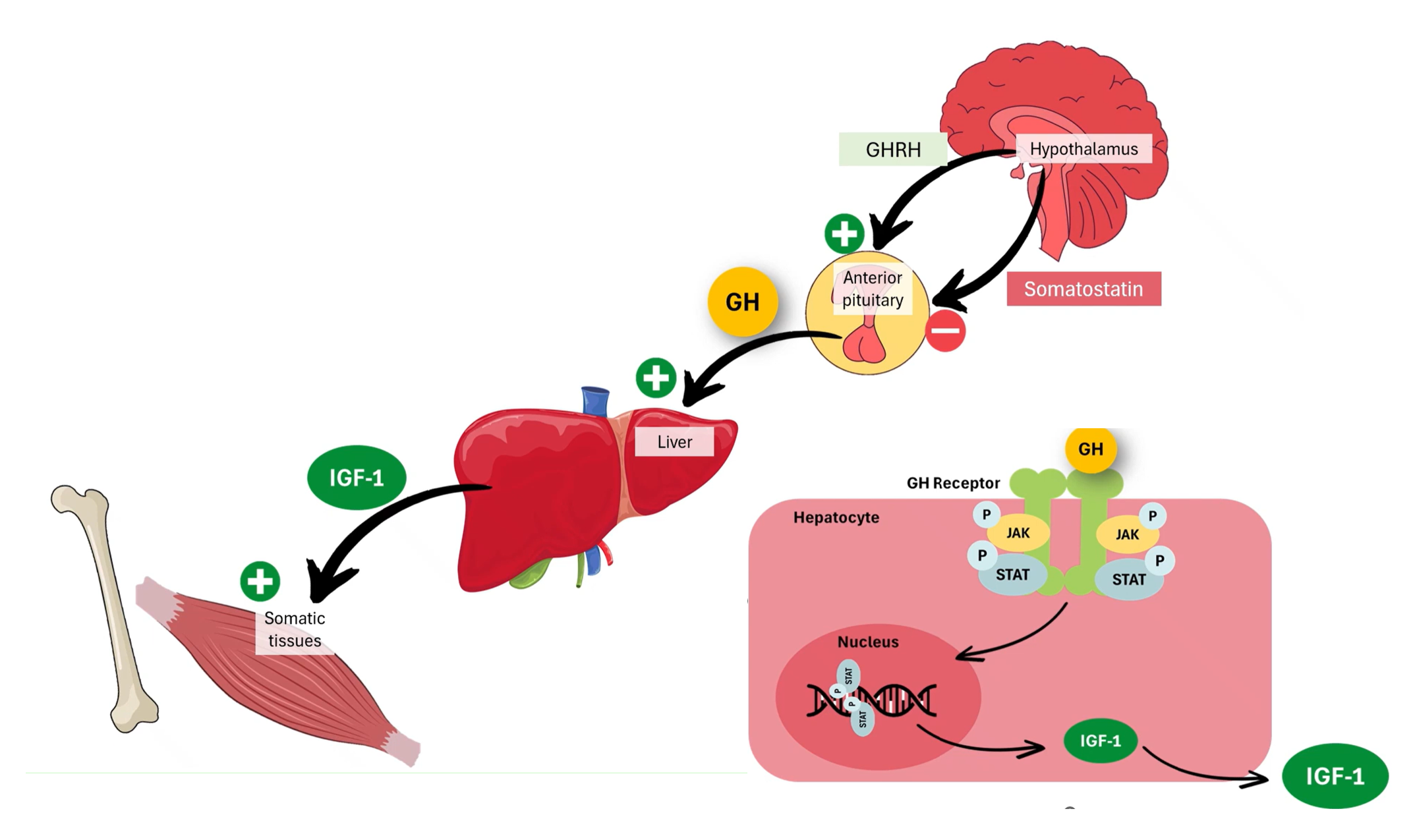
GH 분비 조절은 시상하부에서 분비되는 성장호르몬 방출호르몬(GHRH)과 소마토스타틴 간의 상호작용에 의해 이루어진다. GHRH는 뇌하수체 전엽의 체성장호르몬 분비세포(somatotroph)를 자극하여 GH 분비를 증가시키는 반면, 소마토스타틴(somatostatin)은 동일 세포에서 GH 분비를 억제하는 반대 작용을 한다. 이러한 균형적 조절을 통해 GH 분비는 맥동성(pulsatile) 패턴을 유지한다.
또한 GH와 인슐린유사성장인자-1(insuline-like growth hormone, IGF-1)은 음성 피드백 기전을 통해 시상하부와 뇌하수체에 작용하여 GHRH 분비를 감소시키고 소마토스타틴 분비를 증가시킴으로써 GH 분비를 조절한다(Figure 1).
그러나 GH가 과다 분비될 경우 IGF-1 생성 역시 증가하며, 이러한 GH–IGF-1 축의 지속적인 과활성화는 조직 및 장기의 비정상적인 과성장을 초래한다. 이러한 병태생리적 변화의 결과로 발생하는 질환이 말단비대증이다.
성장호르몬 과다증의 원인은 크게 세 가지로 구분된다.
첫째, 원발성 성장호르몬 과다(primary GH excess)로, 가장 흔한 원인이며 대부분 GH 분비 뇌하수체 선종(pituitary adenoma)에 의해 발생한다. 드물게 GH 분비 암종이나 다호르몬 분비 뇌하수체 선종(multihormonal pituitary adenoma)이 원인이 될 수 있다.
둘째, 이소성 또는 의인성 성장호르몬 과다(ectopic or iatrogenic GH excess)로, 외부에서 GH가 과다 투여되거나 뇌하수체 이외의 종양에서 GH 또는 GH 유사 물질이 분비되는 경우에 해당한다.
셋째, 성장호르몬 방출호르몬(GHRH) 과다로, GHRH의 과잉 분비로 인해 뇌하수체 GH 분비가 과도하게 자극되는 경우이다. 이는 시상하부 과오종(Hypothalamic hamartoma), 신경절종(ganglioma) 등의 중추성 원인이나 기관지 유암종, 갈색세포종 등 말초 종양에 의해 발생할 수 있다.
따라서 말단비대증은 대부분 뇌하수체의 양성 종양(GH 분비 선종)에 의해 발생하며, GH와 IGF-1의 지속적인 과다 분비로 다양한 전신 증상과 합병증을 유발하는 희귀 내분비 질환이다.
GH 과다 분비로 인한 전신적 임상 증상을 특징으로 하며, 연부 조직 및 골격의 비대, 대사 이상, 심혈관 및 호흡기 합병증 등이 동반될 수 있다. 얼굴 및 손발의 비대, 턱 돌출, 피부 비후, 발한 증가, 관절통 등의 특징적인 신체 변화가 나타나며, 장기적으로는 당뇨병, 고혈압, 심근비대 등 다양한 합병증이 발생할 수 있다.
말단비대증의 치료 목표는 GH 및 IGF-1 수치를 정상 범위로 조절하여 질환의 진행을 억제하고 합병증 발생을 최소화하는 것이다. 이러한 치료 전략에서 소마토스타틴 수용체를 표적으로 하는 약물은 GH 분비 억제와 종양 성장 억제를 통해 말단비대증 관리에 중요한 역할을 한다.
소마토스타틴(Somatostatin)은 어떤 호르몬인가?
소마토스타틴은 성장호르몬 억제호르몬(growth hormone-inhibiting hormone, GHIH)으로 1973년 Brazeau 등에 의해 처음 발견되었으며, 이후 GH 분비 조절뿐만 아니라 다양한 내분비 및 외분비 호르몬 분비를 억제하는 중요한 생리적 조절 호르몬으로 밝혀졌다. 이는 시상하부뿐 아니라 췌장, 위장관, 중추신경계 등 다양한 조직에서 생성되며, 국소적인 호르몬 조절에도 관여한다.
소마토스타틴은 주로 두 가지 활성 형태인 소마토스타틴-14(SST-14)와 소마토스타틴-28(SST-28)으로 존재한다. SST-14는 시상하부와 췌장에서 주로 발견되며, SST-28은 위장관에서 상대적으로 높은 농도로 존재한다.
이들 펩타이드는 세포막에 존재하는 G 단백질 결합 수용체(G protein–coupled receptor, GPCR) 계열인 소마토스타틴 수용체(SSTR1~SSTR5)에 결합하여 생물학적 작용을 나타낸다.
이러한 수용체는 다양한 조직에 분포하며, 각 수용체 아형은 호르몬 분비 조절, 세포 증식 억제, 신호 전달 조절 등 여러 생리적 기능에 관여한다.
소마토스타틴의 작용 기전은 주로 세포 내 아데닐산 고리화효소(adenylyl cyclase) 활성을 억제하여 cAMP 생성을 감소시키고, 칼슘 이온 채널(Ca²⁺ channel)의 활성은 억제되고 칼륨 채널(K⁺ channel)은 활성화를 유도하는 방식으로 이루어진다. 이러한 신호 전달 변화는 GH를 포함한 다양한 호르몬의 분비를 감소시키는 결과를 초래한다.
또한 소마토스타틴은 세포 증식 억제와 세포자멸사(apoptosis) 촉진 등 항증식 효과를 나타내어 종양 세포의 성장 억제에도 관여하는 것으로 알려져 있다. 그러나 천연 소마토스타틴은 혈중 반감기가 약 1~3분으로 매우 짧고 체내에서 빠르게 분해되기 때문에 임상적으로 직접 사용하기에는 제한적이다.
이러한 한계를 극복하기 위해 반감기와 안정성을 개선한 소마토스타틴 유사체(somatostatin analogs)가 개발되었으며, 현재 말단비대증, 신경내분비 종양, 쿠싱병 등의 치료에 널리 사용되고 있다. 대표적인 약물로는 옥트레오티드(octreotide), 란레오티드(lanreotide), 파시레오티드(pasireotide)가 있으며, 이들은 특정 소마토스타틴 수용체 아형에 선택적으로 결합하여 GH 분비 억제 및 IGF-1 감소 효과를 나타낸다.
따라서 소마토스타틴은 GH 분비를 조절하는 핵심적인 억제 호르몬으로서 내분비계의 중요한 조절 축을 형성하며, 이러한 생리적 역할을 기반으로 한 소마토스타틴 유사체는 말단비대증과 같은 GH 과다 분비 질환의 치료에서 중요한 치료 전략으로 활용되고 있다.
소마토스타틴수용체(Somatostatin receptor, SSTR)는 무엇인가?
소마토스타틴의 생리적 작용은 소마토스타틴 수용체(somatostatin receptor, SSTR)에 의해 매개되며, 이 수용체는 SSTR1부터 SSTR5까지 총 5가지 아형으로 구성된 G 단백질 결합 수용체(G protein-coupled receptor, GPCR) 계열에 속한다. 뇌하수체 전엽에서는 이들 수용체 아형이 모두 발현되지만, 성장호르몬을 분비하는 체성장호르몬 분비세포(somatotroph)에서는 특히 SSTR2와 SSTR5가 높은 수준으로 발현되는 것으로 알려져 있다.
SSTR1은 주로 뇌, 췌장 β세포, 위장관 및 일부 종양 세포에서 발현되며, SSTR2는 뇌, 뇌하수체, 췌장 α세포, 위장관, 부신, 면역세포 및 다양한 종양 세포에 광범위하게 분포한다. SSTR3는 뇌, 위장관, 간, 비장 등에서 발현되고, SSTR4는 비교적 낮은 수준이지만 뇌, 폐, 심장, 위장관 및 태반 등에서 관찰된다.
SSTR5는 뇌, 뇌하수체, 췌장 β세포 및 δ세포, 위장관과 종양 세포에서 발현되는 것으로 알려져 있다. 이러한 광범위한 분포는 소마토스타틴이 내분비계뿐 아니라 신경계, 면역계, 위장관계 등 다양한 생리적 기능 조절에 관여함을 시사한다.
이러한 수용체 발현 양상은 GH 분비 조절에서 중요한 의미를 가진다. 특히 SSTR2 및 SSTR5에 선택적으로 작용하는 경우 SSTR1, SSTR3, SSTR4에 작용하는 경우보다 훨씬 낮은 농도에서도 GH 분비를 효과적으로 억제할 수 있는 것으로 보고되어 있다. 따라서 SSTR2와 SSTR5는 뇌하수체 체성장호르몬 분비세포에서 GH 분비 억제를 매개하는 핵심 수용체로 간주된다.
여러 연구에서 SSTR2를 통한 신호 전달 기전은 비교적 일관된 결과를 보이는 반면, 다른 수용체 아형을 통한 작용은 조직 및 세포 유형에 따라 차이를 보이는 것으로 알려져 있다. SSTR2 활성화에 따른 소마토스타틴의 주요 작용 기전은 세포 내 신호 전달 변화와 관련된다.
SSTR2는 adenylyl cyclase 활성을 억제하여 세포 내 cAMP 생성을 감소시키며, 이에 따라 칼슘 이온 채널의 활성은 억제되고 칼륨 채널은 활성화된다. 이로 인해 세포막 과분극이 유도되고, 결과적으로 성장호르몬 분비가 억제된다. 이러한 신호 전달 기전은 소마토스타틴이 다양한 내분비 호르몬 분비를 억제하는 핵심 메커니즘으로 이해된다.
소마토스타틴 수용체를 표적으로 하는 약물은 이러한 작용 기전을 기반으로 다양한 질환의 치료에 활용된다. 특히 소마토스타틴 유사체는 말단비대증뿐 아니라 위장관 및 췌장 신경내분비종양(gastroenteropancreatic neuroendocrine tumors)의 호르몬 과다 분비 증상 조절에 널리 사용되고 있다.
말단비대증의 약물 치료는 어떻게 하는가?
말단비대증의 치료는 종양의 성장과 GH 및 IGF-I의 분비를 조절하고 질병의 징후와 증상들을 예방해 삶의 질을 향상시키고 조기사망을 예방하는 것이다. 따라서 주로 수술, 방사선치료, 약물치료 등을 이용한 치료법이 사용되며, 혈중 GH 및 IGF-I 수치의 정상화를 달성한 환자의 비율로 치료효과를 평가한다.
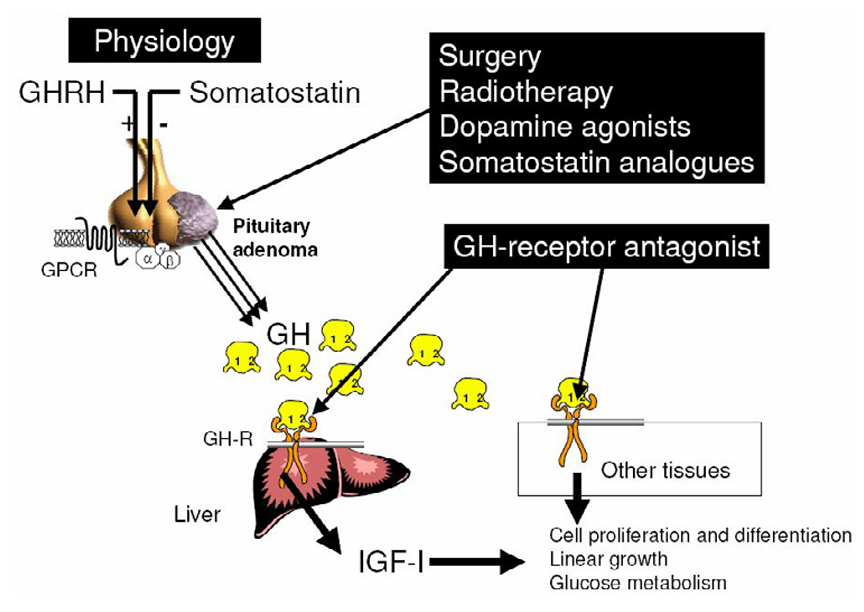
<도파민 작용제(dopamine agonists)>
도파민 작용제는 도파민 수용체를 자극하여 일부 GH 분비 뇌하수체 선종에서 성장호르몬 분비를 감소시키는 효과를 나타낸다. 대표적인 약물로는 카버골린(cabergoline)과 브로모크립틴(bromocriptine)이 있으며, 일반적으로 다른 약물 치료에 비해 효과가 제한적인 경우가 많지만 경구 투여가 가능하다는 장점이 있다. 도파민 작용제는 GH 및 IGF-1 상승 정도가 비교적 경미한 환자나 다른 약물과의 병합 치료에서 사용될 수 있다.
<소마토스타틴 유사체(Somatostatin analogs, SSAs)>
SSAs는 말단비대증의 1차 약물 치료로 가장 널리 사용되는 약물군이다. 이 계통 약물들은 소마토스타틴의 생리적 작용을 모방하여 뇌하수체에서 성장호르몬의 분비를 억제하고, 결과적으로 IGF-1 수치를 감소시킨다.
대표적인 약물로는 1세대 옥트레오티드(octreotide)와 란레오티드(lanreotide), 2세대 파시레오티드(pasireotide)가 있다. 옥트레오티드와 란레오티드는 주로 소마토스타틴 수용체 SSTR2에 높은 친화성을 보이며, 파시레오티드는 SSTR5를 포함한 여러 소마토스타틴 수용체에 더 높은 결합 친화성을 보이는 특징이 있다.
이러한 약물들은 대부분 장기 지속형 제제로 개발되어 4주 간격의 근육 또는 피하 주사 형태로 투여되는 경우가 많으며, 일부 경구 제형도 사용되고 있다. 이 중 SSAs는 성장호르몬분비성 뇌하수체 종양(소마토스타틴 수용체와 결합)에 작용하여 성장호르몬 과분비 및 IGF-1 과분비를 모두 조절하는 합성의약품으로 소마토스타틴 수용체 배위자(somatostatin receptor ligand, SRL)라고도 한다.
<재조합 성장호르몬 수용체 길항제(recombinant GH receptor antagonists, rGHRAs)>
rGHRAs는 GH의 분비 자체를 억제하기보다는 말초 조직에서 GH가 수용체에 결합하는 것을 차단하여 IGF-1 생성과 작용을 감소시키는 방식으로 작용한다. 대표적인 약물은 페그비소만트(pegvisomant, SomavertⓇ)로, 간에서의 IGF-1 생성 억제를 통해 말단비대증의 생화학적 조절을 유도한다. 특히 소마토스타틴 유사체에 충분히 반응하지 않는 환자에서 효과적인 치료 옵션으로 사용될 수 있다.
이와 같이 말단비대증의 약물 치료는 환자의 질환 원인, GH 및 IGF-1 수치, 종양 특성, 기존 치료에 대한 반응 등을 고려하여 선택되며, 수술이나 방사선 치료와 병행하여 질환의 장기적인 조절을 목표로 시행된다.
소마토스타틴 유사체(somatostatin analogs, SSAs)은 어떤 약제인가?
말단비대증의 약물 치료에서 1차적인 접근법은 소마토스타틴의 생리적 작용을 모방하는 소마토스타틴 유사체(SSAs)의 사용이다. 소마토스타틴은 고리형 폴리펩티드 호르몬으로, 내분비 및 외분비 호르몬 분비를 억제하는 주요 조절 인자이다.
이 호르몬은 GH을 포함한 다양한 호르몬의 분비를 억제하며, 세포 증식 억제 작용을 통해 IGF-1에 의해 유도되는 세포 분열 신호를 감소시킨다. 그러나 천연 소마토스타틴은 반감기가 약 1~3분으로 매우 짧고 혈장 및 조직 내 펩티다제에 의해 빠르게 분해되기 때문에 임상적으로 직접 사용하기에는 한계가 있다.
소마토스타틴의 생물학적 효과는 G 단백질 결합 수용체(G protein-coupled receptor, GPCR) 계열인 소마토스타틴 수용체(SSTR1~SSTR5)를 통해 매개된다. 이러한 한계를 극복하기 위해 반감기와 안정성을 개선한 다양한 합성 소마토스타틴 유사체가 개발되었으며, 현재 말단비대증 치료에 사용되는 주요 약물은 다음과 같다.
1세대 소마토스타틴 유사체인 옥트레오티드(octreotide acetate, Sandostatin®)는 1988년 미 FDA 승인을 받은 최초의 SSA로, SSTR2에 높은 친화성을 보이는 것이 특징이다. 이후 치료 편의성을 개선하기 위해 장기 지속형 제형(long-acting release, Sandostatin LAR®)이 개발되어 1998년 미 FDA 승인을 받았으며, 4주 간격으로 근육 주사하는 방식으로 투여된다. 또한 2020년에는 경구용 옥트레오티드 캡슐(Mycapssa®)이 승인되어 주사제 외의 치료 옵션이 추가되었다.
란레오티드(lanreotide)는 고리형 옥타펩타이드 구조의 약물로 1990년대에 개발되었다. 이후 약효 지속 시간을 연장한 서방형 제형이 개발되었으며, 현재는 28일 간격으로 피하 주사하는 장기 지속형 제형(Somatuline®)이 임상에서 널리 사용되고 있다.
2세대 소마토스타틴 유사체인 파시레오티드(pasireotide)는 기존 약물과 비교하여 SSTR1, SSTR3, SSTR5에 대한 높은 친화성을 보이며, 특히 SSTR5에 대한 결합 친화도가 높은 것이 특징이다. 장기 지속형 제형인 파시레오티드 LAR(Signifor LAR®)은 2014년 FDA 승인을 받았으며, 4주 간격으로 근육 주사한다.
말단비대증 환자에서 흔히 발견되는 GH 분비 뇌하수체 선종(소마토트로피노마, somatotroph adenoma)은 주로 SSTR2를 가장 많이 발현하며, SSTR5도 비교적 높은 수준으로 발현되는 것으로 알려져 있다.
이러한 수용체 발현 양상은 소마토스타틴 유사체 치료 반응과 밀접한 관련이 있다. 일반적으로 SSTR2 발현이 높을수록 치료 반응이 우수하게 나타나며, 반대로 발현이 낮은 경우에는 치료 반응이 감소하거나 약물 내성이 나타날 수 있다.
옥트레오티드, 란레오티드, 파시레오티드는 모두 SSTR2에 결합하지만, 파시레오티드는 SSTR5에 대한 친화성이 상대적으로 높은 특징을 가진다. 이러한 수용체 결합 특성의 차이는 환자의 종양 특성과 수용체 발현 양상에 따라 약물 선택에 영향을 미칠 수 있다.
팔투소틴은 어떤 약제인가?
팔투소틴은 비펩타이드(non-peptide) 구조의 소분자 화합물로, 소마토스타틴 수용체 중 SSTR2에 선택적으로 결합하여 작용한다(Figure 3). 말단비대증 환자에서 흔히 나타나는 성장호르몬 분비 뇌하수체 선종은 SSTR2를 높은 수준으로 발현하는 것으로 알려져 있어, 이러한 수용체 선택성은 GH 분비 억제 효과를 유도하는 데 중요한 역할을 한다.
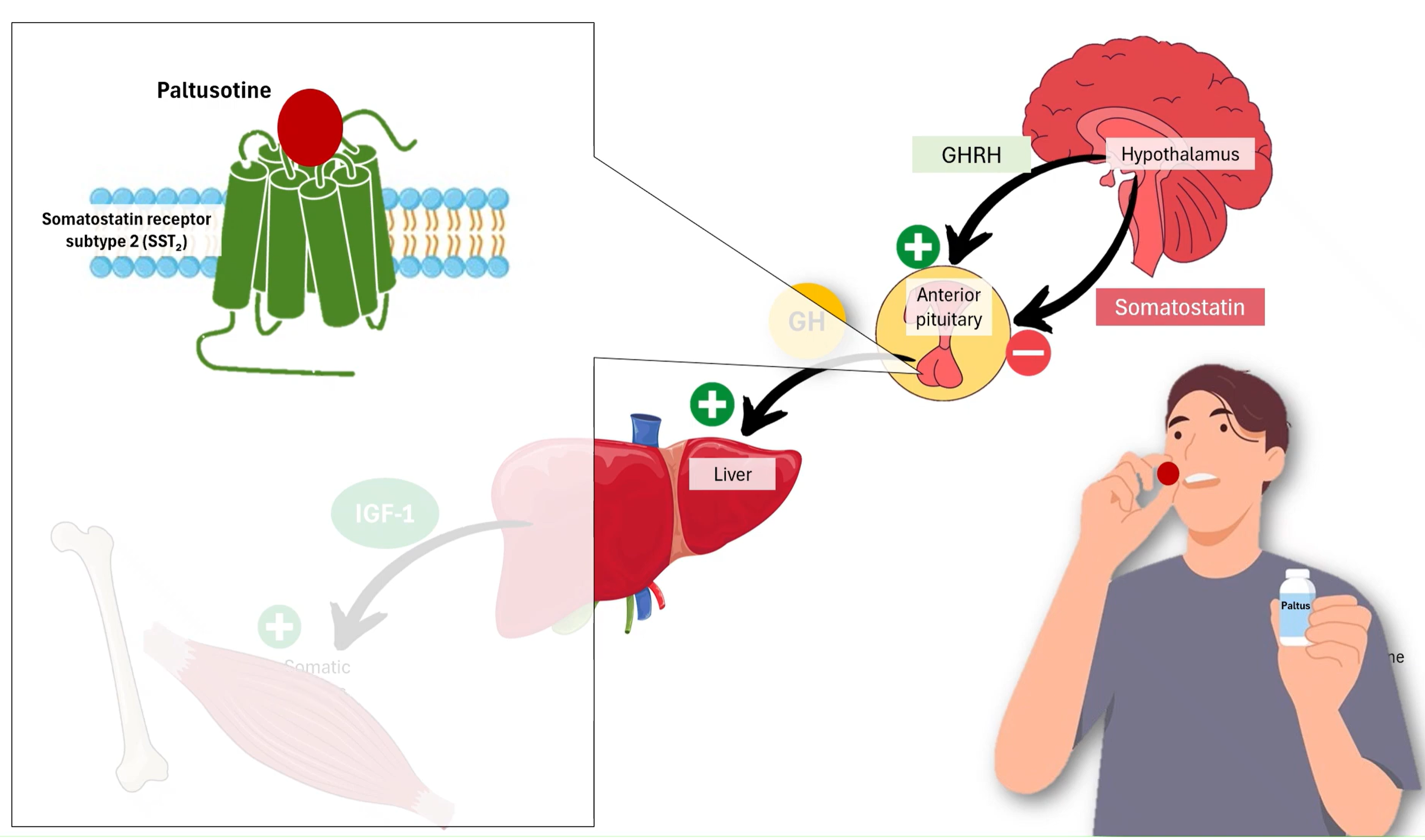
팔투소틴이 SSTR2에 결합하면 세포 내 신호 전달 경로가 변화하여 adenylyl cyclase 활성이 억제되고, 이에 따라 세포 내 cAMP 농도가 감소한다. 동시에 칼슘 채널의 활성은 억제되고 칼륨 채널은 활성화되어 세포막 과분극이 유도되며, 이러한 변화는 뇌하수체 체성장호르몬 분비세포에서 GH 분비를 감소시키는 방향으로 작용한다.
GH 분비가 감소하면 간에서 생성되는 IGF-1의 합성과 분비 역시 감소하게 되며, 결과적으로 말단비대증의 주요 병태생리인 GH–IGF-1 축의 과활성이 억제된다. 이러한 기전을 통해 팔투소틴은 혈중 IGF-1 수치를 감소시키고 말단비대증의 생화학적 조절을 유도한다.
팔투소틴의 또 다른 중요한 특징은 기존 소마토스타틴 유사체와 달리 경구 투여가 가능하다는 점이다. 옥트레오티드, 란레오티드, 파시레오티드와 같은 기존 약물은 펩타이드 구조로 인해 위장관에서 분해되기 쉬워 장기 지속형 주사제로 투여된다.
반면 팔투소틴은 소화 효소에 의해 분해되지 않는 비펩타이드 구조를 가지므로 경구 투여가 가능하며, 일반적으로 하루 1회 복용으로 안정적인 혈중 농도를 유지하도록 설계되었다. 이러한 약리학적 특성은 환자의 치료 순응도를 향상시키고 반복적인 주사 투여에 따른 불편을 줄일 수 있다는 점에서 임상적으로 중요한 의미를 가진다.
또한 임상 연구에서 팔투소틴은 비교적 빠른 시점에 IGF-1 감소 효과를 나타내며, 장기 투여 시에도 생화학적 조절 효과가 유지되는 것으로 보고되었다. 따라서 팔투소틴은 SSTR2 선택적 작용을 기반으로 GH 분비를 억제하고 IGF-1 생성을 감소시키는 경구용 치료제로서, 기존 주사형 소마토스타틴 유사체의 대안 또는 보완적 치료 옵션으로 평가된다.
1상 연구에서는 팔투소틴의 약동학 및 약력학이 평가되었다. 약물은 투여 후 약 1.3~2.2시간 내 최고 혈중 농도에 도달하였으며, 반감기는 약 22~34시간이었다. IGF-1 농도는 투여 약 7일 후 최저 수준에 도달하였고, IGF-1 억제 효과는 5~30mg 범위에서 용량 의존적으로 증가하였다. 다만 40mg에서는 추가적인 억제 효과가 뚜렷하게 나타나지 않았다. 또한 음식과 함께 복용할 경우 약물 흡수가 감소하여 최대 혈중 농도가 약 7배 감소하는 것으로 보고되었다.
2상 연구인 ACROBAT Edge에서는 기존 소마토스타틴 수용체 리간드(SRL) 치료를 받던 말단비대증 환자에서 팔투소틴 단독요법의 효과와 안전성이 평가되었다. 총 47명의 환자가 참여하였으며, 팔투소틴은 10mg에서 시작하여 최대 40mg까지 증량하며 하루 1회 투여하였다. 13주 치료 후 일부 환자에서는 IGF-1 변화가 제한적이었으나, 전반적으로 내약성은 양호하였고 두통, 관절통, 무력감이 가장 흔한 이상반응으로 보고되었다.
ACROBAT Evolve 연구는 이중맹검, 위약 대조, 무작위 배정 방식의 2상 연구로 설계되었으나, 이전 연구 결과가 긍정적으로 나타남에 따라 조기 종료되었다. 연구 종료 시점까지 13명의 환자가 등록되었으며, 이들은 주로 안전성 분석에 포함되었다.
팔투소틴(PALSONIFY)에 대한 허가 임상은 어떠한가?
Study 1(PATHFNDR-2): 소마토스타틴 유사체 치료 경험이 없거나 이전에 치료받은 말단비대증 성인 대상 연구
Study 1은 생화학적으로 조절되지 않는 말단비대증(acromegaly)을 가진 성인 환자를 대상으로 수행된 임상시험으로, 총 111명의 참가자가 등록되었다. 참가자들은 치료 경험에 따라 세 그룹으로 구성되었는데, 치료 경험이 없는 환자가 46명, 스크리닝 전 4개월 동안 어떠한 치료도 받지 않은 환자가 36명으로 이 두 집단은 ‘비약물 치료군(Not Medically Treated)’으로 분류되었으며, 소마토스타틴 수용체 유사체(somatostatin receptor analog) 치료를 받은 후 스크리닝 기간 동안 약물 중단(washout)을 거친 환자 29명은 ‘Washout 군’으로 분류되었다. 등록 시 참가자의 평균 연령은 47세(범위 18~80세)였고 여성의 비율은 53%였다.
말단비대증 진단 이후 경과 기간의 평균은 87개월이었으며, 연구 참여 이전에 95%의 환자가 뇌하수체 수술을 받은 병력이 있었고 수술 후 연구 참여까지의 평균 기간은 78개월이었다. 종양의 크기 분포를 보면 거대선종(macroadenoma, 10mm 초과)이 86명(78%)으로 가장 많았고, 미세선종(microadenoma, 10mm 이하)은 9명(8%), 종양 크기가 확인되지 않은 환자는 16명(14%)이었다.
연구 등록 기준에서 ‘비약물 치료군’은 스크리닝 시 IGF-1 수치가 정상 상한치(upper limit of normal, ULN)의 1.3배 이상이어야 했으며, ‘Washout 군’의 경우 스크리닝 시 IGF-1 수치가 ULN 이하(≤1.0×ULN)이고 약물 중단 이후 IGF-1 수치가 최소 30% 이상 상승하면서 1.1×ULN 이상을 나타내야 했다. 모든 참가자는 무작위 배정을 통해 PALSONIFY 투여군(n=54) 또는 위약군(n=57)으로 배정되어 총 24주 동안 치료를 받았다.
<용량>
투여 용량은 초기 20mg을 1일 1회 투여하는 것으로 시작하였으며, 2주 후 40mg으로 증량하였다. 치료 초기 12주 동안은 IGF-1 수치를 기준으로 용량을 조절할 수 있었으며, 40mg에서 최대 60mg까지 증량이 가능하였다. 12주 이후에는 연구의 무작위 대조 기간이 종료되는 24주까지 동일 용량을 유지하도록 하였다.
또한 약물의 내약성에 따라 연구 기간 중 언제든지 용량을 감량할 수 있도록 허용되었다. 연구 중 IGF-1 수치 상승과 임상 증상으로 말단비대증이 충분히 조절되지 않는 것으로 판단되는 경우 표준 치료(rescue therapy)를 시행하도록 하였으며, 전체 참가자 중 14명(13%)이 구조 치료를 받았다. 이 중 PALSONIFY 투여군에서는 1명(2%)이 구조 치료를 받았고, 위약군에서는 13명(23%)이 구조 치료를 받았다.
<유효성 평가 및 결과>
본 연구의 1차 평가 변수(primary endpoint)는 IGF-1 수치가 정상 상한치 이하(≤1.0×ULN)로 감소하여 생화학적 조절(biochemical control)을 달성한 환자의 비율이었다. 24주 치료 후 평가 결과, PALSONIFY 투여군의 56%가 생화학적 조절을 달성한 반면 위약군에서는 5%만이 해당 기준을 충족하였다. 이러한 차이는 통계적으로 유의하였으며(p<0.0001), PALSONIFY가 위약 대비 말단비대증 환자의 IGF-1 수치 조절에 있어 유의하게 높은 치료 효과를 나타냄을 보여주었다(Table 5).

Study 1에서 IGF-1 정상화를 달성한 참가자들의 대부분은 치료 시작 후 2~4주 이내에 이러한 반응을 보였으며, 이후 치료 기간 종료 시점까지 그 효과가 지속적으로 유지되었다. 또한 1차 유효성 평가 변수에 대해 사후 분석(post hoc subgroup analysis)이 수행되었는데, 이는 이전 약물 치료 경험과 반응 여부에 따라 참가자들을 두 하위 그룹으로 구분하여 반응률을 평가한 것이다.
그룹 A(Group A)는 이전에 의학적 치료를 받은 적이 없거나, 이전 약물 치료에도 불구하고 생화학적 조절을 달성하지 못했거나, 이전 치료에서의 생화학적 조절 여부가 확인되지 않은 참가자들로 구성되었다.
반면 그룹 B(Group B)는 이전 약물 치료에서 반응을 보였던 참가자들로, 기저 시점 이전에 기존 치료를 중단(washout)한 경우이거나 이전 약물 치료에서 생화학적 조절이 문서화되어 확인된 환자들로 구성되었다. 이와 같은 하위군 분석 결과는 아래에 제시되어 있다(Table 6).

Study 1에서 PALSONIFY를 투여받은 참가자들은 말단비대증과 관련된 증상의 중증도 점수에서 위약군과 비교하여 전반적으로 더 낮은 수치를 보였다. 이러한 증상 평가는 환자 보고형 증상 중증도 평가 도구(patient-reported symptom severity instrument)를 이용하여 측정되었으며, 두통, 관절 통증, 발한, 피로, 쇠약감, 부종, 그리고 저림 또는 감각 이상과 같은 증상들을 포함하여 평가되었다.
Study 2(PATHFNDR-1): 소마토스타틴 유사체로 이전에 조절되었던 말단비대증 성인 환자 대상 연구
Study 2는 기존에 소마토스타틴 유사체 치료로 생화학적으로 조절되었던 말단비대증(acromegaly) 성인 환자를 대상으로 수행된 임상시험으로, 총 58명의 참가자가 등록되었다.
본 연구에 포함된 참가자들은 스크리닝과 무작위 배정 시점 모두에서 IGF-1 수치가 정상 상한치(ULN)의 1.0배 이하(≤1.0×ULN)로 유지되어 생화학적 조절 상태가 확인된 환자들이었으며, 이전에 주사형 데포 옥트레오타이드(octreotide) 또는 라네오타이드(lanreotide) 소마토스타틴 유사체 제제로 치료를 받고 있었다. 등록 시 참가자의 평균 연령은 55세(범위 29~84세)였고 여성의 비율은 55%였다.
말단비대증 진단 이후 경과 기간의 평균은 155개월이었다. 연구 참여 이전에 86%의 참가자가 뇌하수체 수술을 받은 병력이 있었으며, 수술 후 연구 참여까지의 평균 기간은 138개월이었다. 종양 크기 분포를 보면 거대선종(macroadenoma, 10mm 초과)이 33명(57%)이었고, 미세선종(microadenoma, 10mm 이하)은 11명(19%), 종양 크기가 확인되지 않은 환자는 14명(24%)이었다. 참가자들은 무작위 배정을 통해 PALSONIFY 투여군(n=30) 또는 위약군(n=28)에 배정되었으며, 총 36주 동안 치료를 받았다.
<용량>
투여 용량은 초기 40mg으로 시작하였으며, 치료 첫 24주 동안 IGF-1 수치를 기준으로 40mg에서 최대 60mg까지 용량을 조절할 수 있도록 하였다. 24주 이후에는 연구의 무작위 대조 기간 종료 시점인 36주까지 동일 용량을 유지하였다. 또한 약물의 내약성에 따라 연구 기간 중 언제든지 용량을 감량할 수 있도록 허용되었다. 연구 기간 동안 IGF-1 수치 상승 및 임상 증상으로 말단비대증이 조절되지 않는 것으로 판단되는 경우 표준 치료(rescue therapy)를 시행하도록 하였으며, 전체 참가자 중 18명(31%)이 구조 치료를 받았다. 이 중 PALSONIFY 투여군에서는 1명(3%)이 구조 치료를 받았고, 위약군에서는 17명(61%)이 구조 치료를 받았다.
<유효성 평가 및 결과>
본 연구의 1차 평가 변수(primary endpoint)는 PALSONIFY 투여군에서 생화학적 반응 유지(biochemical response maintenance), 즉 IGF-1 수치가 정상 상한치 이하(≤1.0×ULN)로 유지된 참가자의 비율을 위약군과 비교하여 평가하는 것이었다. 36주 치료 후 평가 결과, PALSONIFY 투여군의 83%가 생화학적 조절 상태를 유지한 반면 위약군에서는 4%만이 해당 기준을 유지하였다.
이러한 차이는 통계적으로 유의하였으며(p<0.0001), PALSONIFY가 기존 소마토스타틴 유사체 치료로 조절되던 말단비대증 환자에서 생화학적 조절 상태를 유지하는 데 있어 위약 대비 유의하게 높은 효과를 나타냄을 보여주었다(Table 7).
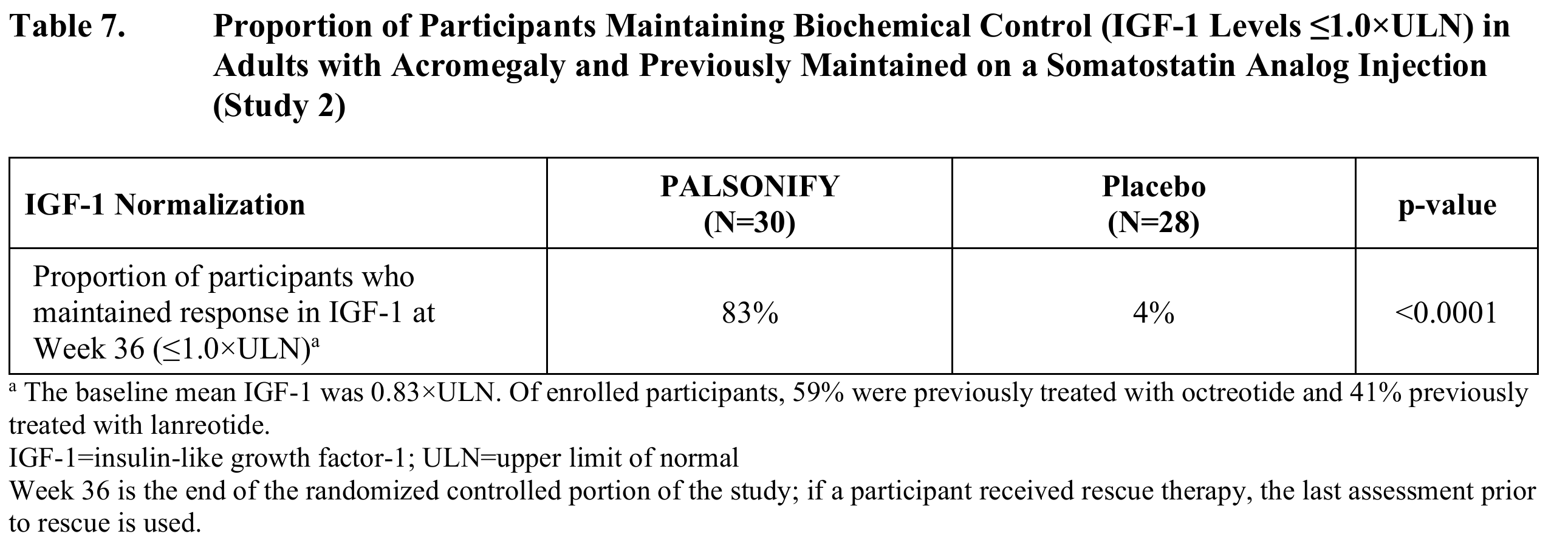
Study 2에서 PALSONIFY를 투여받은 참가자들은 말단비대증과 관련된 증상 중증도 점수에서 위약군과 비교하여 전반적으로 더 낮은 수치를 보였다. 이러한 증상 평가는 환자 보고형 증상 중증도 평가 도구(patient-reported symptom severity instrument)를 사용하여 측정되었으며, 두통, 관절 통증, 발한, 피로, 쇠약감, 부종, 그리고 저림 또는 감각 이상 등의 증상을 포함하여 평가되었다.
팔투소틴 장점 단점 허가 임상 문제점 추후 쟁점은?
팔투소틴은 말단비대증 치료를 위해 개발된 경구용 소마토스타틴 수용체 작용제로, 기존의 주사형 소마토스타틴 유사체 치료의 한계를 보완하기 위한 새로운 치료 옵션으로 평가되고 있다. 이 약물은 특히 SSTR2에 선택적으로 결합하여 뇌하수체 성장호르몬 분비세포에서 GH 분비를 억제하고, 그 결과 간에서 생성되는 IGF-1의 생성을 감소시키는 기전을 통해 말단비대증의 생화학적 조절을 유도한다. 기존 치료제와 비교했을 때 팔투소틴의 가장 큰 장점은 경구 투여가 가능하다는 점이다.
현재 표준적으로 사용되는 소마토스타틴 유사체인 옥트레오티드, 란레오티드, 파시레오티드는 대부분 장기 지속형 주사제 형태로 4주 간격의 근육 또는 피하 주사가 필요하다. 이러한 주사 치료는 환자에게 통증과 불편을 유발할 수 있으며 의료기관 방문이 필요하다는 단점이 있다.
반면 팔투소틴은 비펩타이드 구조의 소분자 약물로 설계되어 경구 투여가 가능하며 일반적으로 하루 1회 복용으로 치료가 가능하다는 점에서 환자의 치료 순응도와 편의성을 높일 수 있는 장점을 가진다. 또한 임상시험 결과에서 기존 소마토스타틴 유사체 치료를 받던 환자에서 IGF-1 조절을 유지하거나 치료 경험이 없는 환자에서도 생화학적 조절을 유도할 수 있는 효과가 보고되어 새로운 치료 대안으로서의 가능성이 제시되었다.
그러나 이러한 장점에도 불구하고 몇 가지 한계와 잠재적인 단점이 존재한다. 우선 기존 주사형 소마토스타틴 유사체는 수십 년간 임상에서 사용되어 안전성과 효과에 대한 장기 데이터가 축적되어 있는 반면, 팔투소틴은 비교적 최근 개발된 약물로 장기적인 안전성 및 효과에 대한 데이터가 아직 충분히 축적되지 않았다는 점이 한계로 지적된다.
또한 경구 약물의 특성상 음식 섭취, 위장관 흡수, 약물 상호작용 등의 영향을 받을 가능성이 있으며, 환자의 복약 순응도에 따라 약물 효과가 달라질 수 있다는 점도 고려해야 한다. 일부 환자에서는 기존 소마토스타틴 유사체에 비해 충분한 IGF-1 억제 효과가 나타나지 않을 가능성도 제기되고 있으며, 특히 SSTR2 발현이 낮은 종양에서는 치료 반응이 제한될 수 있다.
팔투소틴의 허가 과정은 말단비대증 환자를 대상으로 한 여러 임상시험 결과를 기반으로 진행되었다. 대표적으로 생화학적으로 조절되지 않은 말단비대증 환자를 대상으로 한 무작위 대조 임상시험에서는 약물 투여군에서 위약군보다 유의하게 높은 IGF-1 정상화 비율이 나타났다.
또한 기존 주사형 소마토스타틴 유사체로 조절되던 환자를 대상으로 한 연구에서도 팔투소틴으로 전환 후 IGF-1 조절 상태가 유지되는 결과가 보고되었다. 이러한 임상 결과를 바탕으로 팔투소틴은 말단비대증 치료를 위한 새로운 경구 치료제로 허가 절차가 진행되었으며, 일부 국가에서는 이미 허가 또는 승인 절차가 이루어지고 있다.
임상적으로 제기되는 문제점으로는 환자군에 따른 치료 반응의 차이, 기존 소마토스타틴 유사체와의 직접 비교 연구 부족, 그리고 장기 치료 시 종양 크기 변화에 대한 충분한 데이터가 아직 제한적이라는 점이 있다. 기존 주사형 소마토스타틴 유사체는 GH 억제뿐만 아니라 일부 환자에서 뇌하수체 종양 크기를 감소시키는 효과가 보고되어 왔는데, 팔투소틴이 이러한 종양 억제 효과를 동일하게 나타낼 수 있는지에 대해서는 추가적인 연구가 필요하다. 또한 약물 비용과 건강보험 적용 여부 역시 실제 임상 적용에서 중요한 요소로 고려될 수 있다.
향후 연구 및 임상에서 논의될 추후 쟁점으로는 팔투소틴의 장기 안전성과 효과에 대한 추가적인 임상 데이터 확보, 기존 소마토스타틴 유사체 및 다른 약물 치료와의 비교 연구, 병합 치료 전략에서의 역할 등이 있다. 또한 어떤 환자군에서 팔투소틴이 가장 효과적인지에 대한 환자 선택 기준(patient selection)을 확립하는 것도 중요한 과제가 될 것으로 보인다.
특히 SSTR 발현 양상, 종양 특성, 기존 치료 반응 등을 고려한 개인 맞춤형 치료 전략에서 팔투소틴의 위치를 규명하는 것이 향후 연구의 중요한 방향이 될 것으로 예상된다. 이러한 점을 종합하면 팔투소틴은 말단비대증 치료에서 새로운 경구 치료 옵션으로서 의미 있는 잠재력을 가지지만, 장기적인 임상 경험과 추가 연구를 통해 그 역할과 한계가 보다 명확하게 규명될 필요가 있다.
참고문헌
1. Charles P. Daniel et al. “Acromegaly: Pathophysiological Considerations andTreatment Options Including the Evolving Role of OralSomatostatin Analogs” Pathophysiology 2023, 30,377–388.
2. Philippe Chanson et al. “Acromegaly” Orphanet Journal of Rare Diseases 2008, 3:17).
3. Justine Cristante et al. “New treatments for acromegaly: Is a revolution underway?” nnales d’Endocrinologie 86 (2025) 101710.
4. Jie Zha et al. “Prospect of acromegaly therapy: molecularmechanism of clinical drugs octreotide andpaltusotine” Nature Communications (2023) 14:962.
5. Erika Peverelli et al. “Dopamine and SomatostatinAnalogues Resistance of PituitaryTumors: Focus on Cytoskeletoninvolvement” Front. Endocrinol. (2015) 6:187.
6. Agnieszka Milewska-Kranc et al. “The Role of Receptor–Ligand Interaction in SomatostatinSignaling Pathways: Implications for Neuroendocrine Tumors” Cancers 2024, 16, 116.
7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).
관련기사
-
㉓최초의 PDE4B 선택적 억제제 '네란도밀라스트'
2026-03-06 06:00
-
㉒인간 유래 FcRn 억제 단클론항체 '니포칼리맙'
2026-02-20 06:00
-
㉑새 기전의 만성 자발성 두드러기 치료제 '레미브루티닙'
2026-02-06 06:00
-
⑳ 수제트리진, 새로운 기전의 비마약성 진통제
2026-01-16 10:23
-
⑲ GIFT 지정된 PBC 새로운 치료제 '셀라델파'
2026-01-02 06:00
- 익명 댓글
- 실명 댓글
- 댓글 0
- 최신순
- 찬성순
- 반대순
















 응원투표
응원투표 
































![[노보노디스크] 위고비](https://cdn.platpharm.co.kr/static/dailypharm/Wigobi.png)
![[유한양행] 마그비 시리즈](https://cdn.platpharm.co.kr/2024/03/2403261023280000193.jpg)
![[리쥬올] PDLLA 퍼밍 크림 30ml](https://cdn.platpharm.co.kr/2026/04/2604070229110000386.webp)
![[옵투스] 오에수 시리즈](https://cdn.platpharm.co.kr/2026/02/2602130209000031633.webp)
![[일양약품] 프로엑스피](https://cdn.platpharm.co.kr/2026/01/2601221008450010125.webp)
![[신신제약] 모스키토 밀크](https://cdn.platpharm.co.kr/2025/10/2510150733400004067.webp)
![[종근당] 브레이닝캡슐](https://cdn.platpharm.co.kr/2025/06/2506040708450012544.png)
![[일양약품] 도담도담 시리즈](https://cdn.platpharm.co.kr/2024/02/2402020935180000240.jpg)
![[유한양행] 안티푸라민 파스 시리즈](https://cdn.platpharm.co.kr/2024/05/2405280631070000069.png)
![[삼진제약] 게보핏 시리즈](https://cdn.platpharm.co.kr/2024/07/2407100728250000386.png)
![[신신제약] 아렉스마일드](https://cdn.platpharm.co.kr/2023/11/2311300927130000133.jpg)
![[경방신약] 방콜브이산](https://cdn.platpharm.co.kr/2025/12/2512310630020002495.webp)
![[쥬베룩] 진짜 쥬베룩을 담은 약국전용 PDLLA 크림](https://i.baropharm.com/products/202604/1775343960671.png?label=바뷰페로고)
![[레비온] PDRN+EGF, 레비온RX PDRN EGF 크림](https://i.baropharm.com/products/202512/1765949426601.png)
![[리쥬올] 닥터 리쥬올 어드밴스드 PDRN 리쥬비네이팅 크림 30ml](https://i.baropharm.com/partner/products/a201d2b4-f21e-4b13-957c-846d286b3d21.jpg?label=바뷰페로고)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/partner/products/3f39593e-6318-4dd9-a778-c008c868b5c8.png)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202604/1776750298620.png)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[경동제약] 인태반 자양강장제, 파워콤프](https://i.baropharm.com/partner/products/0a2cbb4c-96c5-40a5-aec2-8beeae11682c.png)
![[CHD제약] 50년 전통의 천혜당 식염포도당](https://i.baropharm.com/products/202604/1775095858899.png)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
![[알엑스미] 알엑스미 리쥬영 울트라 PDRN 10000 딥리페어 크림](https://i.baropharm.com/partner/products/70c72dd0-cfd3-4d80-87e4-dc4f8de6658b.png?label=바뷰페로고)



