㉕돋보기 대신 노안 치료 복합점안제 '유브지'
- 최병철 박사
- 2026-04-03 06:00:54
-
가
- 가
- 가
- 가
- 가
- 가
- 최병철 박사의 노벨드럭 인사이트
- 수술과 달리 비침습·가역적 치료 유의미
- 두통 다빈도 보고...저조도 환경 추가 평가 필요
- PR
- 잘 나가는 약국은 매달 보는 신제품 정보 ‘팜노트’
- 팜스타클럽

유브지(YuvezziⓇ, 카르바콜 및 브리모니딘 타르트레이트 점안액 2.75%/0.1%, Tenpoint Therapeutics)는 올해 1월 미국 FDA에서 성인의 노안(presbyopia) 치료제로 승인된 복합 점안제이다. 이 약은 부교감신경 작용제인 카르바콜(carbachol)과 알파 교감신경 수용체 작용제인 브리모니딘(brimonidine)을 결합한 제제이다.
노안은 눈이 점차 가까운 사물을 선명하게 보는 능력을 잃는 현상이다. 일반적으로 40세 이후부터 증상이 나타나며, 책을 읽을 때 글씨를 더 멀리 떨어뜨려야 잘 보이게 된다.
눈 안쪽에는 색깔 있는 홍채 뒤에 투명한 수정체가 있다. 수정체는 모양을 바꾸어 빛을 망막에 집중시켜 시각을 형성한다. 젊은 시기에는 수정체가 부드럽고 유연하여 쉽게 형태를 변화시킬 수 있어 가까운 물체와 먼 물체 모두에 초점을 맞출 수 있다. 그러나 40세 이후에는 수정체가 점차 단단해져 형태 변형이 어려워지고, 이로 인해 근거리 작업이 어려워진다.
노화로 인해 발생하는 노안을 완전히 멈추거나 되돌릴 방법은 없다. 다만 안경, 콘택트렌즈, 약물, 수술 등을 통해 교정할 수 있다. 노안을 교정하지 않으면 두통이나 눈의 피로가 나타날 수 있다.
유브지는 기존에 녹내장 치료제로 사용되던 카르바콜과 브리모니딘 타르트레이트를 결합하여 노안 치료제로 개발된 약물이다. 카르바콜은 동공 수축 작용을 하고, 브리모니딘 타르트레이트는 동공 확장을 억제한다. 두 성분을 함께 사용하면 핀홀 효과(pin hole effect)가 발생하여 동공 크기가 줄어들고, 중심부에 초점을 맞춘 빛만 눈으로 들어오게 된다. 그 결과 초점 심도가 증가하고 근거리 및 원거리 시야가 모두 선명해진다.
유브지의 FDA 승인은 두 건의 3상 임상시험 결과를 기반으로 이루어졌다. BRIO I 연구에서는 복합요법이 각 단일 성분보다 우수한 효과를 보였으며, 이는 고정용량 복합제 승인 요건을 충족한 것이다.
BRIO II 연구에서는 모든 주요 근거리 시력 개선 지표를 달성하였고, 8시간 동안 양안 나안 근거리 시력(BUNVA)에서 통계적으로 유의한 3줄 이상의 시력 향상이 확인되었다. 또한 양안 나안 원거리 시력(BUDVA)에서는 1줄 이상의 시력 저하가 나타나지 않았다.
유브지는 하루 1회, 각 눈에 1방울씩 점안하는 방식으로 사용한다. 사용 시 주의사항으로는 시야 흐림, 망막 박리 위험, 홍채염, 혈관 기능 부전 악화 등이 있다. 흔한 이상반응(발생률 5% 이상)으로는 점안 시 안구 통증, 시력 저하, 점안 시 자극감, 두통 등이 보고되었다.
노안(Presbyopia)이란 무엇인가?
노안은 연령 증가에 따라 발생하는 생리적 시기능 저하로, 근거리 시력 감소를 특징으로 하는 대표적인 노화 관련 안과 질환이다. 일반적으로 40대 중반 이후부터 증상이 나타나며, 이는 조절능력(accommodation)의 점진적인 감소와 밀접하게 연관된다. 노안은 전 세계적으로 높은 유병률을 보이며, 삶의 질과 시각 기능에 중요한 영향을 미친다.
노안의 주요 병태생리 기전은 수정체의 경화(lens sclerosis)와 탄성 감소로 설명된다. 정상적인 조절 과정에서 수정체는 모양체근(ciliary muscle)의 수축과 이완에 따라 곡률을 변화시켜 다양한 거리의 물체에 초점을 맞춘다.
연령 증가에 따라 수정체 단백질(주로 crystallin)의 변성과 축적, 그리고 단백질 간 교차결합(cross-linking)이 증가하면서 수정체는 점차 단단해진다. 이러한 변화는 수정체의 변형 능력을 제한하여 조절 시 충분한 곡률 변화를 유도하지 못하게 한다. 결과적으로 근거리 초점 형성이 어려워지고, 근거리 시력 저하가 발생하게 된다.
또한 수정체의 두께 증가와 핵(nucleus) 부위의 밀도 증가 역시 중요한 요인으로 작용한다. 수정체는 평생에 걸쳐 새로운 섬유가 축적되는 구조를 가지므로, 나이가 들수록 중심부가 압축되고 경화되는 경향을 보인다. 이러한 구조적 변화는 광학적 특성에도 영향을 미쳐 굴절력 조절의 유연성을 감소시킨다.
한편, 모양체근의 기능 변화에 대한 연구도 진행되어 왔으나, 다수의 연구에서는 모양체근의 수축 능력은 비교적 유지되는 반면, 경화된 수정체가 이에 충분히 반응하지 못하는 것이 주요 문제로 보고된다. 이는 노안이 근육 기능 저하보다는 수정체 자체의 기계적 제한에 의해 주로 발생하는 질환임을 시사한다.
동공 또한 시각 기능에 영향을 미치는 요소로, 동공 크기의 변화는 초점 심도(depth of focus)를 조절하여 시력에 간접적인 영향을 준다. 특히 동공 수축은 핀홀 효과를 통해 근거리 시력을 일부 보완할 수 있으나, 이는 노안의 근본적인 병태를 해결하는 것은 아니며 보조적인 역할에 해당한다.
임상적으로 노안은 근거리 작업 시 흐림, 초점 전환의 지연, 눈의 피로, 두통 등의 증상으로 나타난다. 진단은 주로 근거리 시력 검사 및 조절력 평가를 통해 이루어지며, 환자의 연령, 증상, 시각적 요구를 종합적으로 고려하여 평가한다. 치료 전략은 크게 광학적 교정(돋보기, 다초점 렌즈), 수술적 방법, 그리고 약물 치료로 구분된다.
최근 미국 FDA에서 유베지(Yuvezzi) 점안액이 승인되면서 노안 치료에 있어 약물 치료의 중요성이 더욱 부각되고 있다. 약물 치료는 국소적이고 비침습적이며 가역적인 치료 옵션을 제공한다는 점에서 임상적 의의가 크다.
수정체(Lens)는 어떤 기능과 역할을 하는가?
수정체는 안구 내에서 홍채와 유리체 사이에 위치한 투명한 이중볼록(biconvex) 구조로, 시각 형성 과정에서 빛을 굴절시켜 망막에 정확한 상을 맺도록 하는 중요한 역할을 수행한다. 수정체는 각막과 함께 안구의 주요 굴절 매체로 작용하며, 특히 조절을 통해 다양한 거리의 물체에 초점을 맞추는 데 핵심적인 기능을 담당한다.
수정체는 해부학적으로 크게 수정체낭(lens capsule), 수정체상피(lens epithelium), 수정체섬유(lens fibers)로 구성된다. 수정체낭은 수정체를 둘러싸는 탄력성 있는 기저막으로, 수정체의 형태를 유지하고 외부와의 경계를 형성한다. 수정체상피는 전면에 존재하는 단층 세포층으로, 세포 분열과 분화를 통해 새로운 수정체섬유를 지속적으로 생성하는 역할을 한다.
수정체섬유는 수정체의 대부분을 구성하며, 중심부의 핵(nucleus)과 주변부의 피질(cortex)로 구분된다. 이러한 섬유세포는 핵과 세포소기관이 소실된 특수한 구조를 가지며, 이는 빛의 산란을 최소화하고 투명성을 유지하는 데 기여한다.
수정체의 주요 기능은 굴절력 조절과 조절 기능이다. 빛은 각막을 통과한 후 수정체에서 추가적으로 굴절되어 망막에 초점을 형성하게 된다. 특히 근거리 시에서는 모양체근의 수축에 의해 섬모체대(zonules)의 장력이 감소하고, 이에 따라 수정체가 보다 구형으로 변하면서 굴절력이 증가한다. 반대로 원거리 시에서는 모양체근이 이완되어 수정체가 평평해지고 굴절력이 감소한다. 이러한 동적 형태 변화는 수정체의 탄성에 의존하며, 정상적인 시각 기능 유지에 필수적이다.
또한 수정체는 고도로 정렬된 단백질 구조, 특히 crystallin 단백질을 통해 높은 투명성과 굴절률을 유지한다. 수정체는 혈관이 없는 조직으로, 주로 방수(aqueous humor)를 통해 영양분을 공급받고 대사산물을 제거한다. 이러한 무혈관 구조는 광학적 투명성을 유지하는 데 유리하지만, 동시에 산화 스트레스나 단백질 변성에 취약한 환경을 형성하기도 한다.
연령 증가에 따라 수정체는 점진적인 구조적 변화를 겪게 되며, 단백질의 변성 및 축적, 수분 함량 변화, 그리고 섬유 간 결합 증가로 인해 탄성이 감소하고 경화되는 경향을 보인다. 이러한 변화는 조절 기능의 저하로 이어져 노안의 주요 병태생리적 기반이 된다.
따라서 수정체는 정교한 구조적 조직과 생화학적 특성을 바탕으로 투명성과 가변적 굴절력을 유지하며, 시각 형성 및 조절 기능에 핵심적인 역할을 수행한다. 이러한 특성은 정상 시각 기능 유지뿐 아니라 노화 및 질환과 관련된 시기능 변화 이해에 있어 중요한 기초를 제공한다.
노안의 수술적 및 비수술적 치료법은?
노안은 안경이나 콘택트렌즈와 같은 시력 보조 기구를 사용하거나, 각막 또는 수정체에 대한 외과적 수술을 통해 교정할 수 있다. 각 방법에는 장단점이 있으며, 자연적인 조절 기능을 회복하는 것은 현재로서는 불가능하다.
안경에 대한 의존도를 줄이거나 없애는 것이 목표라면, 노안 교정은 근시, 원시, 난시를 포함한 원거리 시력 결함의 교정과 함께 이루어져야 한다. 이러한 교정은 일반적으로 선택된 시술 과정에서 함께 달성된다.
기능적으로 노안 치료법은 주로 교정 가능한 시력 영역에 따라 구분된다. 시력 영역은 근거리(30~40cm), 중간거리(60~80cm), 원거리(1m 이상)의 세 가지로 나눌 수 있다. 목표 굴절률이란 특정 시술을 통해 추가적인 보조 장치 없이 선명한 시력을 얻을 수 있는 범위를 의미한다.
단초점 인공수정체(intraocular lens, IOL)는 한 가지 시력 영역만 교정하는 반면, 다초점 인공수정체는 두 개 이상의 시력 영역을 동시에 교정할 수 있다.
Figure 1은 노안의 비수술적 및 수술적 교정 방법을 도식적으로 나타낸 것으로, 녹색 선은 가까운 물체에서 오는 빛을, 파란색 선은 먼 물체에서 오는 빛을 의미한다.
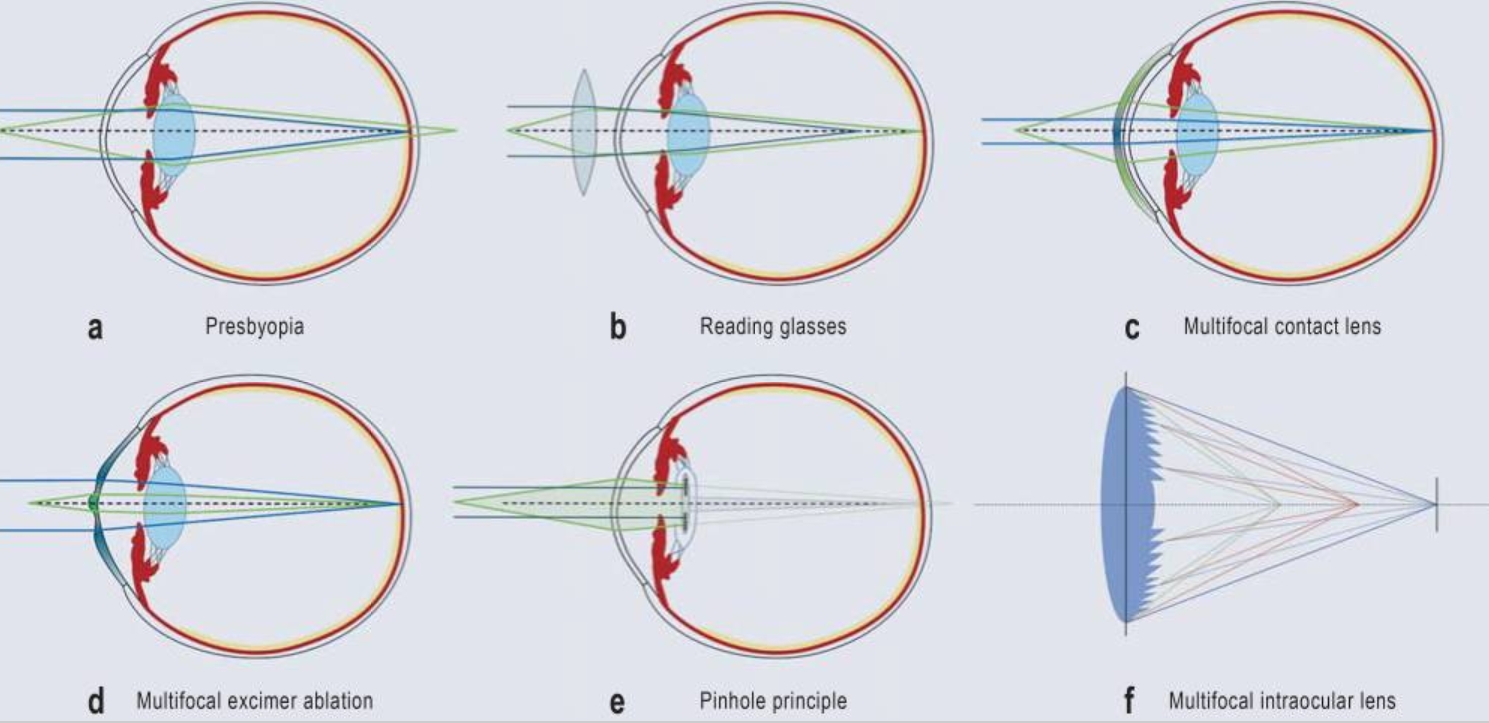
a. 정상적인 눈에서는 멀리 있는 물체가 중심와에 선명하게 초점을 맞추는 것과는 달리, 이 경우에는 눈 전체의 굴절력이 가까이 있는 물체에 선명하게 초점을 맞추기에 충분하지 않다.
b. 볼록 렌즈에 해당하는 돋보기 안경을 사용하면 빛이 더 촘촘하게 모여 가까운 물체는 망막에 선명하게 초점이 맞춰지고, 멀리 있는 물체는 망막 앞쪽에 초점이 맞춰진다.
c. 다초점 콘택트렌즈는 여러 영역으로 구성된다. 예를 들어, 멀리 있는 물체는 렌즈 중앙부를 통해 선명하게 초점이 맞춰지고, 가까이 있는 물체는 굴절률이 더 강한 주변부를 통해 망막에 선명하게 상이 맺힌다.
d. 다초점 엑시머 레이저 절제술은 각막 중심부에 더 강한 굴절 영역을 생성하여 근거리 시력을 향상시키고, 각막 주변부에는 덜 강한 굴절 영역을 생성하여 원거리 시력을 향상시킨다.
e. 핀홀 원리는 눈의 광축에 거의 평행한 빛만 중앙 구멍을 통해 눈으로 들어오게 하여, 서로 다른 거리에 있는 물체가 망막에 선명한 초점을 맺도록 하는 것이다. 이는 부교감신경작동제 점안액이나 중앙에 작은 빛 투과 고리가 있는 인공수정체를 사용하여 구현할 수 있다.
f. 수정체낭에 삽입된 회절형 다초점 인공수정체에 의한 빛의 굴절 및 회절을 나타낸 모식도. 인공수정체는 입사광을 여러 초점으로 나누는 동심원형 회절 영역을 가지고 있다.
동공(Pupil) 크기를 조절하는 주요 요인은 무엇인가?
동공은 눈의 일부로서 망막으로 향하는 빛의 양을 조절하는 조리개 역할을 한다. 따라서 동공 크기의 변화가 망막에 형성되는 이미지에 영향을 미치는 것은 자연스러운 현상이다. 즉 조리개 크기는 눈으로 들어오는 빛의 양과 이미지의 심도에 영향을 준다.
수동 조리개를 사용하는 카메라의 경우를 보면, 조리개를 열면 이미지 센서(망막)에 도달하는 빛의 양은 증가하지만 심도는 얕아진다. 반대로 조리개를 좁히면 센서에 도달하는 빛의 양은 감소하지만 심도는 깊어져 더 넓은 거리 범위의 피사체에 초점을 맞출 수 있다.
또한 동공 크기가 작아지면 렌즈에 닿는 빛의 면적이 줄어들어 렌즈로 인한 광학적 왜곡이 감소하고, 그에 따라 시력이 향상될 수 있다. 따라서 동공이 확장되면 더 많은 빛이 들어와 피사체를 쉽게 감지할 수 있지만 시력의 선명도는 저하될 수 있으며, 반대로 동공이 축소되면 빛의 양은 줄어들지만 더 선명하게 피사체를 구분할 수 있다.
이러한 조절은 주로 홍채의 두 가지 근육, 즉 홍채 괄약근(sphincter pupillae)과 홍채 확장근(dilator iridis 또는 dilator pupillae)의 상호작용을 통해 이루어진다.
동공 크기 조절의 가장 핵심적인 기전은 자율신경계(autonomic nervous system)에 의해 매개된다. 부교감신경계는 동안신경(oculomotor nerve)을 통해 신호를 전달하여 무스카린 수용체를 활성화하고, 이에 따라 홍채 괄약근이 수축하면서 동공 수축(miosis)이 일어난다.
반면 교감신경계는 α-아드레날린 수용체를 통해 홍채 확장근을 자극하여 동공 확장(mydriasis)을 유도한다. 이 두 신경계의 균형은 동공 크기 조절의 기본적인 생리적 기반을 형성한다.
광 자극(Light stimulus)은 동공 크기를 조절하는 가장 직접적인 외부 요인이다. 밝은 환경에서는 망막의 광수용체가 자극되어 동공광반사(pupillary light reflex)가 활성화되고, 이는 부교감신경 경로를 통해 동공 수축을 유도한다. 반대로 어두운 환경에서는 교감신경계의 활성 증가로 동공이 확장되어 더 많은 빛이 망막에 도달하도록 한다.
또한 조절 반응(accommodation response)도 동공 크기에 중요한 영향을 미친다. 근거리 물체를 볼 때 나타나는 조절-수렴-축동(accommodation–convergence–miosis) 반응의 일환으로 동공이 수축하며, 이는 초점 심도를 증가시켜 근거리 시력을 향상시키는 데 기여한다. 이러한 반응은 시각적 선명도를 높이기 위한 생리적 적응 기전으로 이해된다.(Figure 2).
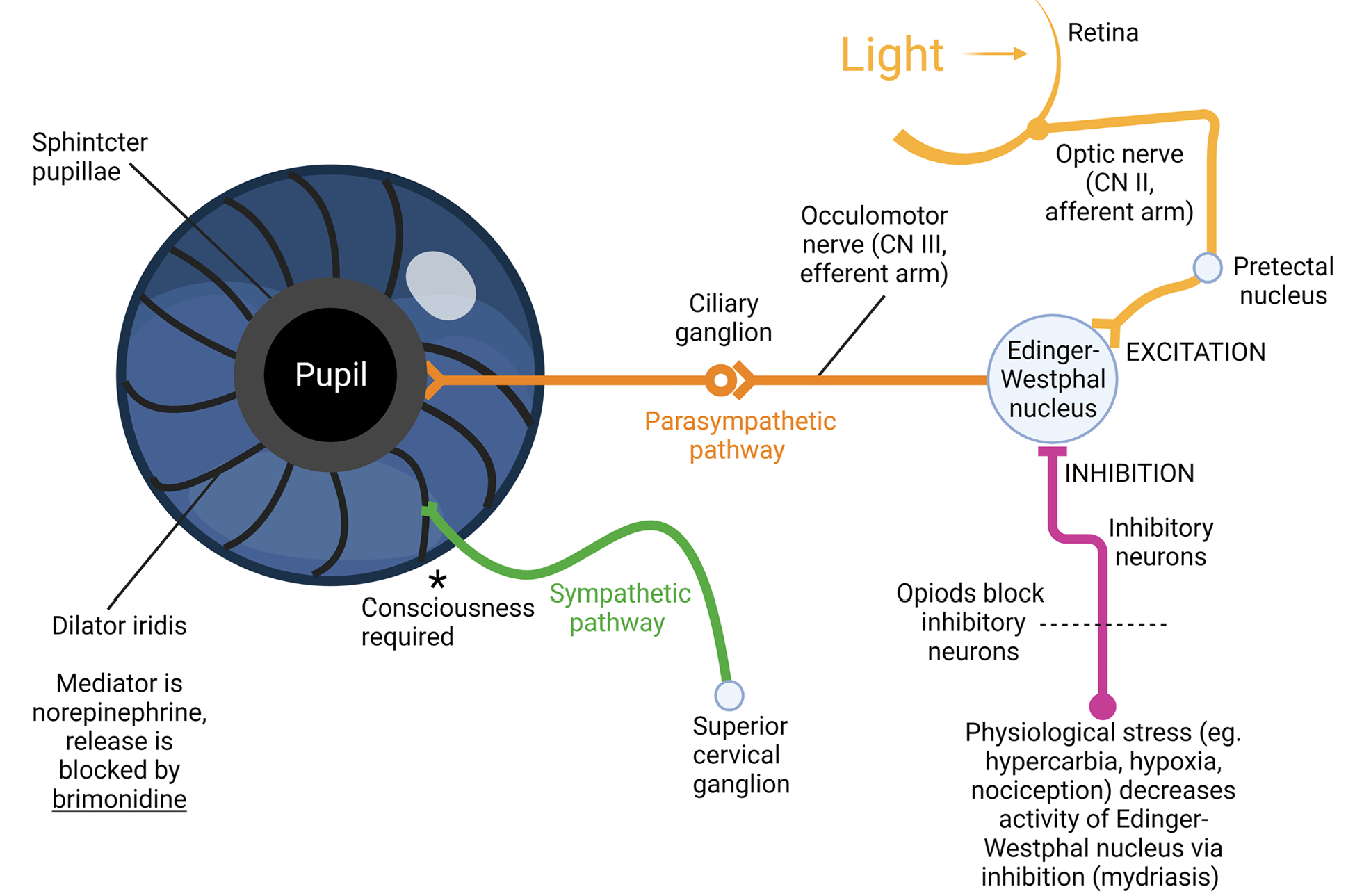
연령(Age) 역시 동공 크기에 영향을 미치는 중요한 요소이다. 일반적으로 나이가 증가함에 따라 동공의 최대 확장 능력이 감소하는 노인성 축동(senile miosis) 현상이 나타난다. 이는 홍채 근육의 반응성 감소와 자율신경 조절 능력의 변화와 관련이 있으며, 야간 시력 저하와도 연관될 수 있다.
이 외에도 약물(drugs)과 전신 상태(systemic conditions)는 동공 크기에 영향을 줄 수 있다. 콜린성 작용제는 동공 수축을 유도하는 반면, 항콜린제나 교감신경 작용제는 동공 확장을 유발한다. 또한 정서적 상태(emotional state), 인지적 부하(cognitive load), 통증 등도 교감신경 활성 변화를 통해 동공 크기에 영향을 미치는 것으로 알려져 있다.
따라서 동공 크기는 자율신경계의 균형, 광 자극, 조절 반응, 연령, 약물 등 다양한 요인의 복합적인 상호작용에 의해 조절된다. 이러한 생리적 기전은 시각 기능 유지에 필수적이며, 특히 노안 치료에서 동공 조절을 표적으로 하는 약물 개발의 중요한 이론적 기반이 된다.
노안에 대한 약물치료에서 축동제(miotic agents)는 어떤 역할을 하는가?
현재 노안 치료용 약물은 크게 두 가지 범주로 나눌 수 있다. 하나는 동공 수축을 유도하여 핀홀 효과를 통해 초점 심도를 증가시키는 약물(miotic agents)이며, 다른 하나는 수정체의 구조적·기능적 보존을 목표로 하는 약물(lenz softer)이다. 그러나 수정체의 생체역학적 특성 회복을 직접적으로 유도하는 약물은 아직 연구 단계에 머물러 있으며, 현재까지 임상적으로 승인된 치료 옵션은 존재하지 않는다.
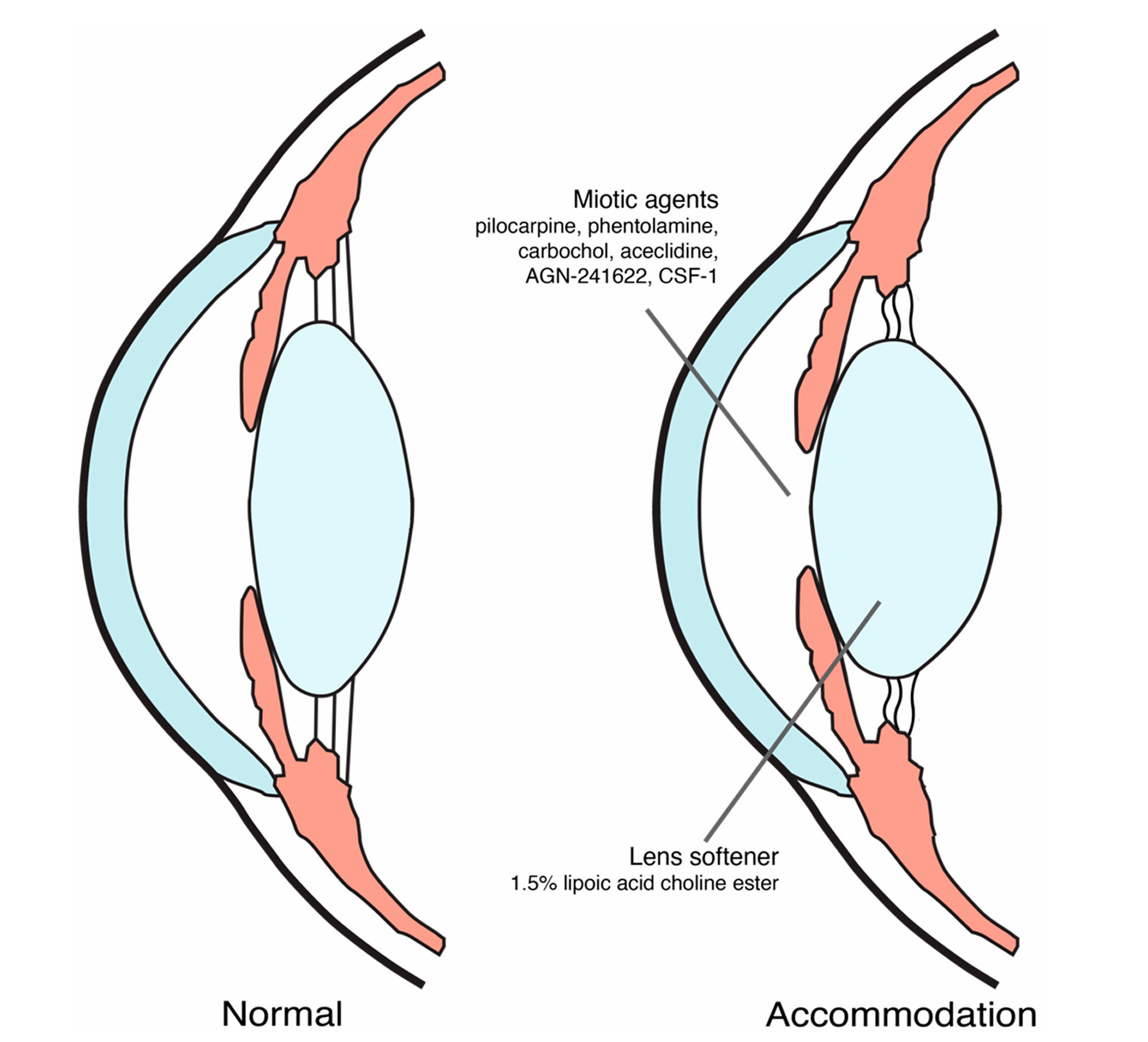
노안은 연령 증가에 따른 수정체의 탄성 감소 및 조절력 저하로 인해 발생하는 생리적 시기능 변화로, 근거리 시력 저하를 주요 특징으로 한다. 최근에는 비침습적 치료 전략으로서 축동제(miotic agents)를 활용한 약물 요법이 주목받고 있으며, 이는 동공 크기 조절을 통한 광학적 원리를 기반으로 한다.
축동제의 주요 작용 기전은 홍채 괄약근에 작용하여 동공 수축(miosis)을 유도하는 것이다. 대표적으로 콜린성 작용제(cholinergic agonists)는 부교감신경계를 활성화하여 동공을 축소시키며, 이로 인해 핀홀 효과(pinhole effect)가 발생한다. 동공이 작아지면 초점 심도(depth of focus)가 증가하고, 주변부 광선의 산란이 감소하여 망막에 도달하는 상의 선명도가 향상된다. 이러한 광학적 변화는 조절력의 감소를 보완하여 근거리 시력을 개선하는 데 기여한다.
현재 대부분의 노안 약물 치료법은 부교감 신경 경로를 통해 초점 심도를 증가시키기 위해 일시적인 동공 축소를 유도하여 핀홀 효과를 내는 것을 목표로 한다.
축동제는 노안 치료를 위해 단독 요법 또는 다른 축동제나 다른 약물과의 병용 요법으로 사용되었다. 대부분은 병용 요법으로 사용되었지만, 단독 요법으로 연구된 약물은 필로카르핀(pilocarpine)과 펜톨아민(phentolamine) 두 가지뿐이었다.
가장 대표적인 축동제는 콜린성 무스카린 수용체 작용제(muscarinic receptor agonist)인 필로카르핀(pilocarpine) 계열이다. 제품으로 부이티(Vuity) 및 클로시(QLOSI)는 M3 무스카린 수용체를 자극하여 홍채 괄약근의 수축을 유도하고 동공 축소(miosis)를 발생시킨다. 이로 인해 핀홀 효과(pinhole effect)가 발생하여 초점 심도(depth of focus)가 증가하고 망막에 도달하는 주변 광선의 산란이 감소하면서 근거리 시력이 개선된다. 동시에 모양체근(ciliary muscle) 수축을 유도하여 일부 조절력 증가를 유발할 수 있으나, 이로 인해 두통이나 눈의 피로와 같은 부작용이 동반될 수 있다.
먼저 부이티(VuityⓇ)는 2021년 최초로 승인된 노안 치료용 점안제로, 주성분인 필로카르핀 1.25%가 동공 수축을 유도한다. 하루 1~2회 점안 시 약 6~10시간 동안 효과가 지속되며, 임상 연구를 통해 근거리 시력 개선 효과가 입증되어 널리 사용되고 있다. 다만 비교적 높은 농도로 인해 일부 환자에서 두통이나 야간 시야 감소가 보고된다.
이후 개발된 클로시(QLOSIⓇ)는 필로카르핀 농도를 0.4%로 낮춘 제제로 2023년에 승인되었다. 하루 1~2회 점안으로 최대 8시간의 효과를 제공하며, 고농도 제제 대비 부작용 발생 가능성을 줄이면서도 유의한 근거리 시력 개선을 목표로 한다. 이러한 저농도 전략은 장기 사용 시 안전성과 내약성을 향상시키기 위한 접근이다.
한편 비즈(VIZZⓇ, LENZ Therapeutics)는 아세클리딘(aceclidine) 1.44%를 기반으로 한 약제로 2025년에 승인되었으며 기존 필로카르핀 계열과는 다른 약리적 특성을 갖는다. 아세클리딘은 홍채 괄약근에 선택적으로 작용하여 동공 수축을 유도하면서 모양체근에 대한 과도한 자극을 상대적으로 줄인다. 이로 인해 조절 경련과 관련된 부작용을 감소시키면서도 근거리 시력 개선 효과를 기대할 수 있다. 이 약제는 2분 간격으로 2방울 점안하는 투여 방식을 사용하며 약효는 최대 10시간까지 지속된다.
최근에는 단일 콜린성 작용을 넘어 복합 기전을 활용한 약제도 승인되었다. 유베지(Yuvezzi)는 콜린성 작용제와 교감신경 억제제를 병용한 복합제병용한 복합제로, 한 성분은 홍채 괄약근을 자극하여 동공 수축을 유도하고 다른 성분은 α-아드레날린 수용체를 억제하여 동공 확장을 방지한다. 이러한 이중 기전은 동공 축소 상태를 보다 안정적으로 유지하여 약효 지속 시간을 연장시키고, 일정한 초점 심도를 유지함으로써 시력의 질적 안정성을 향상시킨다.
이와 같이 노안 치료에 사용되는 축동제는 공통적으로 동공 크기 조절을 통한 광학적 원리를 기반으로 하지만, 성분에 따라 수용체 선택성, 작용 부위, 부작용 프로파일, 지속 시간에서 차이를 보인다. 필로카르핀은 강력한 축동 효과와 함께 조절근 작용을 동반하는 반면, 아세클리딘은 보다 선택적인 작용으로 부작용 감소를 목표로 한다. 또한 복합제는 약효 지속성과 시각적 안정성을 동시에 개선하는 방향으로 발전하고 있다.
따라서 축동제 기반 약물은 노안 치료에서 수정체의 구조적 한계를 보완하는 중요한 비침습적 치료 전략으로 자리잡고 있으며, 향후에는 수용체 선택성 향상과 복합 기전의 최적화를 통해 보다 안전하고 효과적인 치료 옵션으로 발전할 것으로 기대된다.
유브지(카르바콜 및 브리모니딘 타르트레이트 점안액) 2.75%/0.1%)의 약리기전은 어떠한가?
유베지는 노안 치료를 위한 복합 점안제로, 동공 크기 조절을 기반으로 근거리 시력을 개선하는 약리학적 기전을 가진다. 이 약제는 상호 보완적인 두 가지 작용 성분을 통해 동공 수축 유도와 그 지속 효과를 동시에 구현함으로써 기능적 시력 향상을 유도한다(Figure 4).
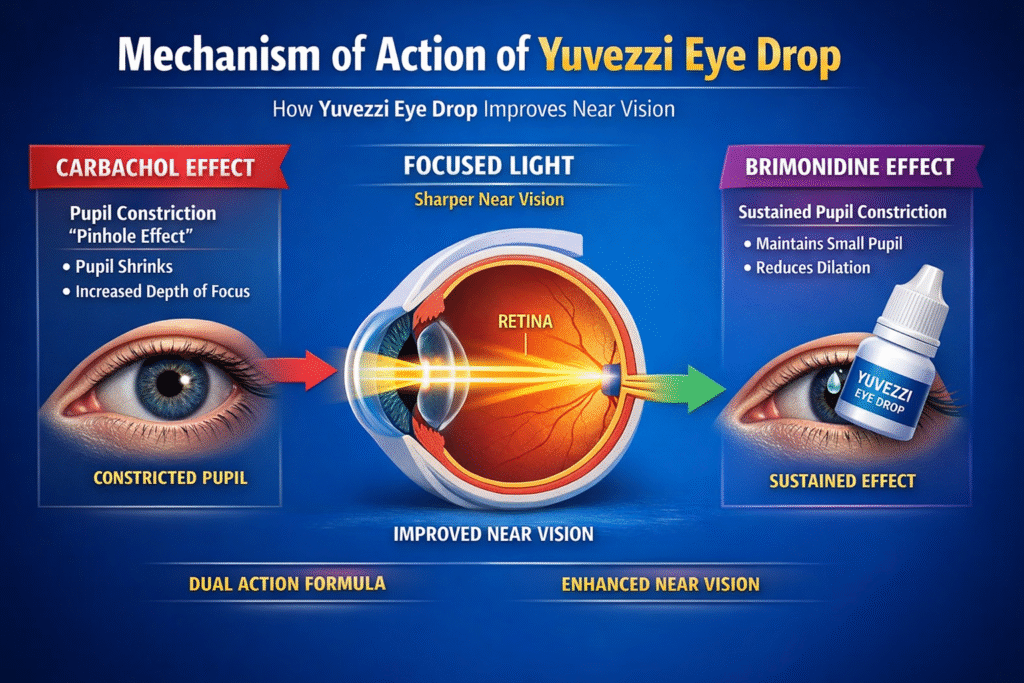
첫째, 카르바콜(carabchol)은 무스카린 수용체와 니코틴 수용체에 작용하는 부교감신경 작용제이다. 필로카르핀이 주로 M3 무스카린 수용체에 선택적으로 작용하는 것과 달리, 카르바콜은 보다 광범위한 수용체 작용을 가지며 강력한 축동 효과를 나타낸다.
또한 카르바콜은 동공 수축을 유도하는 효과가 강하고 지속 시간이 긴 것으로 알려져 있다. 이러한 작용을 통해 홍채 괄약근의 수축을 유도하고 동공 축소를 일으킨다. 동공이 축소되면 핀홀 효과가 발생하여 초점 심도가 증가하고, 망막에 도달하는 주변부 광선의 산란이 감소함으로써 상의 선명도가 향상된다. 그 결과 중심부를 통과하는 광선이 망막에 보다 정확히 초점을 형성하게 되어 근거리 시인성이 개선된다.
둘째, 브리모니딘(brimonidine)은 알파-2 아드레날린 수용체에 선택적으로 작용하는 교감신경 작용제이다. 이 성분은 동공확대근과 관련된 시냅스 전 신경 말단에 작용하여 노르에피네프린 분비를 억제하고, 동공 확장을 유도하는 교감신경 신호를 감소시킨다. 그 결과 동공확대근의 활성이 저하되어 동공 확장이 억제된다. 또한 브리모니딘은 축동제에서 흔히 나타날 수 있는 일부 부작용을 완화하는 데 기여할 가능성이 있다.
카르바콜과 브리모니딘의 병용은 동공 수축 유도와 동공 확장 억제를 동시에 작용시켜 축소된 동공 상태를 보다 안정적으로 유지하도록 한다. 이러한 이중 기전은 단일 작용제 대비 약효 지속 시간을 연장시키며, 수 시간 동안 안정적인 근거리 시력 개선 효과를 가능하게 한다.
이와 같은 복합 기전은 근거리 시력 개선과 원거리 시력 보존 간의 균형을 유지하는 데 중요한 역할을 한다. 즉, 동공을 과도하게 축소하지 않으면서도 충분한 초점 심도 증가를 유도하여 원거리 시력의 유의한 저하 없이 기능적 시력을 향상시키는 것이 특징이다.
따라서 유베지는 동공 크기 조절이라는 광학적 원리를 약리학적으로 구현한 복합제제로, 빠른 작용 발현과 지속 효과를 동시에 제공하며 노안 치료에서 비침습적이고 가역적인 치료 전략을 제시한다.
특히 브리모콜은 작용 기전이 필로카르핀과 유사하거나 더 강력할 수 있어, 동공 수축과 관련된 부작용이 나타날 가능성이 있다. 이에 따라 두통, 시야 흐림, 야간 시야 저하와 같은 이상반응이 발생할 수 있으며, 이러한 안전성을 충분히 평가하기 위해서는 장기간 추적 연구가 필요하다.
유브지(YUVEZZIⓇ)의 허가임상은 어떠한가?
유비지의 노안 치료 효과는 45세에서 80세 사이의 노안 환자를 대상으로 수행된 두 건의 3상(Phase 3), 무작위배정(randomized), 이중눈가림(double-masked), 대조 임상시험인 BRIO I 및 BRIO II 연구를 통해 평가되었다. 두 연구 모두 굴절교정수술 후 환자 및/또는 인공수정체 삽입 환자(pseudophakic)를 포함하였다.
BRIO I 연구는 교차(crossover) 설계로 진행되었으며, 총 182명의 참가자가 등록되어 각 눈에 유비지(YUVEZZI), 카바콜(carbachol), 브리모니딘 타르트레이트(brimonidine tartrate)를 최소 3일의 세척기간을 두고 각각 1회 점안받았다.
이 연구는 복합제인 유비지가 각 단일 활성 성분(monotherapy) 대비 우월성을 가지는지를 평가하기 위해 설계되었다.
한편 BRIO II 연구에서는 총 436명의 참가자가 무작위로 배정되어 각 눈에 유비지 또는 위약(vehicle)을 1회 점안받았으며, 각 군에는 218명씩 포함되었다. 이후 참가자들은 6개월 동안 하루 1회 점안 치료를 지속하였고, 이어서 추가 6개월간 공개연장(open-label extension) 연구에 참여하였다.
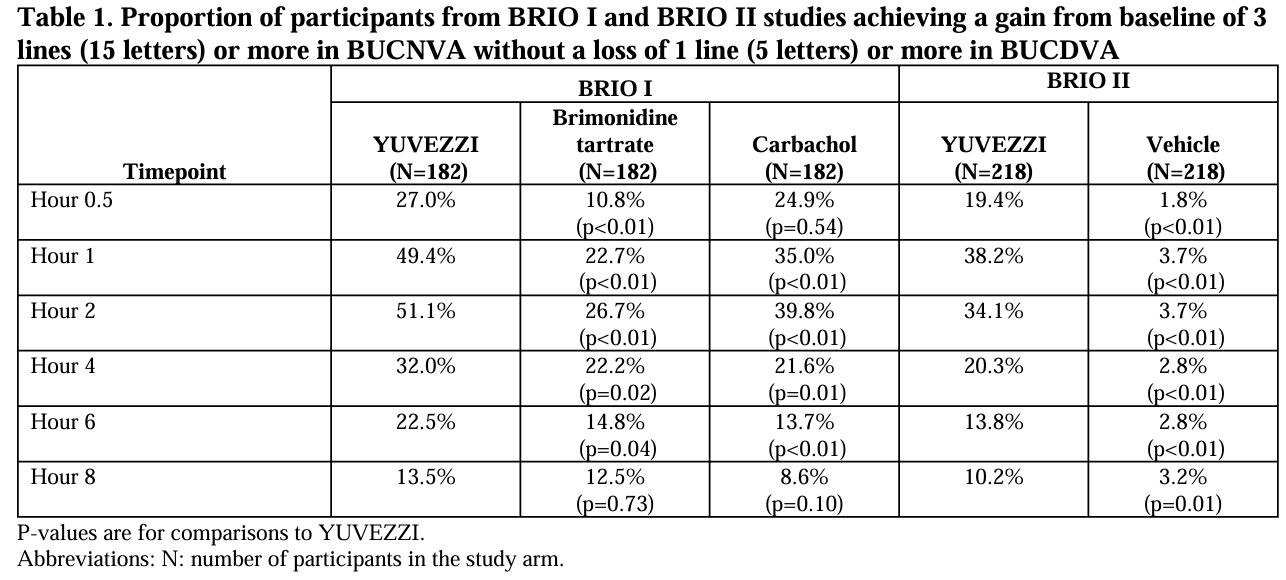
두 연구의 주요 평가 변수는 어두운 환경(메소픽 조건)에서 양안 비교정 근거리 시력(binocular uncorrected near visual acuity, BUCNVA)이 기준치 대비 3줄(15글자) 이상 개선되면서 동시에 양안 비보정 원거리 시력(binocular uncorrected distance visual acuity, BUCDVA)이 1줄(5글자) 이상 감소하지 않는 참가자의 비율로 정의되었으며, 이는 근거리 시력 개선과 원거리 시력 유지라는 임상적 유용성을 동시에 평가하기 위한 복합 지표이다.
두 연구 결과, 유비지는 투여 후 30분 시점부터 효과가 발현되어 최대 8시간까지 지속적인 노안 개선 효과를 나타내었으며, 이러한 결과는 단회 투여뿐 아니라 반복 투여 조건에서도 일관되게 확인되었다(Table 1).
유브즈 허가임상의 문제점은 무엇인가?
BRIO I 및 BRIO II 임상시험 모두에서 1차 평가 변수는 근거리 시력의 개선을 기반으로 설정되었으며, 일정 수준 이상의 근거리 시력 향상과 함께 원거리 시력의 유의한 감소가 없음을 동시에 만족하도록 설계되었다.
그러나 이러한 평가 변수는 실제 임상에서 환자가 경험하는 기능적 시력 개선을 충분히 반영하지 못할 가능성이 있다. 즉 시력표 상의 문자 인식 능력(letter score)의 향상이 반드시 일상생활에서의 독서 편의성이나 시각적 만족도 향상으로 이어진다고 단정하기 어렵다. 따라서 환자 보고 결과(patient-reported outcomes)나 삶의 질 지표가 상대적으로 부족하다는 점은 본 임상의 중요한 한계로 지적된다.
또한 약물의 효과 지속시간은 대체로 수 시간(약 6~10시간)으로 보고되었으며, 이는 하루 종일 지속적인 시력 개선을 기대하기에는 제한적이다. 특히 저녁 시간이나 야간 활동 시에는 약효가 감소할 가능성이 있어, 실제 임상 적용 시 환자의 생활 패턴에 따른 제한이 발생할 수 있다.
안전성 측면에서는 두통이 비교적 높은 빈도로 보고되었으며, 이는 동공 축소 및 조절 기전 변화와 관련된 약리학적 특성에 기인하는 것으로 추정된다. 이러한 이상반응은 환자의 장기 복약 순응도에 영향을 미칠 수 있는 요소로 고려된다. 더불어 동공 축소에 따른 야간 시력 저하 가능성 역시 중요한 안전성 고려사항으로, 특히 저조도 환경에서의 시각 기능에 미치는 영향에 대한 추가적인 평가가 필요하다.
BRIO I 연구의 경우, 복합제와 개별 성분 간 비교를 통해 조합의 우월성을 입증하는 데 초점을 두었으나, 실제 임상 환경에서 중요한 비교 대상인 기존 치료제와의 직접 비교가 이루어지지 않았다는 점에서 외적 타당성에 한계가 있다. 이는 해당 약제가 실제 임상에서 차지할 위치를 명확히 규정하는 데 제한 요인으로 작용할 수 있다.
BRIO II 연구에서 일정 규모의 안전성 데이터가 확보되었음에도 불구하고, 노안 치료가 장기간 지속적으로 사용되는 특성을 고려할 때 수년 단위의 장기 안전성 자료는 여전히 부족한 상황이다. 특히 지속적인 동공 변화 및 조절 기전에 대한 장기적 영향에 대해서는 추가적인 연구가 요구된다.
유베지의 임상적 의의는 무엇인가?
유베지는 노안(presbyopia) 치료에서 기존의 광학적 보정(예: 돋보기, 다초점 렌즈)이나 수술적 접근을 대체하거나 보완할 수 있는 새로운 약물학적 치료 옵션으로서 중요한 임상적 의의를 가진다. 특히 이 약제는 동공 조절 및 조절력 개선을 유도하는 기전을 통해 근거리 시력을 향상시키면서도 원거리 시력에 미치는 영향을 최소화하는 특징을 보인다.
임상 3상 연구(BRIO I 및 BRIO II) 결과에 따르면, 유베지는 단회 점안 후 30분 이내에 효과가 발현되며 최대 8시간까지 근거리 시력 개선 효과를 유지하였다. 또한 양안 비교정 근거리 시력(BUCNVA)의 유의한 개선과 함께 양안 비보정 원거리 시력(BUCDVA)의 저하 없이 시기능을 향상시키는 것으로 나타났다. 이러한 결과는 기존 단일 성분 제제 대비 복합제의 시너지 효과를 시사하며, 실제 임상 환경에서 기능적 시력 개선에 기여할 가능성을 뒷받침한다.
유베지의 또 다른 중요한 임상적 의의는 비침습적이고 가역적인 치료 옵션이라는 점이다. 수술적 치료와 달리 조직의 영구적 변형을 유발하지 않으며, 투약 중단 시 효과가 소실되어 환자의 선택권과 안전성을 높인다. 더불어 1일 1회 점안이라는 간편한 투여 방식은 치료 순응도를 향상시키는 요소로 작용할 수 있다.
특히, 굴절교정수술 후 환자나 인공수정체 삽입 환자(pseudophakic)를 포함한 다양한 환자군에서 효과가 입증되었다는 점은, 기존 치료 옵션이 제한적이었던 환자군에서도 활용 가능성을 확대한다는 측면에서 의미가 크다.
따라서 유베지는 빠른 작용 발현, 선택적 시력 개선, 우수한 안전성 및 편의성을 기반으로 노안 치료 패러다임을 확장하는 약물로 평가될 수 있으며, 향후 노안 관리 전략에서 중요한 역할을 수행할 것으로 기대된다.
참고문헌
1. Thomas Kohnen et al. “Treatments for Presbyopia” Deutsches Ärzteblatt International | Dtsch Arztebl Int 2025; 122: 501–7.
2. Elisabeth Waldemar Jakobsen “Brimonidine eye drops reveal diminished sympathetic pupillary tone in comatose patients with brain injury” Acta Neurochirurgica (2023) 165:1483–1494).
3. Andrzej Grzybowski et al. “Pharmacological Treatment in Presbyopia” J. Clin. Med. 2022, 11, 1385.
4. HamdiaGulAslam et al. “FDAapprovalofaceclidine(Vizz):anewchapterin nonsurgicalpresbyopiamanagement” Annals of Medicine & Surgery(2025)87:6967–6969.
5. Andrzej Grzybowskia et al. “An updated systematic review of pharmacological treatments for presbyopia” Advances in Ophthalmology Practice and Research 4 (2024) 220–225.
6. Nikola Grujic et al. “Neurobehavioral meaning of pupil size” Neuron 112, October 23, 2024.
7. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).
- 익명 댓글
- 실명 댓글
- 댓글 0
- 최신순
- 찬성순
- 반대순
오늘의 TOP 10
- 1불순물 트라마돌 리스크 확산…회수제품 처방 점유율 16%
- 2아리바이오 "치매약 기술수출로 상업화 채비…상장도 검토"
- 3경찰, 약국장 모집 채용 공고 낸 업체 조사 본격화
- 4[단독] 약정원 데이터 사업 우선협상대상자로 피코 선정
- 5식약처, 의약품 소포장 일단 규정대로…올해 처분 유예 없어
- 6비혁신형에 더 가혹한 다등재 룰...옥석가리기 본격화
- 7이수앱지스, 원가 부담에 적자 확대…신약 투자 지속
- 8다잘렉스SC·옴짜라 약가협상 타결...급여 등재 수순
- 9휴온스, 휴온스랩 흡수합병…'신약·바이오' 강화 승부수
- 10검찰·복지부·공단·심평원, 의약사범 합동수사팀 출범

















































![[유한양행] 마그비 시리즈](https://cdn.platpharm.co.kr/2024/03/2403261023280000193.jpg)
![[일양약품] 도담도담 시리즈](https://cdn.platpharm.co.kr/2024/02/2402020935180000240.jpg)
![[삼진제약] 게보핏 시리즈](https://cdn.platpharm.co.kr/2024/07/2407100728250000386.png)
![[옵투스] 오에수 시리즈](https://cdn.platpharm.co.kr/2026/02/2602130209000031633.webp)
![[신신제약] 아렉스마일드](https://cdn.platpharm.co.kr/2023/11/2311300927130000133.jpg)
![[경방신약] 방콜브이산](https://cdn.platpharm.co.kr/2025/12/2512310630020002495.webp)
![[일양약품] 프로엑스피](https://cdn.platpharm.co.kr/2026/01/2601221008450010125.webp)
![[신신제약] 모스키토 밀크](https://cdn.platpharm.co.kr/2025/10/2510150733400004067.webp)
![[노보노디스크] 위고비](https://cdn.platpharm.co.kr/static/dailypharm/Wigobi.png)
![[유한양행] 안티푸라민 파스 시리즈](https://cdn.platpharm.co.kr/2024/05/2405280631070000069.png)
![[종근당] 브레이닝캡슐](https://cdn.platpharm.co.kr/2025/06/2506040708450012544.png)
![[리쥬올] PDLLA 퍼밍 크림 30ml](https://cdn.platpharm.co.kr/2026/04/2604070229110000386.webp)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202604/1776750298620.png)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
![[레비온] PDRN+EGF, 레비온RX PDRN EGF 크림](https://i.baropharm.com/products/202512/1765949426601.png)
![[CHD제약] 50년 전통의 천혜당 식염포도당](https://i.baropharm.com/products/202604/1775095858899.png)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/partner/products/3f39593e-6318-4dd9-a778-c008c868b5c8.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[알엑스미] 알엑스미 리쥬영 울트라 PDRN 10000 딥리페어 크림](https://i.baropharm.com/partner/products/70c72dd0-cfd3-4d80-87e4-dc4f8de6658b.png?label=바뷰페로고)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[쥬베룩] 진짜 쥬베룩을 담은 약국전용 PDLLA 크림](https://i.baropharm.com/products/202604/1775343960671.png?label=바뷰페로고)
![[리쥬올] 닥터 리쥬올 어드밴스드 PDRN 리쥬비네이팅 크림 30ml](https://i.baropharm.com/partner/products/a201d2b4-f21e-4b13-957c-846d286b3d21.jpg?label=바뷰페로고)
![[경동제약] 인태반 자양강장제, 파워콤프](https://i.baropharm.com/partner/products/0a2cbb4c-96c5-40a5-aec2-8beeae11682c.png)




