-
 식약처, 첨단바이오약 장기추적조사 안정적 운영 지원[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 첨단바이오의약품 장기추적조사 분야 자주 묻는 질의응답집과 장기추적조사 이행& 8231;평가 결과보고 가이드라인을 발간했다고 31일 밝혔다. 첨단바이오의약품 장기추적조사 제도는 줄기세포 또는 유전물질이 포함된 첨단바이오의약품을 투여받은 환자의 안전을 확보하기 위해 투여 후 장기간 동안 암 등 이상사례 발생 여부를 추적& 8231;조사하는 것이다. 첨단바이오의약품 장기추적조사 분야 자주묻는 질의응답집은 첨단바이오의약품 장기추적조사 제도 전반을 쉽게 이해하는 데 도움을 주기 위해 마련했다. 주요 내용은 ▲첨단바이오의약품 장기추적조사 제도 도입 취지 ▲장기추적조사 지정 대상, 기간 ▲장기추적조사 계획부터 이행·평가 결과 보고까지 내용과 방법 ▲투여환자에 대한 투여 내역 등록 방법 등이다. 장기추적조사 이행& 8231;평가 결과보고 가이드라인’은 국내 제약사·개발사가 장기추적조사 이행& 8231;평가 결과보고를 원활하게 하는 데 도움을 주기 위해 마련했다. 주요 내용은 ▲관련 규정 ▲이행& 8231;평가 결과보고서 작성요령 등이다. 식약처는 이번에 발간된 질의응답집과 가이드라인이 첨단바이오의약품을 투여받은 환자의 안전을 확보하는 데 도움을 줄 것으로 기대하며, 앞으로도 과학적 지식을 기반으로 규제과학 전문성을 강화해 첨단바이오의약품의 안전관리에 최선을 다하겠다고 했다. 자세한 내용은 식약처 홈페이지(www.mfds.go.kr) > 법령/자료 > 법령정보 > 공무원지침서/민원안내서’에서 확인할 수 있다.2022-08-31 09:50:04이혜경
식약처, 첨단바이오약 장기추적조사 안정적 운영 지원[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 첨단바이오의약품 장기추적조사 분야 자주 묻는 질의응답집과 장기추적조사 이행& 8231;평가 결과보고 가이드라인을 발간했다고 31일 밝혔다. 첨단바이오의약품 장기추적조사 제도는 줄기세포 또는 유전물질이 포함된 첨단바이오의약품을 투여받은 환자의 안전을 확보하기 위해 투여 후 장기간 동안 암 등 이상사례 발생 여부를 추적& 8231;조사하는 것이다. 첨단바이오의약품 장기추적조사 분야 자주묻는 질의응답집은 첨단바이오의약품 장기추적조사 제도 전반을 쉽게 이해하는 데 도움을 주기 위해 마련했다. 주요 내용은 ▲첨단바이오의약품 장기추적조사 제도 도입 취지 ▲장기추적조사 지정 대상, 기간 ▲장기추적조사 계획부터 이행·평가 결과 보고까지 내용과 방법 ▲투여환자에 대한 투여 내역 등록 방법 등이다. 장기추적조사 이행& 8231;평가 결과보고 가이드라인’은 국내 제약사·개발사가 장기추적조사 이행& 8231;평가 결과보고를 원활하게 하는 데 도움을 주기 위해 마련했다. 주요 내용은 ▲관련 규정 ▲이행& 8231;평가 결과보고서 작성요령 등이다. 식약처는 이번에 발간된 질의응답집과 가이드라인이 첨단바이오의약품을 투여받은 환자의 안전을 확보하는 데 도움을 줄 것으로 기대하며, 앞으로도 과학적 지식을 기반으로 규제과학 전문성을 강화해 첨단바이오의약품의 안전관리에 최선을 다하겠다고 했다. 자세한 내용은 식약처 홈페이지(www.mfds.go.kr) > 법령/자료 > 법령정보 > 공무원지침서/민원안내서’에서 확인할 수 있다.2022-08-31 09:50:04이혜경 -
 스카이코비원 1일부터 사전예약…국산 백신 접종 본격화[데일리팜=김정주 기자] SK바이오사이언스가 개발한 코로나19 백신 '스카이코비원' 접종이 본격화 했다. 내일(1일) 사전예약을 시작으로 5일부터는 당일·방문접종을 개시한다. 이와 함께 코로나19 2가 백신은 올 4분기 중에 도입, 접종이 추진된다. 이기일 중앙재난안전대책본부 제1총괄조정관(보건복지부 제2차관)은 오늘(31일) 오전 중대본 회의에서 모두발언을 하고 이 같은 2가 백신과 국산 백신 접종계획 등 연휴 방역 계획에 대해 밝혔다. 먼저 정부는 최근 BA.5 변이에 효과적으로 대응할 수 있도록 2가 백신을 올 4분기 중 도입하기로 하고 고위험군을 우선 접종하기로 했다. 2차 접종 이상 완료한 18세 이상 성인도 접종이 가능하다. 국산 코로나19 백신 접종 계획도 잡혔다. 정부는 국내 제약기업 SK바이오사이언스가 개발한 스카이코비원 백신의 사전예약이 9월 1일부터 시작된다고 밝혔다. 5일부터는 당일·방문 접종, 13일부터는 예약접종이 가능하다. 앞서 식약처는 이 스카이코비원멀티주 61만회분에 대해 지난 26일 국가출하승인 했다. 이 백신은 코로나19 바이러스 항원을 유전자재조합 방식으로 제조 후 체내에 주입해 항체 생성을 유도하는 제품이다. 국내 기업 개발 백신 접종이 본격화 함에 따라 당국은 만 18세 이상 성인 중 미접종자를 대상으로 이 제품 접종을 권고했다. 이 제1총괄조정관은 "스카이코비원 백신은 기존 백신에 비해 중화항체 값이 2.9배 높으며 이상반응도 대부분 미미한 정도"라며 "18세 이상 성인 중 아직 접종을 하지 않은 사람에게 국산 백신 접종을 권고드린다"고 밝혔다.2022-08-31 09:33:00김정주
스카이코비원 1일부터 사전예약…국산 백신 접종 본격화[데일리팜=김정주 기자] SK바이오사이언스가 개발한 코로나19 백신 '스카이코비원' 접종이 본격화 했다. 내일(1일) 사전예약을 시작으로 5일부터는 당일·방문접종을 개시한다. 이와 함께 코로나19 2가 백신은 올 4분기 중에 도입, 접종이 추진된다. 이기일 중앙재난안전대책본부 제1총괄조정관(보건복지부 제2차관)은 오늘(31일) 오전 중대본 회의에서 모두발언을 하고 이 같은 2가 백신과 국산 백신 접종계획 등 연휴 방역 계획에 대해 밝혔다. 먼저 정부는 최근 BA.5 변이에 효과적으로 대응할 수 있도록 2가 백신을 올 4분기 중 도입하기로 하고 고위험군을 우선 접종하기로 했다. 2차 접종 이상 완료한 18세 이상 성인도 접종이 가능하다. 국산 코로나19 백신 접종 계획도 잡혔다. 정부는 국내 제약기업 SK바이오사이언스가 개발한 스카이코비원 백신의 사전예약이 9월 1일부터 시작된다고 밝혔다. 5일부터는 당일·방문 접종, 13일부터는 예약접종이 가능하다. 앞서 식약처는 이 스카이코비원멀티주 61만회분에 대해 지난 26일 국가출하승인 했다. 이 백신은 코로나19 바이러스 항원을 유전자재조합 방식으로 제조 후 체내에 주입해 항체 생성을 유도하는 제품이다. 국내 기업 개발 백신 접종이 본격화 함에 따라 당국은 만 18세 이상 성인 중 미접종자를 대상으로 이 제품 접종을 권고했다. 이 제1총괄조정관은 "스카이코비원 백신은 기존 백신에 비해 중화항체 값이 2.9배 높으며 이상반응도 대부분 미미한 정도"라며 "18세 이상 성인 중 아직 접종을 하지 않은 사람에게 국산 백신 접종을 권고드린다"고 밝혔다.2022-08-31 09:33:00김정주 -
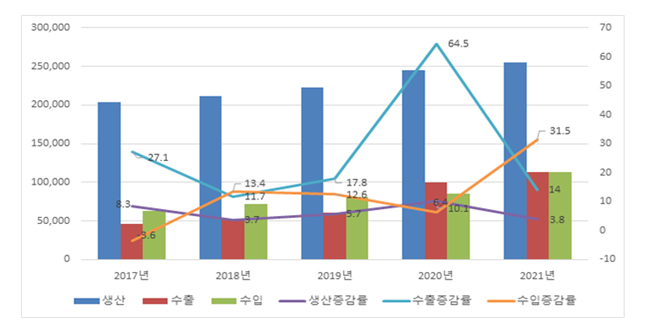 국내 의약품 시장 25조원 돌파…코로나 백신·치료제 영향[데일리팜=이혜경 기자] 코로나19 백신과 치료제의 생산·수입실적 상승으로 지난해 국내 의약품 시장규모가 관련 통계 집계(1998년부터) 이후 처음으로 25조를 돌파했다. 의약품 시장규모는 생산금액과 수입금액에서 수출금액을 제외한 금액으로 지난해 생산실적 25조4906억원, 수입실적 11조2668억원, 수출실적 11조3642억원을 기록하면서 무역수지는 2020년에 이어 2년 연속 흑자를 기록했다. 의약품 생산실적이 1조원 이상인 업체는 2개소로 1위는 셀트리온(1조2687억원, 2020년보다 14.1%↓), 2위는 한미약품(1조1291억원, 2020년보다 11.3%↑)으로 나타났다. 이 같은 통계는 31일 식품의약품안전처가 발표한 '2021년 국내 의약품·의약외품 생산·수출·수입 현황'을 통해 나타났다. 지난해 의약품 생산실적은 25조4906억원으로 2020년보다 3.8% 증가했고, 수출실적은 11조3642억원(99억2842만 달러)으로 14%, 수입실적은 11조2668억원(98억4335만 달러)으로 31.5% 증가했다. 생산실적은 국내 총생산(GDP) 대비 1.2%, 국내 제조업 총생산 대비 4.8% 수준으로 최근 5년간 연평균 성장률은 5.8%로 같은 기간 국내 제조업 총생산 연평균 성장률(1.6%)보다 3배 이상 높았다. 의약품 시장규모는 25조3932억원으로 전년 대비 9.6% 증가했으며, 지난 5년간 4%의 연평균 성장률을 보였다. 코로나19 백신·치료제의 2021년 총 생산실적은 1조475억원, 총 수입실적은 2조2644억원으로 전체 완제의약품 생산실적(22조4451억원)의 4.7%, 수입실적(8조8713억원)의 25.5%를 차지했다. 완제의약품 중 생산액 상위 3개 품목은 '스파이크박스주'(4561억원, 모더나코리아), '한국아스트라제네카백스제브리아주'(4055억원, 한국아스트라제네카), '렉키로나주960mg'(1859억원, 셀트리온) 순이다. 수입액 상위 3개 품목은 '코미나티주'(1조5869억원, 한국화이자제약), '모더나코비드-19백신주'(5601억원, 녹십자), '베클루리주정맥주사용동결건조분말'(1045억원, 길리어드사이언스코리아)로 집계됐다. 코로나19 백신 생산 국가인 독일과 스페인에서 의약품 수입이 급증(각각 175.5%↑, 672.4%↑)했다. 지난해 국내 바이오의약품 시장규모는 7조111억원으로 2020년(3조3029억원) 대비 112.3% 증가해 최근 5년 중에 가장 높은 증가폭을 보였다. 이는 2021년 바이오의약품에 해당하는 코로나19 백신·치료제의 신규 생산·수입실적이 추가된 데 기인한 것으로 보인다. 국내 바이오의약품 시장의 성장을 주도한 것은 백신으로, 백신의 시장규모는 3조8050억원으로 바이오의약품 시장에서 가장 큰 비중(약 54%)을 차지했으며 2020년보다 322.3% 증가했다. 바이오의약품 생산실적은 백신접종 본격화에 따라 큰 폭(20.6%)으로 성장한 4조7398억원으로 최근 5년간 연평균 16.2%의 성장률을 보이고 있다. 수출실적은 약 1조8169억원(약 15억8738만 달러)으로 전년 대비 23.7% 감소했으며 수입실적은 4조883억원(약 35억7175만 달러)으로 전년 대비 132.9% 증가했다. 의약품 수출액은 11조3642억원으로 역대 최대치였고, 2020년(9조9648억원)보다는 14.0% 증가한 수준이었으며, 바이오의약품 중심으로 세계 시장에서 품질을 인정받으며 최근 5년간 연평균 25.4%의 높은 성장세를 기록했다. 국가별로는 독일(2조1006억원)에 의약품을 가장 많이 수출했으며, 뒤를 이어 미국(1조4100억원), 일본(9258억원) 순을 보였다. 완제의약품 생산액 22조4451억원으로 2020년보다 6.8% 증가했고, 최근 5년간 연평균 증가율은 6.3%로 꾸준한 상승세를 보여주고 있다. 지난해 완제의약품 수출액은 9조 921억원으로 2020년보다 14.6% 증가했고, 최근 5년간 연평균 증가율은 32.7%로 큰 폭의 성장세를 보이고 있다. 우리나라가 완제의약품을 가장 많이 수출하는 국가는 독일(17억7094만 달러), 미국(10억9726만 달러), 일본(4억8505만 달러) 순이었고, 완제의약품을 가장 많이 수입하는 국가는 독일(23억4205만 달러), 미국(11억4785만 달러), 스위스(5억3413만 달러) 순으로 2020년에 이어 독일, 미국이 최대 교역국 지위를 유지했다. 전문의약품의 생산실적(19조3759억원)이 완제의약품 중 86.3%를 차지해 최근 5년간 80%대 이상의 높은 생산 비중을 계속 유지했다. 전문의약품 1만5947품목의 생산실적은 19조3759억원으로 2020년(17조8457억원)보다 8.6% 증가했으나, 일반의약품(4807품목) 생산실적은 3조692억원으로 2020년(3조1779억원)보다 3.4% 감소했다. 의약외품 생산실적은 2조3368억원으로 2020년(3조7149억원)보다 37.1% 감소했다. 의약외품 생산업체 수는 1324개소로 2020년 보다 6.9% 증가했으며, 2021년 생산품목 수는 6384개로 2020년 보다 20.7% 증가했다. 코로나19 방역물품(마스크, 외용소독제)의 생산실적은 1조 623억원으로 2020년보다 56.4% 감소하면서 생산실적이 크게 증가했던 전년 대비 증가세는 꺾였으나, 코로나19 발생 이전인 2019년 대비 각각 326%, 197% 증가했다. 업체별 의약외품 생산실적은 동아제약(3159억원)이 2020년에 이어 1위를 차지했고, 엘지생활건강(1615억원), 유한킴벌리(1400억원), 아모레퍼시픽(1229억원), 엘지유니참(484억원)이 뒤를 이었으며, 이들 업체가 전체 의약외품 생산실적의 33.8%를 차지했다. 지난해 품목별 의약외품 생산실적은 박카스디액(1437억원)이 2020년에 이어 1위를 차지했고, 박카스에프액(1055억원), 메디안치석오리지널치약(438억원)이 뒤를 이었다. 식약처는 "지난해 의약품 생산·수출·수입실적 자료가 국내 의약품 산업 현황을 분석하기 위한 기초자료로 활용되고, 업계의 제품 개발·연구와 정부 정책 수립 등 의약품 산업 발전에 널리 활용될 것으로 기대한다"고 밝혔다.2022-08-31 08:59:17이혜경
국내 의약품 시장 25조원 돌파…코로나 백신·치료제 영향[데일리팜=이혜경 기자] 코로나19 백신과 치료제의 생산·수입실적 상승으로 지난해 국내 의약품 시장규모가 관련 통계 집계(1998년부터) 이후 처음으로 25조를 돌파했다. 의약품 시장규모는 생산금액과 수입금액에서 수출금액을 제외한 금액으로 지난해 생산실적 25조4906억원, 수입실적 11조2668억원, 수출실적 11조3642억원을 기록하면서 무역수지는 2020년에 이어 2년 연속 흑자를 기록했다. 의약품 생산실적이 1조원 이상인 업체는 2개소로 1위는 셀트리온(1조2687억원, 2020년보다 14.1%↓), 2위는 한미약품(1조1291억원, 2020년보다 11.3%↑)으로 나타났다. 이 같은 통계는 31일 식품의약품안전처가 발표한 '2021년 국내 의약품·의약외품 생산·수출·수입 현황'을 통해 나타났다. 지난해 의약품 생산실적은 25조4906억원으로 2020년보다 3.8% 증가했고, 수출실적은 11조3642억원(99억2842만 달러)으로 14%, 수입실적은 11조2668억원(98억4335만 달러)으로 31.5% 증가했다. 생산실적은 국내 총생산(GDP) 대비 1.2%, 국내 제조업 총생산 대비 4.8% 수준으로 최근 5년간 연평균 성장률은 5.8%로 같은 기간 국내 제조업 총생산 연평균 성장률(1.6%)보다 3배 이상 높았다. 의약품 시장규모는 25조3932억원으로 전년 대비 9.6% 증가했으며, 지난 5년간 4%의 연평균 성장률을 보였다. 코로나19 백신·치료제의 2021년 총 생산실적은 1조475억원, 총 수입실적은 2조2644억원으로 전체 완제의약품 생산실적(22조4451억원)의 4.7%, 수입실적(8조8713억원)의 25.5%를 차지했다. 완제의약품 중 생산액 상위 3개 품목은 '스파이크박스주'(4561억원, 모더나코리아), '한국아스트라제네카백스제브리아주'(4055억원, 한국아스트라제네카), '렉키로나주960mg'(1859억원, 셀트리온) 순이다. 수입액 상위 3개 품목은 '코미나티주'(1조5869억원, 한국화이자제약), '모더나코비드-19백신주'(5601억원, 녹십자), '베클루리주정맥주사용동결건조분말'(1045억원, 길리어드사이언스코리아)로 집계됐다. 코로나19 백신 생산 국가인 독일과 스페인에서 의약품 수입이 급증(각각 175.5%↑, 672.4%↑)했다. 지난해 국내 바이오의약품 시장규모는 7조111억원으로 2020년(3조3029억원) 대비 112.3% 증가해 최근 5년 중에 가장 높은 증가폭을 보였다. 이는 2021년 바이오의약품에 해당하는 코로나19 백신·치료제의 신규 생산·수입실적이 추가된 데 기인한 것으로 보인다. 국내 바이오의약품 시장의 성장을 주도한 것은 백신으로, 백신의 시장규모는 3조8050억원으로 바이오의약품 시장에서 가장 큰 비중(약 54%)을 차지했으며 2020년보다 322.3% 증가했다. 바이오의약품 생산실적은 백신접종 본격화에 따라 큰 폭(20.6%)으로 성장한 4조7398억원으로 최근 5년간 연평균 16.2%의 성장률을 보이고 있다. 수출실적은 약 1조8169억원(약 15억8738만 달러)으로 전년 대비 23.7% 감소했으며 수입실적은 4조883억원(약 35억7175만 달러)으로 전년 대비 132.9% 증가했다. 의약품 수출액은 11조3642억원으로 역대 최대치였고, 2020년(9조9648억원)보다는 14.0% 증가한 수준이었으며, 바이오의약품 중심으로 세계 시장에서 품질을 인정받으며 최근 5년간 연평균 25.4%의 높은 성장세를 기록했다. 국가별로는 독일(2조1006억원)에 의약품을 가장 많이 수출했으며, 뒤를 이어 미국(1조4100억원), 일본(9258억원) 순을 보였다. 완제의약품 생산액 22조4451억원으로 2020년보다 6.8% 증가했고, 최근 5년간 연평균 증가율은 6.3%로 꾸준한 상승세를 보여주고 있다. 지난해 완제의약품 수출액은 9조 921억원으로 2020년보다 14.6% 증가했고, 최근 5년간 연평균 증가율은 32.7%로 큰 폭의 성장세를 보이고 있다. 우리나라가 완제의약품을 가장 많이 수출하는 국가는 독일(17억7094만 달러), 미국(10억9726만 달러), 일본(4억8505만 달러) 순이었고, 완제의약품을 가장 많이 수입하는 국가는 독일(23억4205만 달러), 미국(11억4785만 달러), 스위스(5억3413만 달러) 순으로 2020년에 이어 독일, 미국이 최대 교역국 지위를 유지했다. 전문의약품의 생산실적(19조3759억원)이 완제의약품 중 86.3%를 차지해 최근 5년간 80%대 이상의 높은 생산 비중을 계속 유지했다. 전문의약품 1만5947품목의 생산실적은 19조3759억원으로 2020년(17조8457억원)보다 8.6% 증가했으나, 일반의약품(4807품목) 생산실적은 3조692억원으로 2020년(3조1779억원)보다 3.4% 감소했다. 의약외품 생산실적은 2조3368억원으로 2020년(3조7149억원)보다 37.1% 감소했다. 의약외품 생산업체 수는 1324개소로 2020년 보다 6.9% 증가했으며, 2021년 생산품목 수는 6384개로 2020년 보다 20.7% 증가했다. 코로나19 방역물품(마스크, 외용소독제)의 생산실적은 1조 623억원으로 2020년보다 56.4% 감소하면서 생산실적이 크게 증가했던 전년 대비 증가세는 꺾였으나, 코로나19 발생 이전인 2019년 대비 각각 326%, 197% 증가했다. 업체별 의약외품 생산실적은 동아제약(3159억원)이 2020년에 이어 1위를 차지했고, 엘지생활건강(1615억원), 유한킴벌리(1400억원), 아모레퍼시픽(1229억원), 엘지유니참(484억원)이 뒤를 이었으며, 이들 업체가 전체 의약외품 생산실적의 33.8%를 차지했다. 지난해 품목별 의약외품 생산실적은 박카스디액(1437억원)이 2020년에 이어 1위를 차지했고, 박카스에프액(1055억원), 메디안치석오리지널치약(438억원)이 뒤를 이었다. 식약처는 "지난해 의약품 생산·수출·수입실적 자료가 국내 의약품 산업 현황을 분석하기 위한 기초자료로 활용되고, 업계의 제품 개발·연구와 정부 정책 수립 등 의약품 산업 발전에 널리 활용될 것으로 기대한다"고 밝혔다.2022-08-31 08:59:17이혜경 -
 식약처, 국내 mRNA 유전자치료제 개발 지원[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 메신저리보핵산(mRNA) 기반 유전자치료제 개발을 지원하기 위해 품질평가 시 고려해야 할 사항을 안내하는 mRNA 기반 유전자치료제의 품질평가 가이드라인을 세계 최초로 8월 30일 마련·배포했다. 이번 가이드라인의 주요 내용은 ▲mRNA 기반 치료제 개발 시 고려사항 ▲ 공정개발·제조 시 고려사항 ▲ 원료·완제 의약품 품질평가 시 고려사항 등이다. mRNA 기반 유전자치료제는 바이러스 벡터 유전자치료제보다 안전하고 플라스미드 DNA 기반 유전자치료제보다 치료 단백질 발현 효율이 높은 장점이 있지만, mRNA의 체내 안정성이 낮아 개발에 어려움이 있었다. 최근 지질나노입자 등과 같이 mRNA 백신 등에서 체내 안정성을 높이는 기술이 상용화되어 앞으로 mRNA 기반 유전자치료제 개발이 증가할 것으로 예상된다. 이번 가이드라인에서는 mRNA가 봉입된 지질나노입자(Lipid nanoparticle, LNP)의 품질관리 평가항목, 시험방법 예시 등도 제공한다. 식약처는 이번 안내서가 국내 개발사들이 시행착오를 줄이고 mRNA 기반 유전자치료제를 신속하게 개발하는 데 도움을 줄 것으로 기대한다고 밝혔다. RNA 기반 유전자치료제의 품질평가 가이드라인’은 식약처 홈페이지 > 법령자료 > 자료실 > 안내서/지침에서 확인할 수 있다.2022-08-30 10:23:41이혜경
식약처, 국내 mRNA 유전자치료제 개발 지원[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 메신저리보핵산(mRNA) 기반 유전자치료제 개발을 지원하기 위해 품질평가 시 고려해야 할 사항을 안내하는 mRNA 기반 유전자치료제의 품질평가 가이드라인을 세계 최초로 8월 30일 마련·배포했다. 이번 가이드라인의 주요 내용은 ▲mRNA 기반 치료제 개발 시 고려사항 ▲ 공정개발·제조 시 고려사항 ▲ 원료·완제 의약품 품질평가 시 고려사항 등이다. mRNA 기반 유전자치료제는 바이러스 벡터 유전자치료제보다 안전하고 플라스미드 DNA 기반 유전자치료제보다 치료 단백질 발현 효율이 높은 장점이 있지만, mRNA의 체내 안정성이 낮아 개발에 어려움이 있었다. 최근 지질나노입자 등과 같이 mRNA 백신 등에서 체내 안정성을 높이는 기술이 상용화되어 앞으로 mRNA 기반 유전자치료제 개발이 증가할 것으로 예상된다. 이번 가이드라인에서는 mRNA가 봉입된 지질나노입자(Lipid nanoparticle, LNP)의 품질관리 평가항목, 시험방법 예시 등도 제공한다. 식약처는 이번 안내서가 국내 개발사들이 시행착오를 줄이고 mRNA 기반 유전자치료제를 신속하게 개발하는 데 도움을 줄 것으로 기대한다고 밝혔다. RNA 기반 유전자치료제의 품질평가 가이드라인’은 식약처 홈페이지 > 법령자료 > 자료실 > 안내서/지침에서 확인할 수 있다.2022-08-30 10:23:41이혜경 -
 식약처, 화이자 코미나티2주0.1mg/mL 허가심사 착수[데일리팜=김정주 기자] 화이자의 코로나19 2가 백신 코미나티2주0.1mg/mL 허가심사가 시작됐다. 식품의약품안전처(처장 오유경)는 한국화이자가 초기 코로나19 바이러스와 변이 바이러스(오미크론주 변이 BA.1) 항원을 각각 발현하는 메신저리보핵산(mRNA) 방식의 2가백신인 코미나티2주0.1mg/mL의 수입 품목허가를 오늘(29일) 신청해 심사에 착수했다고 밝혔다. 코미나티2주0.1mg/mL은 12세 이상에서 SARS-CoV-2 바이러스에 의한 코로나19의 예방 효능효과를 보이며 기초접종 이후 추가 접종에 사용하기 위해 개발됐다. 당국은 이번 품목허가 신청 시 제출된 임상·비임상·품질·GMP 자료 등을 신속하고 면밀하게 검토하고, 감염내과 전문의를 포함한 백신 전문가에게 해당 백신의 안전성·효과성에 대해 자문한 후 허가 여부를 결정할 예정이다. 식약처는 화이자가 지난 5일 코미나티2주0.1mg/mL의 임상 자료에 대한 사전검토를 신청함에 따라 검토를 진행하고 있다고 설명했다. 식약처는 "앞으로도 우리 국민에게 안전하고 효과 있는 백신을 공급할 수 있도록 최선을 다하겠다"고 밝혔다.2022-08-29 17:56:11김정주
식약처, 화이자 코미나티2주0.1mg/mL 허가심사 착수[데일리팜=김정주 기자] 화이자의 코로나19 2가 백신 코미나티2주0.1mg/mL 허가심사가 시작됐다. 식품의약품안전처(처장 오유경)는 한국화이자가 초기 코로나19 바이러스와 변이 바이러스(오미크론주 변이 BA.1) 항원을 각각 발현하는 메신저리보핵산(mRNA) 방식의 2가백신인 코미나티2주0.1mg/mL의 수입 품목허가를 오늘(29일) 신청해 심사에 착수했다고 밝혔다. 코미나티2주0.1mg/mL은 12세 이상에서 SARS-CoV-2 바이러스에 의한 코로나19의 예방 효능효과를 보이며 기초접종 이후 추가 접종에 사용하기 위해 개발됐다. 당국은 이번 품목허가 신청 시 제출된 임상·비임상·품질·GMP 자료 등을 신속하고 면밀하게 검토하고, 감염내과 전문의를 포함한 백신 전문가에게 해당 백신의 안전성·효과성에 대해 자문한 후 허가 여부를 결정할 예정이다. 식약처는 화이자가 지난 5일 코미나티2주0.1mg/mL의 임상 자료에 대한 사전검토를 신청함에 따라 검토를 진행하고 있다고 설명했다. 식약처는 "앞으로도 우리 국민에게 안전하고 효과 있는 백신을 공급할 수 있도록 최선을 다하겠다"고 밝혔다.2022-08-29 17:56:11김정주 -
 비호지킨림프종 치료제 '포텔리지오' 국내 허가 임박[데일리팜=이혜경 기자] 쿄와하코기린의 희귀 2종 비호지킨 림프종 치료제인 '포텔리지오주20mg(모가물리주맙)'이 국내 품목허가를 받을 전망이다. 지난 2018년 8월 미국 식품의약국(FDA)으로부터 난치·재발성 균상식육종(mycosis fungoides, MF) 혹은 세자리 증후군(S& 233;zary syndrome, SS)의 치료에 허가를 받은 지 4년 만이다. 26일 제약업계에 따르면 식약처는 최근 포스텔리지오의 안전성·유효성 심사를 종료했다. 안전성·유효성 심사가 종료된 만큼 다른 변수가 없다면 조만간 허가를 받을 가능성이 높다는 분석이다. 포텔리지오는 단일클론항체 성분으로 암세포에서 발견되는 C-C케모카인 수용체-4(CC chemokine receptor type 4)에 작용해 치료 효과를 낸다. 4년 전 미국 승인 당시 세자리 증후군 치료제로는 최초 승인이라는 타이틀을 얻었다. 3상 임상시험에서 질환의 악화 없이 생존한 기간(PFS)은 포텔리지오 그룹(7.6개월)이 졸린자 그룹(3.1개월) 보다 2배 이상 길었다. 종양의 크기가 특정 수준으로 줄어든 환자의 비율(전체 반응률, ORR)은 포텔리지오 그룹 28%, 졸린자 그룹 5%로 나타났다. 포텔리지오 투여로 발생한 이상사례는 발진·주사부위반응·피로·설사·근골격계 통증 등이다. 한편 포텔리지오는 FDA 승인 이후, 최소 1가지 이상의 전신요법을 받은 균상식육종(Mycosis Fungoides)과 세자리증후군(S& 233;zary Syndrome) 성인 환자를 위한 치료제로 2018년 11월 유럽집행위원회 승인을 받은 바 있다.2022-08-27 17:54:58이혜경
비호지킨림프종 치료제 '포텔리지오' 국내 허가 임박[데일리팜=이혜경 기자] 쿄와하코기린의 희귀 2종 비호지킨 림프종 치료제인 '포텔리지오주20mg(모가물리주맙)'이 국내 품목허가를 받을 전망이다. 지난 2018년 8월 미국 식품의약국(FDA)으로부터 난치·재발성 균상식육종(mycosis fungoides, MF) 혹은 세자리 증후군(S& 233;zary syndrome, SS)의 치료에 허가를 받은 지 4년 만이다. 26일 제약업계에 따르면 식약처는 최근 포스텔리지오의 안전성·유효성 심사를 종료했다. 안전성·유효성 심사가 종료된 만큼 다른 변수가 없다면 조만간 허가를 받을 가능성이 높다는 분석이다. 포텔리지오는 단일클론항체 성분으로 암세포에서 발견되는 C-C케모카인 수용체-4(CC chemokine receptor type 4)에 작용해 치료 효과를 낸다. 4년 전 미국 승인 당시 세자리 증후군 치료제로는 최초 승인이라는 타이틀을 얻었다. 3상 임상시험에서 질환의 악화 없이 생존한 기간(PFS)은 포텔리지오 그룹(7.6개월)이 졸린자 그룹(3.1개월) 보다 2배 이상 길었다. 종양의 크기가 특정 수준으로 줄어든 환자의 비율(전체 반응률, ORR)은 포텔리지오 그룹 28%, 졸린자 그룹 5%로 나타났다. 포텔리지오 투여로 발생한 이상사례는 발진·주사부위반응·피로·설사·근골격계 통증 등이다. 한편 포텔리지오는 FDA 승인 이후, 최소 1가지 이상의 전신요법을 받은 균상식육종(Mycosis Fungoides)과 세자리증후군(S& 233;zary Syndrome) 성인 환자를 위한 치료제로 2018년 11월 유럽집행위원회 승인을 받은 바 있다.2022-08-27 17:54:58이혜경 -
 국내 개발 '스카이코비원' 61만회분 국가출하승인[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는SK바이오사이언스사가 국내에서 개발·제조한 '스카이코비원멀티주' 61만회분에 대해 26일 국가출하승인했다고 밝혔다. 스카이코비원은 코로나19 바이러스 항원을 유전자재조합 방식으로 제조한 후 체내에 주입해 항체를 생성하도록 유도하는 백신이다. 식약처는 안전을 최우선으로 과학적 근거에 기반을 두고 철저하게 국가출하승인을 진행했다. 스카이코비원 61만회분에 대해 검정시험을 수행하고, 제조사의 제조& 8231;시험 자료를 검토한 결과 허가받은 품질에 적합하다고 판단해 국가출하승인을 결정했다. 식약처는 앞으로도 코로나19 백신을 신속하고 철저하게 검증해 품질이 확보된 백신이 안정적으로 공급될 수 있도록 최선을 다하겠다고 밝혔다.2022-08-26 18:18:12이혜경
국내 개발 '스카이코비원' 61만회분 국가출하승인[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는SK바이오사이언스사가 국내에서 개발·제조한 '스카이코비원멀티주' 61만회분에 대해 26일 국가출하승인했다고 밝혔다. 스카이코비원은 코로나19 바이러스 항원을 유전자재조합 방식으로 제조한 후 체내에 주입해 항체를 생성하도록 유도하는 백신이다. 식약처는 안전을 최우선으로 과학적 근거에 기반을 두고 철저하게 국가출하승인을 진행했다. 스카이코비원 61만회분에 대해 검정시험을 수행하고, 제조사의 제조& 8231;시험 자료를 검토한 결과 허가받은 품질에 적합하다고 판단해 국가출하승인을 결정했다. 식약처는 앞으로도 코로나19 백신을 신속하고 철저하게 검증해 품질이 확보된 백신이 안정적으로 공급될 수 있도록 최선을 다하겠다고 밝혔다.2022-08-26 18:18:12이혜경 -
 브롬화수소산시탈로프람, 동공 확장...타크로벨, 신장애 유발[데일리팜=이혜경 기자] 우울증 치료제 '브롬화수소산시탈로프람' 성분제제와 신장 및 간이식 이후 쓰이는 '타크로리무스' 성분제제의 허가사항이 변경될 예정이다. 식품의약품안전처는 미국 식품의약품청(FDA) 및 유럽집행위원회(EC)의 안전성 정보 검토 결과를 토대로 허가사항 변경(안)을 마련하고 내달 7일까지 의견조회를 진행한다. 우울증, 공황장애, 강박장애 치료제인 브롬화수소산시탈로프람 성분 제제는 한국산도스의 '산도스시탈로프람정' 1품목이지만, 현재 국내 유통은 이뤄지지 않고 있다. 식약처 안전성 검토 결과 '이 약을 포함한 항우울제 사용과 관련하여 동공 확장이 발생할 수 있다. 이러한 동공 확장은 개방 홍채 절제술을 받지 않아 해부학적으로 좁은 각을 가진 환자에게서 폐쇄우각 발작을 유발할 수 있다'는 내용이 주의사항에 신설된다. 특히 치료를 받지 않아 해부학적으로 좁은 각을 가진 환자에게 이 약을 포함한 항우울제의 사용을 피해야 한다. QT 간격 연장을 유발하는 약물과 함께 브롬화수소산시탈로프람 성분 제제를 사용하면 이 약만 투여하는 경우에 비해 QT가 추가로 연장될 수 있어 QT 간격 연장을 유발하는 약물과 이 약의 병용 투여를 피해야 한다는 내용은 상호작용 항에 신설된다. 이식 후 감염 방지에 투약하는 타크로리무스 성분제제는 종근당의 '타크로벨' 이연제약의 '타크로리' 한미약품의 '타리무스' 한국아스텔라스제약의 '프로그랍'과 '아드바그랍' 한국피엠지제약의 '타르신' 성원애드콕제약의 '타크로인' 한림제약의 '타크로스' 킴스제약의 '타그랍' 셀트리온제약의 '셀로그리' 한국유니온제약의 '유니로리' 에이프로젠제약의 '타클로' 안국뉴팜의 '뉴로미스' 등이 있다. 식약처 검토 결과 신기능 장애가 있는 환자는 타크로리무스의 용량을 조절하기 위해 면밀히 모니터링 해야 하며 일시적인 감량 또는 중단이 필요할 수 있다는 경고 조항이 주의사항에 신설된다. CMV(거대세포바이러스) 감염이 관찰됐으며, 이식편 거부를 포함한 중대하고 치명적인 결과를 가져올 수 있다는 내용도 포함된다. '트리메토프림'은 '아미로라이드'와 같이 칼륨보전 이뇨제로 작용한다고 알려져 있으므로, 타크로리무스와 혈청 칼륨 수치를 증가시키는 다른 제제(트리메토프림 및 코트리목사졸(트리메토프림·설파메톡사졸) 등)와 병용 시 주의가 필요하다.2022-08-26 16:58:23이혜경
브롬화수소산시탈로프람, 동공 확장...타크로벨, 신장애 유발[데일리팜=이혜경 기자] 우울증 치료제 '브롬화수소산시탈로프람' 성분제제와 신장 및 간이식 이후 쓰이는 '타크로리무스' 성분제제의 허가사항이 변경될 예정이다. 식품의약품안전처는 미국 식품의약품청(FDA) 및 유럽집행위원회(EC)의 안전성 정보 검토 결과를 토대로 허가사항 변경(안)을 마련하고 내달 7일까지 의견조회를 진행한다. 우울증, 공황장애, 강박장애 치료제인 브롬화수소산시탈로프람 성분 제제는 한국산도스의 '산도스시탈로프람정' 1품목이지만, 현재 국내 유통은 이뤄지지 않고 있다. 식약처 안전성 검토 결과 '이 약을 포함한 항우울제 사용과 관련하여 동공 확장이 발생할 수 있다. 이러한 동공 확장은 개방 홍채 절제술을 받지 않아 해부학적으로 좁은 각을 가진 환자에게서 폐쇄우각 발작을 유발할 수 있다'는 내용이 주의사항에 신설된다. 특히 치료를 받지 않아 해부학적으로 좁은 각을 가진 환자에게 이 약을 포함한 항우울제의 사용을 피해야 한다. QT 간격 연장을 유발하는 약물과 함께 브롬화수소산시탈로프람 성분 제제를 사용하면 이 약만 투여하는 경우에 비해 QT가 추가로 연장될 수 있어 QT 간격 연장을 유발하는 약물과 이 약의 병용 투여를 피해야 한다는 내용은 상호작용 항에 신설된다. 이식 후 감염 방지에 투약하는 타크로리무스 성분제제는 종근당의 '타크로벨' 이연제약의 '타크로리' 한미약품의 '타리무스' 한국아스텔라스제약의 '프로그랍'과 '아드바그랍' 한국피엠지제약의 '타르신' 성원애드콕제약의 '타크로인' 한림제약의 '타크로스' 킴스제약의 '타그랍' 셀트리온제약의 '셀로그리' 한국유니온제약의 '유니로리' 에이프로젠제약의 '타클로' 안국뉴팜의 '뉴로미스' 등이 있다. 식약처 검토 결과 신기능 장애가 있는 환자는 타크로리무스의 용량을 조절하기 위해 면밀히 모니터링 해야 하며 일시적인 감량 또는 중단이 필요할 수 있다는 경고 조항이 주의사항에 신설된다. CMV(거대세포바이러스) 감염이 관찰됐으며, 이식편 거부를 포함한 중대하고 치명적인 결과를 가져올 수 있다는 내용도 포함된다. '트리메토프림'은 '아미로라이드'와 같이 칼륨보전 이뇨제로 작용한다고 알려져 있으므로, 타크로리무스와 혈청 칼륨 수치를 증가시키는 다른 제제(트리메토프림 및 코트리목사졸(트리메토프림·설파메톡사졸) 등)와 병용 시 주의가 필요하다.2022-08-26 16:58:23이혜경 -
 식약처 "수급 원활한 덱시부프로펜·록소프로펜 처방을"[데일리팜=이혜경 기자] 식품의약품안전처가 대한의사협회 등 의료계에 조제용 감기약의 분산처방을 요청하면서 제약업계도 수급 원활 전문의약품 증산에 힘을 보탤 전망이다. 26일 제약업계에 따르면 한국제약바이오협회는 일선 약국 현장에서 품절을 호소하고 있는 '아세트아미노펜' '이부프로펜' 제제 뿐만 아니라 '덱시부프로펜' 및 '록소프로펜' 제제의 증산을 요청했다. 현재 해열진통제 중 덱시부프로펜, 록소프로펜 성분 전문약은 총 210품목으로, 제약바이오협회는 해당 품목과 생산업체 목록을 공개했다. 지난 8일부터 소량포장 의약품 공급 안내 시스템(sosdrug.com)을 활용한 감기약 신속대응시스템을 운영 결과, 대한약사회는 아세트아미노펜 제제와 이부프로펜 제제의 공급을 지속적으로 요청하고 있다. 건강보험심사평가원 의약품관리종합정보센터가 지난 12일부터 공개하고 있는 감기약 전문약 재고 보유 추정 정보를 보더라도 아세트아미노펜, 이부프로펜 제제보다는 덱시부프로펜, 록소프로펜 제제가 상대적으로 수급이 원활한 상태다. 이에 식약처가 의협 등에 유사 효능 의약품인 덱시부프로펜, 록소프로펜 제제로 분산 처방을 요청하면서, 제약바이오협회도 해당 제제에 대한 증산을 요청했다. 한편 정부는 코로나19 확산으로 인한 감기약 품절 사태 재발 방지를 위해 공적 공급 관리 시스템 구축, 특정 품절 의약품에 대한 퇴장방지의약품 지정, 긴급 명령에 따른 관련 제약사의 손실 보상 등 방안을 검토하고 있는 것으로 알려졌다.2022-08-26 11:01:57이혜경
식약처 "수급 원활한 덱시부프로펜·록소프로펜 처방을"[데일리팜=이혜경 기자] 식품의약품안전처가 대한의사협회 등 의료계에 조제용 감기약의 분산처방을 요청하면서 제약업계도 수급 원활 전문의약품 증산에 힘을 보탤 전망이다. 26일 제약업계에 따르면 한국제약바이오협회는 일선 약국 현장에서 품절을 호소하고 있는 '아세트아미노펜' '이부프로펜' 제제 뿐만 아니라 '덱시부프로펜' 및 '록소프로펜' 제제의 증산을 요청했다. 현재 해열진통제 중 덱시부프로펜, 록소프로펜 성분 전문약은 총 210품목으로, 제약바이오협회는 해당 품목과 생산업체 목록을 공개했다. 지난 8일부터 소량포장 의약품 공급 안내 시스템(sosdrug.com)을 활용한 감기약 신속대응시스템을 운영 결과, 대한약사회는 아세트아미노펜 제제와 이부프로펜 제제의 공급을 지속적으로 요청하고 있다. 건강보험심사평가원 의약품관리종합정보센터가 지난 12일부터 공개하고 있는 감기약 전문약 재고 보유 추정 정보를 보더라도 아세트아미노펜, 이부프로펜 제제보다는 덱시부프로펜, 록소프로펜 제제가 상대적으로 수급이 원활한 상태다. 이에 식약처가 의협 등에 유사 효능 의약품인 덱시부프로펜, 록소프로펜 제제로 분산 처방을 요청하면서, 제약바이오협회도 해당 제제에 대한 증산을 요청했다. 한편 정부는 코로나19 확산으로 인한 감기약 품절 사태 재발 방지를 위해 공적 공급 관리 시스템 구축, 특정 품절 의약품에 대한 퇴장방지의약품 지정, 긴급 명령에 따른 관련 제약사의 손실 보상 등 방안을 검토하고 있는 것으로 알려졌다.2022-08-26 11:01:57이혜경 -
 원개발사 허가사항 변경시 제네릭에도 즉시 반영[데일리팜=이혜경 기자] 원개발사 의약품의 안전성·유효성 관련 허가사항이 변경되는 경우, 제네릭의약품(복제의약품)에 즉시 반영해 적용 시기를 최소 1달 이상 단축시킬 수 있는 ‘의약품 안전성·유효성 허가사항 신속 반영(통일조정) 방안이 시행된다. 식품의약품안전처는 기존에 원개발사 품목 허가변경 후 별도 통일조정(월 1회)을 진행하던 것을 오늘(26일)부터는 원개발사 품목 허가변경 시 통일조정(안) 의견조회 및 통일조정을 상시 진행한다고 밝혔다. 종전에는 원개발사 품목의 허가사항이 변경되면 월 1회 통일조정 대상 제네릭 의약품의 목록을 모아 실시했다. 이번 신속 통일조정 절차는 원개발사 품목 허가변경 신청 시 통일조정 대상 제네릭 의약품의 목록 확보→ 원개발사 품목 허가변경 완료 시 통일조정(안) 의견조회→ 원개발사 품목 허가변경 이의신청 기간 경과 후 허가사항 변경 명령 즉시 시행을 거친다. 의약품 안전성·유효성 허가사항 신속 반영 방안은 최신의 안전성과 유효성 자료를 바탕으로 심사를 거쳐 원개발사 품목에 반영된 효능·효과 등 허가사항을 제네릭의약품에도 반영하는 시간 차이를 최소화하기 위해 마련했다. 식약처는 "이번 의약품 안전성·유효성 허가사항 신속 반영 방안 운영이 제네릭의약품을 사용하는 의·약사, 환자 등에게 최신 의약품 정보를 신속히 제공하는 데 도움이 될 것"으로 기대했다.2022-08-26 09:01:56이혜경
원개발사 허가사항 변경시 제네릭에도 즉시 반영[데일리팜=이혜경 기자] 원개발사 의약품의 안전성·유효성 관련 허가사항이 변경되는 경우, 제네릭의약품(복제의약품)에 즉시 반영해 적용 시기를 최소 1달 이상 단축시킬 수 있는 ‘의약품 안전성·유효성 허가사항 신속 반영(통일조정) 방안이 시행된다. 식품의약품안전처는 기존에 원개발사 품목 허가변경 후 별도 통일조정(월 1회)을 진행하던 것을 오늘(26일)부터는 원개발사 품목 허가변경 시 통일조정(안) 의견조회 및 통일조정을 상시 진행한다고 밝혔다. 종전에는 원개발사 품목의 허가사항이 변경되면 월 1회 통일조정 대상 제네릭 의약품의 목록을 모아 실시했다. 이번 신속 통일조정 절차는 원개발사 품목 허가변경 신청 시 통일조정 대상 제네릭 의약품의 목록 확보→ 원개발사 품목 허가변경 완료 시 통일조정(안) 의견조회→ 원개발사 품목 허가변경 이의신청 기간 경과 후 허가사항 변경 명령 즉시 시행을 거친다. 의약품 안전성·유효성 허가사항 신속 반영 방안은 최신의 안전성과 유효성 자료를 바탕으로 심사를 거쳐 원개발사 품목에 반영된 효능·효과 등 허가사항을 제네릭의약품에도 반영하는 시간 차이를 최소화하기 위해 마련했다. 식약처는 "이번 의약품 안전성·유효성 허가사항 신속 반영 방안 운영이 제네릭의약품을 사용하는 의·약사, 환자 등에게 최신 의약품 정보를 신속히 제공하는 데 도움이 될 것"으로 기대했다.2022-08-26 09:01:56이혜경
오늘의 TOP 10
- 1복지부 "한약사약국 전문약 취급 지자체가 관리하라"
- 2약사 16명, 6.3 지방선거 본선 티켓…민주 8명·국힘 5명
- 3배당 한 번 없었는데 성과급?…삼성바이오 주주권 침해 논란
- 4'코싹엘' 처방 시장 승승장구…계속되는 약가인상 선순환
- 5식품에 의약품 유사 명칭 못쓴다…식약처, 행정예고
- 6동성제약, 회생절차 종결 결정…거래재개 수순 본격화
- 7동성제약, 현금성자산 1600억 급증…부분자본잠식 여전
- 8홍승권 심평원장, 취임 한 달…"공공정책수가로 지필공 혁신"
- 9"KDDF, 투자 심의 고도화…완주형 신약 개발 키운다"
- 10AZ '토조라키맙' COPD서 가능성…생물의약품 경쟁 확대









































