총 271건
-
 부광, 유니온제약 인수…공장은 얻었지만 부채는 부담[데일리팜=최다은 기자] 부광약품이 회생절차를 밟고 있는 한국유니온제약 인수에 나선다. 이번 거래의 득과 실은 분명하다. 부족한 생산능력(CAPA)을 단숨에 보완할 수 있다는 점은 확실한 기대 요인인 반면, 완전자본잠식 기업을 떠안는 데 따른 재무 부담은 피할 수 없는 과제다. 신약 파이프라인이나 영업망 확보가 아닌 공장 중심의 구조조정형 인수라는 점에서, 이번 거래는 전통적인 제약사 M&A와는 결이 다르다는 평가다.부광약품은 지난 17일 유니온제약 인수를 위한 우선협상대상자로 선정돼 조건부 투자계약을 체결했다. 이번 거래는 서울회생법원이 주관하는 인가 전 인수합병(M&A)으로, 공개 경쟁입찰을 병행하는 ‘스토킹호스’ 방식이 적용된다.부광약품에 필요한 건 ‘공장’이었다부광약품은 이번 계약을 통해 생산능력 확충뿐만 아니라 ETC(전문의약품) 중심 만성질환 치료 영역으로 포트폴리오를 확장하는 전략적 발판을 마련했다는 입장이다. 부광약품은 1985년 완공한 회사 안산공장이 공간적 제약으로 인해 지난 40년간 생산 추가 설비를 늘리지 못해왔다. 따라서 안산공장의 가동률은 100%를 초과하며 이미 생산능력(capacity)를 초과해 가동돼왔다. 부광약품은 지난 7월 유상증자를 893억원을 조달한 바 있다. 당시 조달 자금의 대부분을 제조시설 확충과 공장 취득에 투입하겠다고 밝히며 생산 능력 강화 필요성을 지속적으로 언급해왔다. 또한 합성의약품 기반 CDMO(위탁개발생산) 시장 진출을 통한 상시적 현금창출 구조를 구축도 모색해왔다. 유니온제약은 강원 원주 문막공장 캐파를 꾸준히 확대해왔다. 특히 액상주사제 생산능력은 유니온제약이 부광약품의 두 배 이상인 것으로 알려졌다. 부광약품은 유니온제약을 인수하면 의약품 생산능력이 30%가량 증가할 것으로 보고 있다.부광약품 관계자는 "이번 인수의 1차 목적은 올해 초 유상증자 과정에서 밝혔듯 부족한 기존 안산공장의 생산능력을 보강하는데 중점을 뒀다"며 "유니온제약 공장은 지난 2020년 3월 대단위공장 GMP(의약품 제조·품질관리) 허가를 마친 최신 시설이며, 항생제 라인 등 부광약품과의 시너지가 날 만한 포트폴리오도 갖고 있어 인수를 결정했다"고 말했다.부광약품은 유니온제약 공장 인수로 항생제·주사제 포트폴리오를 다각화를 기대하고 있다. 그동안 부광약품이 보유하지 않았던 세파계 항생제 제조라인을 확보하고, 세팔로스포린계 항생제 전용 작업소와 품목허가를 확보한다는 구상이다. 이처럼 인수가 성공적으로 마무리될 경우 부광약품은 상대적으로 제한적인 투자로 추가 생산 캐파(CAPA)를 확보할 수 있다. 중장기적으로는 자체 제품 생산 외에도 위탁생산(CMO·CDMO) 등으로 활용 범위를 넓힐 여지도 있다.특히 부광약품이 연구개발과 신제품 출시를 재정비하고 있는 상황에서, 외주 생산 의존도를 낮추고 공급 안정성을 확보할 수 있다는 점은 전략적 장점으로 꼽힌다.공장과 함께 떠안은 재무 부담리스크도 만만치 않다. 유니온제약은 완전자본잠식 상태로, 인수 이후에도 추가적인 자금 투입이 불가피하다. 설비 개선, 인력 재편, 내부 통제 시스템 구축 등 정상화 과정에서 예상보다 큰 비용이 발생할 가능성도 배제하기 어렵다.유니온제약의 올 9월말 연결 기준 자산총계는 약 543억원이지만, 부채총계는 약 636억원으로 자본총계가 마이너스 상태다. 같은 기간 유동 부채는 427억원으로 유동자산(198억원)의 두 배 이상이다. 1년 이내에 현금화되는 돈보다 갚아야 하는 돈이 더 많다는 뜻이다.회생 기업 인수 특성 상 인수 이후에도 소송, 채무 관계, 잠재 부채 등은 변수로 작용할 수 있다.유니온제약의 공장·토지·건물 등 유형자산 장부금액 합계는 289억원인데, 이 자산에 걸려 있는 담보 설정금액과 압류 등 권리 총량은 414억원 수준이다. 담보로 잡힌 자산의 값보다, 그 자산을 근거로 청구할 수 있는 채권 규모가 더 크다는 의미다.올 3분기 기준 유니온제약의 차입금은 모두 만기 1년 이하로 빌린 돈인 단기차입금(211억원)으로만 구성된다. 같은 기간 부광약품의 현금 유동성은(현금 및 현금성자산, 단기금융상품 포함) 약 2200억원 가량이다. 유니온제약 인수를 위해 충분한 실탄을 확보했다는 것이 부광약품 측 입장이지만, 회생 기업 특성상 인수 후 발생할 수 있는 추가 비용과 잠재 리스크까지 감안하면 자금 부담이 예상보다 커질 수 있다는 지적이 나온다. 당장 금전적인 문제가 해결했다 하더라도 공장 정상화와 조직 재편 및 인프라 확충 비용 등이 동시에 발생할 경우 현금 유동성 소모 속도가 빨라질 수 있어서다.이에 따라 부광약품은 유니온제약의 장·단기 부채 상환을 위해 중장기적으로 추가 자금조달이 필요해질 수 있다. 인수 절차가 스토킹호스 방식인 점도 입찰 경쟁 기업이 등장할 경우 최종 인수가가 높아질 수 있어 부담으로 작용할 전망이다. 스토킹호스는 미리 선정된 매수 희망자의 제시 가격을 기준으로 더 나은 조건을 제시할 인수를 추가로 찾는 구조다. 공개 입찰에서 경쟁자가 나타날 경우 최종 매각 가격은 상승하게 된다. 만약 인수가가 예상보다 높아지게 되면 부광약품의 재무 부담과 잠재 리스크도 가중되는 셈이다. 업계 관계자는 “부광약품 입장에서는 생산 캐파 확보라는 명확한 목적이 있는 인수지만, 스토킹호스 방식 특성상 인수가가 상승해 기대 수익과 리스크 간 균형이 흔들릴 수 있다”며 “결국 인수 성패는 얼마나 빠르게 공장을 정상화하고, 불필요한 사업을 정리해 현금 유출을 통제하느냐에 달려 있다”고 평가했다.이어 “유니온제약을 통해 단기간 외형을 키우기보다는, CDMO 등으로 안정적인 현금 창출 구조를 만들 수 있을지도 관건”이라고 말했다.2025-12-19 12:02:58최다은 기자
부광, 유니온제약 인수…공장은 얻었지만 부채는 부담[데일리팜=최다은 기자] 부광약품이 회생절차를 밟고 있는 한국유니온제약 인수에 나선다. 이번 거래의 득과 실은 분명하다. 부족한 생산능력(CAPA)을 단숨에 보완할 수 있다는 점은 확실한 기대 요인인 반면, 완전자본잠식 기업을 떠안는 데 따른 재무 부담은 피할 수 없는 과제다. 신약 파이프라인이나 영업망 확보가 아닌 공장 중심의 구조조정형 인수라는 점에서, 이번 거래는 전통적인 제약사 M&A와는 결이 다르다는 평가다.부광약품은 지난 17일 유니온제약 인수를 위한 우선협상대상자로 선정돼 조건부 투자계약을 체결했다. 이번 거래는 서울회생법원이 주관하는 인가 전 인수합병(M&A)으로, 공개 경쟁입찰을 병행하는 ‘스토킹호스’ 방식이 적용된다.부광약품에 필요한 건 ‘공장’이었다부광약품은 이번 계약을 통해 생산능력 확충뿐만 아니라 ETC(전문의약품) 중심 만성질환 치료 영역으로 포트폴리오를 확장하는 전략적 발판을 마련했다는 입장이다. 부광약품은 1985년 완공한 회사 안산공장이 공간적 제약으로 인해 지난 40년간 생산 추가 설비를 늘리지 못해왔다. 따라서 안산공장의 가동률은 100%를 초과하며 이미 생산능력(capacity)를 초과해 가동돼왔다. 부광약품은 지난 7월 유상증자를 893억원을 조달한 바 있다. 당시 조달 자금의 대부분을 제조시설 확충과 공장 취득에 투입하겠다고 밝히며 생산 능력 강화 필요성을 지속적으로 언급해왔다. 또한 합성의약품 기반 CDMO(위탁개발생산) 시장 진출을 통한 상시적 현금창출 구조를 구축도 모색해왔다. 유니온제약은 강원 원주 문막공장 캐파를 꾸준히 확대해왔다. 특히 액상주사제 생산능력은 유니온제약이 부광약품의 두 배 이상인 것으로 알려졌다. 부광약품은 유니온제약을 인수하면 의약품 생산능력이 30%가량 증가할 것으로 보고 있다.부광약품 관계자는 "이번 인수의 1차 목적은 올해 초 유상증자 과정에서 밝혔듯 부족한 기존 안산공장의 생산능력을 보강하는데 중점을 뒀다"며 "유니온제약 공장은 지난 2020년 3월 대단위공장 GMP(의약품 제조·품질관리) 허가를 마친 최신 시설이며, 항생제 라인 등 부광약품과의 시너지가 날 만한 포트폴리오도 갖고 있어 인수를 결정했다"고 말했다.부광약품은 유니온제약 공장 인수로 항생제·주사제 포트폴리오를 다각화를 기대하고 있다. 그동안 부광약품이 보유하지 않았던 세파계 항생제 제조라인을 확보하고, 세팔로스포린계 항생제 전용 작업소와 품목허가를 확보한다는 구상이다. 이처럼 인수가 성공적으로 마무리될 경우 부광약품은 상대적으로 제한적인 투자로 추가 생산 캐파(CAPA)를 확보할 수 있다. 중장기적으로는 자체 제품 생산 외에도 위탁생산(CMO·CDMO) 등으로 활용 범위를 넓힐 여지도 있다.특히 부광약품이 연구개발과 신제품 출시를 재정비하고 있는 상황에서, 외주 생산 의존도를 낮추고 공급 안정성을 확보할 수 있다는 점은 전략적 장점으로 꼽힌다.공장과 함께 떠안은 재무 부담리스크도 만만치 않다. 유니온제약은 완전자본잠식 상태로, 인수 이후에도 추가적인 자금 투입이 불가피하다. 설비 개선, 인력 재편, 내부 통제 시스템 구축 등 정상화 과정에서 예상보다 큰 비용이 발생할 가능성도 배제하기 어렵다.유니온제약의 올 9월말 연결 기준 자산총계는 약 543억원이지만, 부채총계는 약 636억원으로 자본총계가 마이너스 상태다. 같은 기간 유동 부채는 427억원으로 유동자산(198억원)의 두 배 이상이다. 1년 이내에 현금화되는 돈보다 갚아야 하는 돈이 더 많다는 뜻이다.회생 기업 인수 특성 상 인수 이후에도 소송, 채무 관계, 잠재 부채 등은 변수로 작용할 수 있다.유니온제약의 공장·토지·건물 등 유형자산 장부금액 합계는 289억원인데, 이 자산에 걸려 있는 담보 설정금액과 압류 등 권리 총량은 414억원 수준이다. 담보로 잡힌 자산의 값보다, 그 자산을 근거로 청구할 수 있는 채권 규모가 더 크다는 의미다.올 3분기 기준 유니온제약의 차입금은 모두 만기 1년 이하로 빌린 돈인 단기차입금(211억원)으로만 구성된다. 같은 기간 부광약품의 현금 유동성은(현금 및 현금성자산, 단기금융상품 포함) 약 2200억원 가량이다. 유니온제약 인수를 위해 충분한 실탄을 확보했다는 것이 부광약품 측 입장이지만, 회생 기업 특성상 인수 후 발생할 수 있는 추가 비용과 잠재 리스크까지 감안하면 자금 부담이 예상보다 커질 수 있다는 지적이 나온다. 당장 금전적인 문제가 해결했다 하더라도 공장 정상화와 조직 재편 및 인프라 확충 비용 등이 동시에 발생할 경우 현금 유동성 소모 속도가 빨라질 수 있어서다.이에 따라 부광약품은 유니온제약의 장·단기 부채 상환을 위해 중장기적으로 추가 자금조달이 필요해질 수 있다. 인수 절차가 스토킹호스 방식인 점도 입찰 경쟁 기업이 등장할 경우 최종 인수가가 높아질 수 있어 부담으로 작용할 전망이다. 스토킹호스는 미리 선정된 매수 희망자의 제시 가격을 기준으로 더 나은 조건을 제시할 인수를 추가로 찾는 구조다. 공개 입찰에서 경쟁자가 나타날 경우 최종 매각 가격은 상승하게 된다. 만약 인수가가 예상보다 높아지게 되면 부광약품의 재무 부담과 잠재 리스크도 가중되는 셈이다. 업계 관계자는 “부광약품 입장에서는 생산 캐파 확보라는 명확한 목적이 있는 인수지만, 스토킹호스 방식 특성상 인수가가 상승해 기대 수익과 리스크 간 균형이 흔들릴 수 있다”며 “결국 인수 성패는 얼마나 빠르게 공장을 정상화하고, 불필요한 사업을 정리해 현금 유출을 통제하느냐에 달려 있다”고 평가했다.이어 “유니온제약을 통해 단기간 외형을 키우기보다는, CDMO 등으로 안정적인 현금 창출 구조를 만들 수 있을지도 관건”이라고 말했다.2025-12-19 12:02:58최다은 기자 -
 녹십자 리브말리액 1월 급여 등재...듀피젠트 천식 급여 확대녹십자 '리브말리액'[데일리팜=정흥준 기자]담즙정체성 소양증 치료제로 사용하는 녹십자 ‘리브말리액(마라릭시뱃염화물)’이 1월 급여 등재된다. 또 듀피젠트프리필드주300mg(두필루맙)이 중증 제2형 염증성 천식에 급여 확대된다.19일 업계에 따르면, 녹십자의 리브말리액은 내달 급여 목록표에 이름을 올린다. 상한액은 2900만2835원이다.리브말리액은 지난 8월 약평위를 통과하며 급여 적정성을 인정받은 바 있다. 알라질증후군 환자의 담즙정체성 소양증 치료 효과로 빌베이(오데빅시바트)와는 유사 약제로 분류되는 치료제다.리브말리액이 등재되며 급여기준도 신설됐다. 알라질증후군(Alagille syndrome) 진단 받은 생후 3개월 이상의 환자로 ▲혈청 담즙산(sBA, serum bile acid) 농도가 100μmol/L 이상인 경우 ▲CGIS 점수가 2점 이상인 중등도 이상의 소양증 환자는 급여 적용된다.첫 투약 후 6개월 평가 시 치료 반응을 만족하는 경우 추가 6개월의 투여를 인정하기로 했다.간 이식을 받은 경우나 비대상성 간 경변, 간 보상기전 상실(정맥류 출혈, 복수, 간성 뇌 병증 등)은 급여 대상에서 제외된다.사노피-아벤티스코리아의 듀피젠트는 내달 ‘성인 및 청소년의 중증 제2형 염증성 천식’에 급여 확대된다. 1월부터 듀피젠트300mg 상한액은 67만5753원으로, 종전 67만5807원에서 소폭 조정된다. 확대되는 급여 적용 대상은 ▲치료 시작 전 12개월 이내 혈중 호산구 수치가 150 cells/㎕ 이상 또는 호기산화질소(FeNO)가 25 ppb 이상이면서 치료 시작 전 12개월 이내 전신 코르티코스테로이드가 요구되는 천식 급성 악화가 4번 이상 발생한 경우 ▲치료 시작 6개월 전부터 prednisolone 5mg/day 이상과 동등한 수준의 경구 코르티코스테로이드를 지속적으로 투여한 경우다.평가 방법은 약제 투여 전-후 매 1년마다(경구 코르티코스테로이드 의존성 천식의 경우 매 6개월마다) 평가해 두 가지 조건 중 하나에 해당하면 인정한다.두 조건은 ▲천식 급성 악화의 빈도가 치료 시작 전 대비 50% 이상 감소 ▲지속적인 경구 코르티코스테로이드 치료가 필요한 환자의 경우 천식 증상 조절을 개선하거나 유지하면서 경구 코르티코스테로이드 용량이 치료 시작 전 대비 50% 이상 감소한 경우다.2025-12-19 06:00:48정흥준 기자
녹십자 리브말리액 1월 급여 등재...듀피젠트 천식 급여 확대녹십자 '리브말리액'[데일리팜=정흥준 기자]담즙정체성 소양증 치료제로 사용하는 녹십자 ‘리브말리액(마라릭시뱃염화물)’이 1월 급여 등재된다. 또 듀피젠트프리필드주300mg(두필루맙)이 중증 제2형 염증성 천식에 급여 확대된다.19일 업계에 따르면, 녹십자의 리브말리액은 내달 급여 목록표에 이름을 올린다. 상한액은 2900만2835원이다.리브말리액은 지난 8월 약평위를 통과하며 급여 적정성을 인정받은 바 있다. 알라질증후군 환자의 담즙정체성 소양증 치료 효과로 빌베이(오데빅시바트)와는 유사 약제로 분류되는 치료제다.리브말리액이 등재되며 급여기준도 신설됐다. 알라질증후군(Alagille syndrome) 진단 받은 생후 3개월 이상의 환자로 ▲혈청 담즙산(sBA, serum bile acid) 농도가 100μmol/L 이상인 경우 ▲CGIS 점수가 2점 이상인 중등도 이상의 소양증 환자는 급여 적용된다.첫 투약 후 6개월 평가 시 치료 반응을 만족하는 경우 추가 6개월의 투여를 인정하기로 했다.간 이식을 받은 경우나 비대상성 간 경변, 간 보상기전 상실(정맥류 출혈, 복수, 간성 뇌 병증 등)은 급여 대상에서 제외된다.사노피-아벤티스코리아의 듀피젠트는 내달 ‘성인 및 청소년의 중증 제2형 염증성 천식’에 급여 확대된다. 1월부터 듀피젠트300mg 상한액은 67만5753원으로, 종전 67만5807원에서 소폭 조정된다. 확대되는 급여 적용 대상은 ▲치료 시작 전 12개월 이내 혈중 호산구 수치가 150 cells/㎕ 이상 또는 호기산화질소(FeNO)가 25 ppb 이상이면서 치료 시작 전 12개월 이내 전신 코르티코스테로이드가 요구되는 천식 급성 악화가 4번 이상 발생한 경우 ▲치료 시작 6개월 전부터 prednisolone 5mg/day 이상과 동등한 수준의 경구 코르티코스테로이드를 지속적으로 투여한 경우다.평가 방법은 약제 투여 전-후 매 1년마다(경구 코르티코스테로이드 의존성 천식의 경우 매 6개월마다) 평가해 두 가지 조건 중 하나에 해당하면 인정한다.두 조건은 ▲천식 급성 악화의 빈도가 치료 시작 전 대비 50% 이상 감소 ▲지속적인 경구 코르티코스테로이드 치료가 필요한 환자의 경우 천식 증상 조절을 개선하거나 유지하면서 경구 코르티코스테로이드 용량이 치료 시작 전 대비 50% 이상 감소한 경우다.2025-12-19 06:00:48정흥준 기자 -
 8억원 체납한 허모 약사 등 고액 상습체납 약사 실명공개[데일리팜=강신국 기자]8억 8800만원의 세금을 체납한 허00 약사 등 2025년 고액상습체납자 명단이 공개됐다. 국세청(청장 임광현)은 국세체납액이 2억원 이상인 개인 6848명, 법인 4161개의 명단을 국세청 누리집을 통해 공개했다고 12일 밝혔다.이중 상호명 약국을 검색해 보니 총 6명의 약사가 고액상습체납자 명단에 이름을 올렸다.19건의 종합소득세 등 8억 8800만원을 체납한 ▲허00 약사(55) 외에 ▲김00 약사(62) 5억7700만원 ▲배00 약사(80) 3억 8500만원 ▲이00 약사(80) 3억 8500만원 ▲조00 약사(75) 3억6000만원 ▲유00 약사(74) 2억6200만원 등이었다.병원으로 검색하면 한방병원 3곳, 병원 2곳 등이었다. 의원급에서는 총 13곳의 실명이 공개됐다. 이중 어린이한의원을 운영한 안00 한의사는 10억 900만원의 세금을 체납했다. 한편 올해 신규 공개대상은 개인 6848명(4조661원), 법인 4161개(2조9710억원)다. 총 체납액은 7조371억원이다. 신규 공개대상자는 지난해(9666명)에 비해 1343명 늘며 처음으로 1만명을 넘어섰다.체납액도 전년(6조1896억원)보다 8475억원 증가했다. 개인 명단 공개자 중 3938명(57.5%)이 수도권(경기·서울·인천)에 거주했다. 체납액은 2억∼5억원 구간에 5350명(78.1%)이 몰려 있다.연령별로 50대가 2353명(34.4%)으로 비중이 가장 컸다. 개인 최고액 체납자인 권혁 시도그룹 회장은 종합소득세 등 3938억원을 내지 않았다.2025-12-13 06:00:54강신국 기자
8억원 체납한 허모 약사 등 고액 상습체납 약사 실명공개[데일리팜=강신국 기자]8억 8800만원의 세금을 체납한 허00 약사 등 2025년 고액상습체납자 명단이 공개됐다. 국세청(청장 임광현)은 국세체납액이 2억원 이상인 개인 6848명, 법인 4161개의 명단을 국세청 누리집을 통해 공개했다고 12일 밝혔다.이중 상호명 약국을 검색해 보니 총 6명의 약사가 고액상습체납자 명단에 이름을 올렸다.19건의 종합소득세 등 8억 8800만원을 체납한 ▲허00 약사(55) 외에 ▲김00 약사(62) 5억7700만원 ▲배00 약사(80) 3억 8500만원 ▲이00 약사(80) 3억 8500만원 ▲조00 약사(75) 3억6000만원 ▲유00 약사(74) 2억6200만원 등이었다.병원으로 검색하면 한방병원 3곳, 병원 2곳 등이었다. 의원급에서는 총 13곳의 실명이 공개됐다. 이중 어린이한의원을 운영한 안00 한의사는 10억 900만원의 세금을 체납했다. 한편 올해 신규 공개대상은 개인 6848명(4조661원), 법인 4161개(2조9710억원)다. 총 체납액은 7조371억원이다. 신규 공개대상자는 지난해(9666명)에 비해 1343명 늘며 처음으로 1만명을 넘어섰다.체납액도 전년(6조1896억원)보다 8475억원 증가했다. 개인 명단 공개자 중 3938명(57.5%)이 수도권(경기·서울·인천)에 거주했다. 체납액은 2억∼5억원 구간에 5350명(78.1%)이 몰려 있다.연령별로 50대가 2353명(34.4%)으로 비중이 가장 컸다. 개인 최고액 체납자인 권혁 시도그룹 회장은 종합소득세 등 3938억원을 내지 않았다.2025-12-13 06:00:54강신국 기자 -
 '고마진 원료로 실탄 확보'...에스티팜, 신약 개발 외연 확장[데일리팜=차지현 기자] 에스티팜이 신약개발 분야로 보폭을 넓히고 있다. 올리고뉴클레오타이드 원료의약품(CDMO) 사업을 통해 벌어들인 안정적인 수익을 바탕으로 메신저 리보핵산(mRNA)과 유전자 편집 치료제 등 차세대 RNA 치료제 시장 공략에 속도를 내는 분위기다.13일 바이오 업계에 따르면 에스티팜은 최근 전염병예방혁신연합(CEPI)이 추진하는 중증열성혈소판감소증후군(SFTS) mRNA 백신 개발 프로젝트의 핵심 제조·기술 파트너로 선정됐다.이번 연구는 인공지능(AI)·구조기반 설계를 활용해 항원 후보물질을 도출하고 면역원성과 안전성을 검증하는 장기 연구다. 오는 2030년까지 CEPI의 지원을 받아 수행될 예정이다. 질병관리청 국립보건연구원과 국제백신연구소(IVI), 서울대학교가 공동으로 참여한다.백신 후보물질은 질병관리청과 서울대학교가 항원을 설계하고 에스티팜은 mRNA 원료 설계와 생산을 담당한다. 구체적으로 에스티팜은 자체 mRNA 5’ 캡핑 기술(SmartCap)과 지질나노입자(LNP) 전달 기술(STLNP), 글로벌 표준의 GMP 제조 역량을 제공한다.SFTS는 국내 비롯한 중국·일본·대만 등 동아시아에서 주로 발생하는 참진드기 매개 감염병이다. 고열과 혈소판 감소, 신부전 등을 일으켜 고령 환자에게서는 치명률이 높은 질환이다. 바이러스 면역 회피 특성 탓에 아직 상용화된 백신이 없는 상황으로 mRNA 백신은 항원 구조를 정밀하게 구현해 효과적인 면역 반응을 유도할 수 있을 것이라는 게 회사 측 기대다.에스티팜은 올해 들어 mRNA와 차세대 RNA 치료제 분야에서 존재감을 본격적으로 드러내고 있다. 회사는 올해 TIDES USA 2025와 CRISPR MEDiCiNE 2025 등 RNA·유전자 치료제 분야를 대표하는 국제 학회에 연이어 참가하며 적극적인 대외 행보에 나섰다. 해당 학회에서 에스티팜은 mRNA 관련 자체 플랫폼을 소개하고 gRNA 등 mRNA 플랫폼 응용 범위를 유전자치료제 영역까지 확장하겠다는 중장기 전략과 비전을 제시했다.가시적인 성과도 나오고 있다. 에스티팜은 올해 1분기와 2분기 각각 mRNA 부문 매출 6억원, 7억원을 기록하며 관련 사업에서 첫 실적을 창출했다. 3분기에는 mRNA 부문과 관련 초기 R&D 프로젝트에서 14억원의 매출을 올렸다. LNP 지질 중간체 공급과 mRNA 목록제품, 자체개발 캡핑 시약 CDMO를 통해 매출이 발생했다.에스티팜 mRNA CDMO 플랫폼 개요 (자료: 에스티팜)동아쏘시오그룹 계열사 에스티팜은 올리고와 저분자 화학합성 신약 원료의약품 위탁개발생산(CDMO)을 주력으로 영위하는 업체다. 당초 제네릭 원료의약품(API) 생산 업체로 출발했으나 이후 고성장·고부가가치 올리고 원료 생산 중심으로 사업 구조를 고도화해 왔다. 최근에는 mRNA와 유전자 편집 치료제 등 차세대 RNA 치료제 분야로 사업 영역 확장을 꾀하는 모습이다.에스티팜은 2020년 mRNA 사업에 처음 뛰어들었다. 코로나19 팬데믹을 계기로 mRNA 기술의 상업적 가능성이 부각되자 같은 해 8월 반월캠퍼스에 비임상 실험용 mRNA 생산 설비 증설에 착수하며 관련 사업을 본격화했다. 이후 단계적으로 투자를 확대해 상업화 수준 mRNA 원액 생산 설비를 완공하며 생산 인프라를 갖췄다.에스티팜은 2020년 8월 반월캠퍼스 내 비임상 실험용 규모 증설을 시작으로 2021년 5월 추가 증설을 완료했고 2023년 8월 연간 3000만~1억 도즈 상당 상업화 규모 mRNA 백신 원액을 생산할 수 있는 설비를 완공했다. mRNA 분자를 안정화하는 핵심기술을 독자화하고 mRNA 약물 전달의 핵심기술인 LNP를 공동개발하는 등 핵심 플랫폼 기술도 내재화했다.나아가 에스티팜은 신약개발 영역으로도 보폭을 넓히는 중이다. 단순 mRNA 원료 위탁생산에 그치지 않고 자체 원천기술을 바탕으로 백신·치료제 개발 과정에 직접 참여하는 전략으로 방향을 전환한 것이다.회사는 mRNA 기반 코로나19 백신 후보물질 'STP2104' 개발에 나섰다. STP2104는 코로나19 바이러스의 스파이크 단백질 정보를 담은 mRNA에 T세포 면역을 강화하는 요소를 추가해, 항체와 세포 면역을 동시에 유도하는 백신이다. 에스티팜은 STP2104 임상 1상에서 글로벌 mRNA 백신과 동등 이상의 중화항체 역가와 항체양전율을 확인했다. 다만 전략적 판단에 따라 임상 1상 이후 추가 개발은 중단한 상태다.회사는 미국 자회사를 통해 mRNA 기반 혁신 신약 파이프라인을 강화하는 데 힘을 쏟고 있다. 에스티팜은 2021년 4, 미국 샌디에이고에 mRNA와 CAR-NKT 플랫폼 기술을 이용한 신약개발 바이오텍 레바티오 테라퓨틱스를 설립했다. 또 같은 해 8월 미국 애틀랜타에 mRNA 신약개발 바이오텍 버나젠을 설립했다.현재 버나젠은 현재 10여 개의 항바이러스 질환 mRNA 백신 파이프라인을 보유 중이다. 특히 2023년 3월에는 미국질병청(CDC)와 하트랜드바이러스 mRNA 백신 공동연구개발 업무협약(MOU)을 체결하고 7월 본계약을 완료했다. 백신 개발에 에스티팜의 SmartCap과 STLNP 플랫폼 기술을 적용하는 게 골자다. 레바티오의 경우 작년 말 청산했으나 CAR-NKT, cirRNA 등 핵심 플랫폼 기술 IP와 신약 파이프라인은 모두 에스티팜에게 이전돼 관련 연구를 지속하고 있다.이 같은 신사업 확장 동력은 기존 CDMO 사업에서 창출되는 안정적인 현금흐름에서 나온다. 올 3분기 에스티팜 영업이익은 147억원으로 전년 동기 대비 141.6% 급증했다. 같은 기간 매출액은 819억원으로 전년보다 32.7% 늘었다. 고마진 올리고핵산 CDMO 비중 확대와 상업화 프로젝트 증가가 맞물린 결과다. 매출 구성을 보면 올리고 CDMO 매출이 686억원으로 전체 매출의 84%를 차지했고 이 가운데 상업화 단계 프로젝트가 절반 이상인 54%를 차지해 수익성 개선을 이끌었다.2025-12-13 06:00:53차지현 기자
'고마진 원료로 실탄 확보'...에스티팜, 신약 개발 외연 확장[데일리팜=차지현 기자] 에스티팜이 신약개발 분야로 보폭을 넓히고 있다. 올리고뉴클레오타이드 원료의약품(CDMO) 사업을 통해 벌어들인 안정적인 수익을 바탕으로 메신저 리보핵산(mRNA)과 유전자 편집 치료제 등 차세대 RNA 치료제 시장 공략에 속도를 내는 분위기다.13일 바이오 업계에 따르면 에스티팜은 최근 전염병예방혁신연합(CEPI)이 추진하는 중증열성혈소판감소증후군(SFTS) mRNA 백신 개발 프로젝트의 핵심 제조·기술 파트너로 선정됐다.이번 연구는 인공지능(AI)·구조기반 설계를 활용해 항원 후보물질을 도출하고 면역원성과 안전성을 검증하는 장기 연구다. 오는 2030년까지 CEPI의 지원을 받아 수행될 예정이다. 질병관리청 국립보건연구원과 국제백신연구소(IVI), 서울대학교가 공동으로 참여한다.백신 후보물질은 질병관리청과 서울대학교가 항원을 설계하고 에스티팜은 mRNA 원료 설계와 생산을 담당한다. 구체적으로 에스티팜은 자체 mRNA 5’ 캡핑 기술(SmartCap)과 지질나노입자(LNP) 전달 기술(STLNP), 글로벌 표준의 GMP 제조 역량을 제공한다.SFTS는 국내 비롯한 중국·일본·대만 등 동아시아에서 주로 발생하는 참진드기 매개 감염병이다. 고열과 혈소판 감소, 신부전 등을 일으켜 고령 환자에게서는 치명률이 높은 질환이다. 바이러스 면역 회피 특성 탓에 아직 상용화된 백신이 없는 상황으로 mRNA 백신은 항원 구조를 정밀하게 구현해 효과적인 면역 반응을 유도할 수 있을 것이라는 게 회사 측 기대다.에스티팜은 올해 들어 mRNA와 차세대 RNA 치료제 분야에서 존재감을 본격적으로 드러내고 있다. 회사는 올해 TIDES USA 2025와 CRISPR MEDiCiNE 2025 등 RNA·유전자 치료제 분야를 대표하는 국제 학회에 연이어 참가하며 적극적인 대외 행보에 나섰다. 해당 학회에서 에스티팜은 mRNA 관련 자체 플랫폼을 소개하고 gRNA 등 mRNA 플랫폼 응용 범위를 유전자치료제 영역까지 확장하겠다는 중장기 전략과 비전을 제시했다.가시적인 성과도 나오고 있다. 에스티팜은 올해 1분기와 2분기 각각 mRNA 부문 매출 6억원, 7억원을 기록하며 관련 사업에서 첫 실적을 창출했다. 3분기에는 mRNA 부문과 관련 초기 R&D 프로젝트에서 14억원의 매출을 올렸다. LNP 지질 중간체 공급과 mRNA 목록제품, 자체개발 캡핑 시약 CDMO를 통해 매출이 발생했다.에스티팜 mRNA CDMO 플랫폼 개요 (자료: 에스티팜)동아쏘시오그룹 계열사 에스티팜은 올리고와 저분자 화학합성 신약 원료의약품 위탁개발생산(CDMO)을 주력으로 영위하는 업체다. 당초 제네릭 원료의약품(API) 생산 업체로 출발했으나 이후 고성장·고부가가치 올리고 원료 생산 중심으로 사업 구조를 고도화해 왔다. 최근에는 mRNA와 유전자 편집 치료제 등 차세대 RNA 치료제 분야로 사업 영역 확장을 꾀하는 모습이다.에스티팜은 2020년 mRNA 사업에 처음 뛰어들었다. 코로나19 팬데믹을 계기로 mRNA 기술의 상업적 가능성이 부각되자 같은 해 8월 반월캠퍼스에 비임상 실험용 mRNA 생산 설비 증설에 착수하며 관련 사업을 본격화했다. 이후 단계적으로 투자를 확대해 상업화 수준 mRNA 원액 생산 설비를 완공하며 생산 인프라를 갖췄다.에스티팜은 2020년 8월 반월캠퍼스 내 비임상 실험용 규모 증설을 시작으로 2021년 5월 추가 증설을 완료했고 2023년 8월 연간 3000만~1억 도즈 상당 상업화 규모 mRNA 백신 원액을 생산할 수 있는 설비를 완공했다. mRNA 분자를 안정화하는 핵심기술을 독자화하고 mRNA 약물 전달의 핵심기술인 LNP를 공동개발하는 등 핵심 플랫폼 기술도 내재화했다.나아가 에스티팜은 신약개발 영역으로도 보폭을 넓히는 중이다. 단순 mRNA 원료 위탁생산에 그치지 않고 자체 원천기술을 바탕으로 백신·치료제 개발 과정에 직접 참여하는 전략으로 방향을 전환한 것이다.회사는 mRNA 기반 코로나19 백신 후보물질 'STP2104' 개발에 나섰다. STP2104는 코로나19 바이러스의 스파이크 단백질 정보를 담은 mRNA에 T세포 면역을 강화하는 요소를 추가해, 항체와 세포 면역을 동시에 유도하는 백신이다. 에스티팜은 STP2104 임상 1상에서 글로벌 mRNA 백신과 동등 이상의 중화항체 역가와 항체양전율을 확인했다. 다만 전략적 판단에 따라 임상 1상 이후 추가 개발은 중단한 상태다.회사는 미국 자회사를 통해 mRNA 기반 혁신 신약 파이프라인을 강화하는 데 힘을 쏟고 있다. 에스티팜은 2021년 4, 미국 샌디에이고에 mRNA와 CAR-NKT 플랫폼 기술을 이용한 신약개발 바이오텍 레바티오 테라퓨틱스를 설립했다. 또 같은 해 8월 미국 애틀랜타에 mRNA 신약개발 바이오텍 버나젠을 설립했다.현재 버나젠은 현재 10여 개의 항바이러스 질환 mRNA 백신 파이프라인을 보유 중이다. 특히 2023년 3월에는 미국질병청(CDC)와 하트랜드바이러스 mRNA 백신 공동연구개발 업무협약(MOU)을 체결하고 7월 본계약을 완료했다. 백신 개발에 에스티팜의 SmartCap과 STLNP 플랫폼 기술을 적용하는 게 골자다. 레바티오의 경우 작년 말 청산했으나 CAR-NKT, cirRNA 등 핵심 플랫폼 기술 IP와 신약 파이프라인은 모두 에스티팜에게 이전돼 관련 연구를 지속하고 있다.이 같은 신사업 확장 동력은 기존 CDMO 사업에서 창출되는 안정적인 현금흐름에서 나온다. 올 3분기 에스티팜 영업이익은 147억원으로 전년 동기 대비 141.6% 급증했다. 같은 기간 매출액은 819억원으로 전년보다 32.7% 늘었다. 고마진 올리고핵산 CDMO 비중 확대와 상업화 프로젝트 증가가 맞물린 결과다. 매출 구성을 보면 올리고 CDMO 매출이 686억원으로 전체 매출의 84%를 차지했고 이 가운데 상업화 단계 프로젝트가 절반 이상인 54%를 차지해 수익성 개선을 이끌었다.2025-12-13 06:00:53차지현 기자 -
 대웅, 권역별 거점도매 추진…도매·약국에 미칠 여파는?[데일리팜=김지은 기자] 대웅제약이 수년 전 논란이 됐던 권역별 거점도매 운영 카드를 다시 꺼내들면서 일선 의약품 도매업계는 물론이고 약국에도 영향을 미칠 것이라는 전망이 나온다. 대웅제약은 최근 ‘대웅그룹 블록형 거점도매 업체 선정’ 입찰 공고를 내고 오늘(9일)까지 도매업체들로부터 입찰 참가의향서 및 비밀유지서약서를 받고 있다. 이번 입찰 발주처는 대웅그룹에 소속된 대웅제약, 대웅바이오, 한올바이오로, 회사는 전국을 10개 권역으로 나눠 각 권역을 대표해 의약품 품질, 배송, 환입, 알림 서비스를 제공할 거점도매를 선정해 운영한다고 밝혔다. 선정된 블록형 거점도매는 권역별 물류대행 기능과 제품유통(종합도매)을 수행하게 된다는 것이 회사 설명이다. 계약 기간은 1년이며, 회사 평가에 따라 계약 연장 여부가 결정되며, 제한경쟁 입찰 방식이다. 입찰 참가 자격 중에는 순바닥 면적이 1500㎡ 이상인 KGSP 창고를 보유해야 한다는 조건도 포함됐다. 회사는 지난 5일에 공고문을 게시한 후 4일 만인 오늘까지 도매업체들에 의향서를 제출하게 한 상황이다. 대웅제약의 이 같은 결정의 배경에는 유통 비용을 줄이고 채권 부담을 낮추려는 목적이 있다는 분석이다. 자율경쟁 입찰 방식을 도입한 만큼 현재보다 유통 마진을 낮출 수 있는 상황도 만들어지는 셈이다. 대형 제약사의 거점도매 운영과 관련해서는 의약분업 직후에 이어 지난 5년 전에도 논란이 불거진 바 있다. 일부 제약사가 거점도매 체제를 만들겠다고 나선 데 대해 도매협회가 거세게 반발하면서 무산된 바 있었다. 당시 도매협회는 이 같은 제약사 주도 유통 구조 개편이 소규모 도매의 생존 위협과 더불어 유통 독점화 를 가져올 수 있다고 우려했었다. 도매업계 한 관계자는 대웅제약의 이번 결정에 대해 “일정 부분 자체적으로 거래할 업체를 정해 놓고 방식은 자유경쟁이라는 명목으로 입찰을 진행하는 것 아니냐는 생각도 있다”며 “사실상 내건 조건에 충족할 수 있는 업체는 제한적일 수 밖에 없다. 지방 도매들은 대부분이 해당되지 않을수 있다”고 말했다. 또 다른 도매 관계자는 "거래 유통사를 최소화하고 회사가 자체 운영 중인 온라인몰을 통한 유통에 더욱 집중하려는 의중도 있을 것”이라고 했다. 이번 공개 입찰을 두고 도매업계 당황하는 분위기다. 도매협회는 오늘 오전 회의 중 대웅제약의 이번 거점도매 입찰에 대한 대응 방안 등을 논의할 방침인 것으로 알려졌다. 의약품 유통 전문가들은 대형 제약사의 이 같은 거점도매 운영 방식이 일선 요양기관, 약국에 불편이 전가될 가능성이 있다고 전망했다. 약업계 한 관계자는 “대웅과 같이 대형 제약사가 전국 10곳 도매를 통해서만 약을 유통한다는 것인데 결국 일선 약국, 특히 지방 약국의 경우 이전보다 약을 전달 받는데 제한적일 수 밖에 없다”며 “더불어 제약사가 거점도매와의 계약 과정에서 반품 등의 조건을 타이트하게 가져갈 수 밖에 없다. 대웅의 이번 결정이 다른 제약사들에도 영향을 미칠 수 있다. 그 여파는 약국에 전가 될 수 밖에 없을 것”이라고 말했다.2025-12-10 06:00:56김지은 기자
대웅, 권역별 거점도매 추진…도매·약국에 미칠 여파는?[데일리팜=김지은 기자] 대웅제약이 수년 전 논란이 됐던 권역별 거점도매 운영 카드를 다시 꺼내들면서 일선 의약품 도매업계는 물론이고 약국에도 영향을 미칠 것이라는 전망이 나온다. 대웅제약은 최근 ‘대웅그룹 블록형 거점도매 업체 선정’ 입찰 공고를 내고 오늘(9일)까지 도매업체들로부터 입찰 참가의향서 및 비밀유지서약서를 받고 있다. 이번 입찰 발주처는 대웅그룹에 소속된 대웅제약, 대웅바이오, 한올바이오로, 회사는 전국을 10개 권역으로 나눠 각 권역을 대표해 의약품 품질, 배송, 환입, 알림 서비스를 제공할 거점도매를 선정해 운영한다고 밝혔다. 선정된 블록형 거점도매는 권역별 물류대행 기능과 제품유통(종합도매)을 수행하게 된다는 것이 회사 설명이다. 계약 기간은 1년이며, 회사 평가에 따라 계약 연장 여부가 결정되며, 제한경쟁 입찰 방식이다. 입찰 참가 자격 중에는 순바닥 면적이 1500㎡ 이상인 KGSP 창고를 보유해야 한다는 조건도 포함됐다. 회사는 지난 5일에 공고문을 게시한 후 4일 만인 오늘까지 도매업체들에 의향서를 제출하게 한 상황이다. 대웅제약의 이 같은 결정의 배경에는 유통 비용을 줄이고 채권 부담을 낮추려는 목적이 있다는 분석이다. 자율경쟁 입찰 방식을 도입한 만큼 현재보다 유통 마진을 낮출 수 있는 상황도 만들어지는 셈이다. 대형 제약사의 거점도매 운영과 관련해서는 의약분업 직후에 이어 지난 5년 전에도 논란이 불거진 바 있다. 일부 제약사가 거점도매 체제를 만들겠다고 나선 데 대해 도매협회가 거세게 반발하면서 무산된 바 있었다. 당시 도매협회는 이 같은 제약사 주도 유통 구조 개편이 소규모 도매의 생존 위협과 더불어 유통 독점화 를 가져올 수 있다고 우려했었다. 도매업계 한 관계자는 대웅제약의 이번 결정에 대해 “일정 부분 자체적으로 거래할 업체를 정해 놓고 방식은 자유경쟁이라는 명목으로 입찰을 진행하는 것 아니냐는 생각도 있다”며 “사실상 내건 조건에 충족할 수 있는 업체는 제한적일 수 밖에 없다. 지방 도매들은 대부분이 해당되지 않을수 있다”고 말했다. 또 다른 도매 관계자는 "거래 유통사를 최소화하고 회사가 자체 운영 중인 온라인몰을 통한 유통에 더욱 집중하려는 의중도 있을 것”이라고 했다. 이번 공개 입찰을 두고 도매업계 당황하는 분위기다. 도매협회는 오늘 오전 회의 중 대웅제약의 이번 거점도매 입찰에 대한 대응 방안 등을 논의할 방침인 것으로 알려졌다. 의약품 유통 전문가들은 대형 제약사의 이 같은 거점도매 운영 방식이 일선 요양기관, 약국에 불편이 전가될 가능성이 있다고 전망했다. 약업계 한 관계자는 “대웅과 같이 대형 제약사가 전국 10곳 도매를 통해서만 약을 유통한다는 것인데 결국 일선 약국, 특히 지방 약국의 경우 이전보다 약을 전달 받는데 제한적일 수 밖에 없다”며 “더불어 제약사가 거점도매와의 계약 과정에서 반품 등의 조건을 타이트하게 가져갈 수 밖에 없다. 대웅의 이번 결정이 다른 제약사들에도 영향을 미칠 수 있다. 그 여파는 약국에 전가 될 수 밖에 없을 것”이라고 말했다.2025-12-10 06:00:56김지은 기자 -
 "매출을 줄일 수도 없고"...약가우대 'R&D 비율'의 역차별[데일리팜=김진구 기자] GLP-1 계열 비만치료제 ‘위고비’로 글로벌 제약바이오 시장을 휩쓸고 있는 노보노디스크가 지난 2024년 지출한 R&D 비용은 480억6200만 덴마크크로네(DKK), 당시 환율로는 약 9조5400억원에 달한다.그러나 노보노디스크가 한국 약가제도 개편안에 따라 평가될 경우, ‘약가 가산 최고우대 구간(68%)’을 적용받지 못한다. 개편안에서 약가가산 조건을 ‘R&D 투자 비율’로만 판단하기 때문이다.이처럼 막대한 R&D 자금을 투자하고도 약가제도 개편안 기준에선 약가 가산을 충분히 받지 못하는 모순이 발생한다는 지적이다. ‘기업의 혁신성’에 정책적으로 우대하겠다는 정부 취지가 정작 실제 투자 규모가 큰 기업에겐 제대로 반영되지 않는다는 비판이 제기되는 배경이다.혁신형 제약기업 중 ‘R&D 비율 상위 30%’에 약가가산 최고 우대 적용8일 제약업계에 따르면 정부는 최근 발표한 약가제도 개편안에서 '혁신성에 대한 정책적 우대를 강화한다'고 밝혔다. 혁신형 제약기업 등의 R&D 투자 수준에 따라 가산율을 차등하는 방식이다.이때 중요한 기준은 ‘매출액 대비 R&D 투자 비율’이다. 혁신형 제약기업 중 R&D 비율이 상위 30%인 기업엔 68% 수준의 약가 가산율을, 하위 70%인 기업엔 60%의 가산율을 각각 적용한다. 또한 국내 매출 500억원 미만이면서 신약개발을 위한 임상2상 승인 실적이 3년간 1건 이상인 기업엔 55%의 가산율을 적용한다.이를 혁신형 제약기업 49곳에 적용하면, 총 15곳이 최고우대 구간인 68%의 가산율을 적용받는다는 계산이 나온다.작년 말 기준 혁신형 제약기업 중 R&D 투자 비율 상위 30%는 브릿지바이오테라퓨틱스, 지아이이노베이션, 제넥신, 올릭스, 큐리언트, 에이비엘바이오, 헬릭스미스, 온코닉테라퓨틱스, 알테오젠, 코아스템, 테고사이언스, SK바이오사이언스, LG화학(생명과학 부문), SK바이오팜, 한올바이오파마 등이다.작년 말 기준 R&D 투자 비율이 공개되지 않거나 매출이 없어 계산되지 않는 SK케미칼(제약사업부), 삼양홀딩스(삼양바이오팜), 큐로셀과 다국적제약사 한국법인 4곳(암젠코리아·한국아스트라제네카·한국얀센·한국오츠카)는 집계에서 제외했다.상위 30% 기업 중 브릿지바이오·지아이이노베이션·제넥신·올릭스·큐리언트·에이비엘바이오·헬릭스미스는 매출액보다 R&D 지출이 많다. 온코닉테라퓨틱스와 알테오젠은 R&D 비율이 50% 이상이다. 상위 30% 기업의 마지노선인 한올바이오파마의 R&D 비율은 26.3%다.바꿔 말해, 작년 말 기준 R&D 비율이 26% 미만인 혁신형 제약기업은 약가가산 최고우대 구간을 적용받기 힘들 수 있다는 의미다.매출 규모 클수록 불리…국내 기준 적용 시 글로벌 빅파마 상당수 탈락제약업계에선 매출 규모가 클수록 불리한 기준이라는 비판이 제기된다. 실제로 상위 30% 혁신형 제약기업 대부분은 LG화학 생명과학 부문과 SK바이오팜, SK바이어사이언스 정도를 제외하면 2024년 매출 규모가 크지 않다.반대로 말해 2024년에만 1000억원 이상 R&D 자금을 투입한 셀트리온(4347억원), 유한양행(2688억원), 대웅제약(2346억원), 한미약품(2098억원), 녹십자(1747억원), 동아에스티(1348억원) 등은 최고구간 적용을 받지 못하는 셈이다. 같은 기준을 글로벌 빅파마에 적용하면 더욱 역설적인 상황이 펼쳐진다. 상위 30% 기업의 R&D 비율 최소 기준인 '26% 미만'의 주요 글로벌 빅파마는 2024년 기준 ▲일라이릴리(24.4%) ▲베링거인겔하임(23.2%) ▲BMS(23.1%) ▲로슈(21.6%) ▲바이오젠(21.0%) ▲길리어드사이언스(20.5%) ▲GSK(20.4%) ▲노바티스(19.9%) ▲존슨앤드존슨(19.1%) ▲사노피(18.0%) ▲암젠(18.0%) ▲화이자(17.0%) ▲다케다제약(16.7%) ▲노보노디스크(16.6%) ▲바이엘(13.7%) 등이다. 정부가 국내제약사의 혁신을 요구하며 롤모델로 제시하는 기업들이다.이들의 R&D 투자 규모가 작기 때문이 아니다. 존슨앤드존슨을 예로 들면 2024년에만 170억 달러(약 23조원)을 R&D에 쏟아부었다. 릴리와 BMS, 로슈, 노바티스, 화이자도 R&D에만 100억 달러 이상 지출했다.매출액 기준 따라 분류해도 마찬가지…제약업계 “단편적 평가 구조 개선해야”이와 관련 정부는 매출 규모를 기준으로 한 ‘그룹별 평가’ 운영 방침을 검토하고 있다. 매출 규모가 큰 기업과 작은 기업, 바이오벤처 등으로 나눠 약가가산을 차등 적용하는 방식으로 해석된다.그러나 이러한 방식으로도 모순적인 상황은 마찬가지라다는 비판이 나온다. 일례로 2024년 매출 기준 5000억원 이상을 '대형제약사 그룹'으로 묶을 경우, 셀트리온·유한양행·녹십자·한미약품·대웅제약·HK이노엔·보령·동국제약·동아에스티·SK바이오팜·한독에 LG화학 생명과학부문 등 12개 기업이 해당한다.이 가운데 R&D 비율 상위 30%인 4개 기업은 LG화학 생명과학부문(34.1%), SK바이오팜(29.5%), 동아에스티(19.2%), 대웅제약(18.5%)이다. 자체 신약을 보유한 한미약품(14.0%)과 유한양행(13.0%), 셀트리온(12.2%), 녹십자(10.4%)는 여전히 제외될 가능성이 크다.글로벌 빅파마에 같은 기준을 적용해도 마찬가지다. 대웅제약의 18.5%보다 R&D 투자비율이 낮은 사노피·암젠·화이자·다케다제약·노보노디스크·바이엘은 최고우대 구간을 적용받지 못한다. 모두 R&D 투자에 소극적이라서가 아니라, 매출 규모가 크기 때문이다.나머지 기업들도 마찬가지다. 매출액이 거의 없는 R&D 전문 바이오벤처와 매출 규모가 작은 중소제약사를 어떻게 구분할지도 관건이다. 혁신형 제약기업 중 바이오벤처로 구분된 12곳을 예로 들면, 4곳이 약가가산 최고우대를 받는다. 반대로 말해 큐리언트·에이비엘바이오·헬릭스미스는 매출액을 넘어서는 R&D 자금을 지출하고서도 최고우대를 받지 못한다는 의미다.사정이 이렇다보니 제약업계에선 단편적인 평가 구조를 개선해야 한다는 목소리가 높다. 매출 규모가 클수록 불리한 현행 개편안에 대한 개선이 시급하다는 비판이다.한 대형제약사 관계자는 “혁신형 제약기업 인증 땐 R&D 투자실적 외에 연구인력 현황, 연구·생산시설 현황, 연구개발 비전과 중장기 추진 전략, 국내외 연구기관과의 제휴·협력활동, 의약품 특허, 기술이전과 해외진출 성과 등을 종합적으로 판단하면서 정작 기업들에게 가장 필요한 약가가산 때는 R&D 투자 비율만 본다는 점에 문제가 있다”고 지적했다.그는 “매출이 클수록 불리한 구조에선 R&D 투자에 대한 유인 동기가 크지 않다. 단편적인 평가구조의 개선이 절실하다”며 “개편안 내용대로 약가가산 제도가 바뀔 경우 혁신형 제약기업 인증 제도 자체가 유명무실해질 것”이라고 우려했다.또 다른 제약사 관계자는 ”최고우대 구간을 적용받더라도 현행 우대율(68%)과 동일하다“며 ”기업의 혁신성에 정책적으로 확실한 우대를 제공하려면 현실성을 반영한 재검토가 필요하다”고 말했다.2025-12-08 06:00:59김진구 기자
"매출을 줄일 수도 없고"...약가우대 'R&D 비율'의 역차별[데일리팜=김진구 기자] GLP-1 계열 비만치료제 ‘위고비’로 글로벌 제약바이오 시장을 휩쓸고 있는 노보노디스크가 지난 2024년 지출한 R&D 비용은 480억6200만 덴마크크로네(DKK), 당시 환율로는 약 9조5400억원에 달한다.그러나 노보노디스크가 한국 약가제도 개편안에 따라 평가될 경우, ‘약가 가산 최고우대 구간(68%)’을 적용받지 못한다. 개편안에서 약가가산 조건을 ‘R&D 투자 비율’로만 판단하기 때문이다.이처럼 막대한 R&D 자금을 투자하고도 약가제도 개편안 기준에선 약가 가산을 충분히 받지 못하는 모순이 발생한다는 지적이다. ‘기업의 혁신성’에 정책적으로 우대하겠다는 정부 취지가 정작 실제 투자 규모가 큰 기업에겐 제대로 반영되지 않는다는 비판이 제기되는 배경이다.혁신형 제약기업 중 ‘R&D 비율 상위 30%’에 약가가산 최고 우대 적용8일 제약업계에 따르면 정부는 최근 발표한 약가제도 개편안에서 '혁신성에 대한 정책적 우대를 강화한다'고 밝혔다. 혁신형 제약기업 등의 R&D 투자 수준에 따라 가산율을 차등하는 방식이다.이때 중요한 기준은 ‘매출액 대비 R&D 투자 비율’이다. 혁신형 제약기업 중 R&D 비율이 상위 30%인 기업엔 68% 수준의 약가 가산율을, 하위 70%인 기업엔 60%의 가산율을 각각 적용한다. 또한 국내 매출 500억원 미만이면서 신약개발을 위한 임상2상 승인 실적이 3년간 1건 이상인 기업엔 55%의 가산율을 적용한다.이를 혁신형 제약기업 49곳에 적용하면, 총 15곳이 최고우대 구간인 68%의 가산율을 적용받는다는 계산이 나온다.작년 말 기준 혁신형 제약기업 중 R&D 투자 비율 상위 30%는 브릿지바이오테라퓨틱스, 지아이이노베이션, 제넥신, 올릭스, 큐리언트, 에이비엘바이오, 헬릭스미스, 온코닉테라퓨틱스, 알테오젠, 코아스템, 테고사이언스, SK바이오사이언스, LG화학(생명과학 부문), SK바이오팜, 한올바이오파마 등이다.작년 말 기준 R&D 투자 비율이 공개되지 않거나 매출이 없어 계산되지 않는 SK케미칼(제약사업부), 삼양홀딩스(삼양바이오팜), 큐로셀과 다국적제약사 한국법인 4곳(암젠코리아·한국아스트라제네카·한국얀센·한국오츠카)는 집계에서 제외했다.상위 30% 기업 중 브릿지바이오·지아이이노베이션·제넥신·올릭스·큐리언트·에이비엘바이오·헬릭스미스는 매출액보다 R&D 지출이 많다. 온코닉테라퓨틱스와 알테오젠은 R&D 비율이 50% 이상이다. 상위 30% 기업의 마지노선인 한올바이오파마의 R&D 비율은 26.3%다.바꿔 말해, 작년 말 기준 R&D 비율이 26% 미만인 혁신형 제약기업은 약가가산 최고우대 구간을 적용받기 힘들 수 있다는 의미다.매출 규모 클수록 불리…국내 기준 적용 시 글로벌 빅파마 상당수 탈락제약업계에선 매출 규모가 클수록 불리한 기준이라는 비판이 제기된다. 실제로 상위 30% 혁신형 제약기업 대부분은 LG화학 생명과학 부문과 SK바이오팜, SK바이어사이언스 정도를 제외하면 2024년 매출 규모가 크지 않다.반대로 말해 2024년에만 1000억원 이상 R&D 자금을 투입한 셀트리온(4347억원), 유한양행(2688억원), 대웅제약(2346억원), 한미약품(2098억원), 녹십자(1747억원), 동아에스티(1348억원) 등은 최고구간 적용을 받지 못하는 셈이다. 같은 기준을 글로벌 빅파마에 적용하면 더욱 역설적인 상황이 펼쳐진다. 상위 30% 기업의 R&D 비율 최소 기준인 '26% 미만'의 주요 글로벌 빅파마는 2024년 기준 ▲일라이릴리(24.4%) ▲베링거인겔하임(23.2%) ▲BMS(23.1%) ▲로슈(21.6%) ▲바이오젠(21.0%) ▲길리어드사이언스(20.5%) ▲GSK(20.4%) ▲노바티스(19.9%) ▲존슨앤드존슨(19.1%) ▲사노피(18.0%) ▲암젠(18.0%) ▲화이자(17.0%) ▲다케다제약(16.7%) ▲노보노디스크(16.6%) ▲바이엘(13.7%) 등이다. 정부가 국내제약사의 혁신을 요구하며 롤모델로 제시하는 기업들이다.이들의 R&D 투자 규모가 작기 때문이 아니다. 존슨앤드존슨을 예로 들면 2024년에만 170억 달러(약 23조원)을 R&D에 쏟아부었다. 릴리와 BMS, 로슈, 노바티스, 화이자도 R&D에만 100억 달러 이상 지출했다.매출액 기준 따라 분류해도 마찬가지…제약업계 “단편적 평가 구조 개선해야”이와 관련 정부는 매출 규모를 기준으로 한 ‘그룹별 평가’ 운영 방침을 검토하고 있다. 매출 규모가 큰 기업과 작은 기업, 바이오벤처 등으로 나눠 약가가산을 차등 적용하는 방식으로 해석된다.그러나 이러한 방식으로도 모순적인 상황은 마찬가지라다는 비판이 나온다. 일례로 2024년 매출 기준 5000억원 이상을 '대형제약사 그룹'으로 묶을 경우, 셀트리온·유한양행·녹십자·한미약품·대웅제약·HK이노엔·보령·동국제약·동아에스티·SK바이오팜·한독에 LG화학 생명과학부문 등 12개 기업이 해당한다.이 가운데 R&D 비율 상위 30%인 4개 기업은 LG화학 생명과학부문(34.1%), SK바이오팜(29.5%), 동아에스티(19.2%), 대웅제약(18.5%)이다. 자체 신약을 보유한 한미약품(14.0%)과 유한양행(13.0%), 셀트리온(12.2%), 녹십자(10.4%)는 여전히 제외될 가능성이 크다.글로벌 빅파마에 같은 기준을 적용해도 마찬가지다. 대웅제약의 18.5%보다 R&D 투자비율이 낮은 사노피·암젠·화이자·다케다제약·노보노디스크·바이엘은 최고우대 구간을 적용받지 못한다. 모두 R&D 투자에 소극적이라서가 아니라, 매출 규모가 크기 때문이다.나머지 기업들도 마찬가지다. 매출액이 거의 없는 R&D 전문 바이오벤처와 매출 규모가 작은 중소제약사를 어떻게 구분할지도 관건이다. 혁신형 제약기업 중 바이오벤처로 구분된 12곳을 예로 들면, 4곳이 약가가산 최고우대를 받는다. 반대로 말해 큐리언트·에이비엘바이오·헬릭스미스는 매출액을 넘어서는 R&D 자금을 지출하고서도 최고우대를 받지 못한다는 의미다.사정이 이렇다보니 제약업계에선 단편적인 평가 구조를 개선해야 한다는 목소리가 높다. 매출 규모가 클수록 불리한 현행 개편안에 대한 개선이 시급하다는 비판이다.한 대형제약사 관계자는 “혁신형 제약기업 인증 땐 R&D 투자실적 외에 연구인력 현황, 연구·생산시설 현황, 연구개발 비전과 중장기 추진 전략, 국내외 연구기관과의 제휴·협력활동, 의약품 특허, 기술이전과 해외진출 성과 등을 종합적으로 판단하면서 정작 기업들에게 가장 필요한 약가가산 때는 R&D 투자 비율만 본다는 점에 문제가 있다”고 지적했다.그는 “매출이 클수록 불리한 구조에선 R&D 투자에 대한 유인 동기가 크지 않다. 단편적인 평가구조의 개선이 절실하다”며 “개편안 내용대로 약가가산 제도가 바뀔 경우 혁신형 제약기업 인증 제도 자체가 유명무실해질 것”이라고 우려했다.또 다른 제약사 관계자는 ”최고우대 구간을 적용받더라도 현행 우대율(68%)과 동일하다“며 ”기업의 혁신성에 정책적으로 확실한 우대를 제공하려면 현실성을 반영한 재검토가 필요하다”고 말했다.2025-12-08 06:00:59김진구 기자 -
 "현행과 큰 차이 없는데"...제약업계 '약가가산 개편'에 분통정부가 약가가산 제도 전반을 손보는 개편안을 내놨지만, 제약바이오업계에선 ‘보상 체계가 달라진 게 없다’는 반응이 지배적이다. 기업의 연구개발(R&D) 투자와 필수의약품 공급 기여도를 기준으로 정부가 확실한 우대를 제공한다고 밝혔지만, 실제 보상 수준은 현행 제도와 큰 차이가 없고 오히려 적용 요건만 복잡해졌다는 지적이 이어진다. R&D 비율 따라 최대 68% 가산…정부 “혁신 기업에 확실한 우대” 정부는 이번 개편안에서 약가 가산의 기준점을 기존 53.55%에서 40%대로 낮추는 대신, 혁신형 제약기업 여부와 R&D 투자 비중, 원료 직접 생산 여부 등을 기준으로 가산을 제공하는 구조로 바꾼다고 설명했다. 핵심은 ‘R&D 투자에 적극적인 기업에는 약가를 우대해준다’는 것이다. 기존에는 제네릭 최초 등재 시 1년간 기본가산 59.5%를 제공하고, 이듬해부터는 53.55%로 낮아지는 구조였다. 개편안에선 기본가산을 폐지하고, 제네릭 산정 기준점을 40%대로 낮춘다. 또한 혁신형 제약기업에 대한 약가 가산을 R&D 투자 비율에 따라 세분화한다. 구체적으로 ▲혁신형 제약기업 중 매출액 대비 R&D 비율이 상위 30%인 기업에 68%를 ▲하위 70% 기업엔 60%를 ▲국내 매출 500억원 미만이나 신약개발을 위한 임상 2상 승인 실적이 3년간 1건 이상인 기업에 55%를 각각 우대한다. 정부는 혁신형 제약기업 등 R&D 투자 수준에 따라 가산율을 차등하고, 가산이 적용되는 중에 R&D 투자 수준 변경이 발생하면, 이를 즉시 반영한다고 설명했다. 혁신형 제약기업 인증에서 탈락하거나, 투자 비율이 변경되면 즉시 약가가 떨어진다는 의미다. 정부는 “가산제도는 ‘혁신성’과 ‘수급안정 기여’ 중심으로 개편하되 정책적 우대를 확연히 체감할 수 있도록 할 예정“이라고 밝혔다. R&D 연계 가산이라더니 ‘현상 유지’…”약가 우대 아닌 선별적 허용“ 비판 표면적으로만 보면 기업의 혁신 노력에 대한 보상이 확대된 것처럼 보이지만, 세부 내용을 뜯어보면 ‘기존 제도와 똑같거나 오히려 적용 범위만 축소된 개편’이라는 평가가 나온다. 특히 현행 약가가산 수준과 비교하면 최고 우대 구간이 ‘68%’로 동일하다는 비판의 목소리가 크다. 현재도 혁신형 제약기업에는 68%의 약가 우대가 적용되고 있기 때문이다. 정부가 혁신 추구 기업엔 확연한 우대를 제공한다고 했지만, 잘해야 현상 유지에 그친다는 지적이다. 우대 대상도 제한적이다. 현재 혁신형 제약기업으로 지정된 업체는 총 49곳이다. 이 가운데 최고 우대 구간(68%)을 받는 업체는 R&D 투자 비율 상위 30%인 15곳에 그친다. 나머지 34곳은 60%를 적용받는다. 한 제약사 관계자는 “가산을 ‘주는 방식’으로 바꾼 것이 아니라 ‘주지 않을 이유’를 세분화한 것에 가깝다”며 “정부가 혁신 기업에 인센티브를 준다지만 실질적으로 현상을 유지하는 정도일 뿐, 혁신에 대한 인센티브라기엔 한계가 크다”고 지적했다. 혁신형 제약기업 가산 기간, ‘5년’서 ‘3년’으로 오히려 줄어들 가능성 가산 기간에 대한 우려도 커지고 있다. 현재는 혁신형 제약기업에 대해 68% 수준의 약가우대를 최대 ‘5년간’ 적용하고 있다. 개편안에선 55~68% 수준의 약가우대를 ‘3년+ α’로 제시했다. 정부안이 구체화되면 경우에 따라 가산기간이 되레 감소할 가능성이 있다. 투자 비율이 조금만 변동되더라도 약가 가산 구간이 즉시 재조정되는 방식도 문제로 지목된다. 기업 입장에선 분기별 실적 변동에 따라 약가가 수시로 달라질 수 있어 제품별 손익 예측이 불안정해지고, 현장에서도 약가 변동에 맞춘 청구·정산 과정이 반복되면서 업무 혼선이 불가피하다는 지적이다. 한 업계 관계자는 “보상 수준은 그대로면서 오히려 변동성만 커진 구조”라며 “가산 기간을 늘렸다는 정부 발표는 실효성 없는 숫자 조정에 불과하다”고 목소리를 높였다. ‘필수의약품 수급 안정’ 가산도 현행과 동일…정책 의지 의심하는 업계 정부가 이번 발표에서 강조한 또 다른 축은 ‘필수의약품 수급 안정 기여’ 기업에 대한 가산이다. 원료 직접 생산 또는 국산원료 사용 국가필수의약품에 대한 가산을 제공해 공급 기반을 강화한다는 게 정부 방침이다. 그러나 제약업계에선 가산율(68%)과 가산 기간(5+5년)이 모두 예전과 동일하다고 지적한다. 기존 가산으로도 공급 부족 문제가 해결되지 않았던 만큼, 동일한 우대로는 실질적인 생산 확대를 기대하기 어렵다는 지적이다. 실제로 정부는 올해 3월부터 국산 원료를 사용하는 국가필수의약품에 약가 우대를 적용했지만, 7개월 동안 신청한 제약사는 한 곳도 없었다. 이 문제는 올해 국정감사에서 지적됐다. 백종헌 의원은 "7개월째 국산 원료 사용 국가필수약 약가우대 신청 제약사가 한 곳도 없다는 점은 이름뿐인 제도가 시행되고 있다는 방증"이라며 "복지부가 규정 현실화에 나서지 않는다면 국산 원료약 산업 육성 정책은 실패할 것"이라고 지적했다. 사정이 이렇다보니 제약업계에선 정부의 정책 의지를 의심하는 목소리도 제기된다. 한 원료의약품 업체 관계자는 “수급 안정에 대한 정부 의지가 보이지 않는다. 현재와 같은 수준의 가산으로는 어떠한 기업도 생산 확대에 나서지 않을 것”이라고 전망했다. 한 중견제약사 관계자는 “가산 구조를 혁신적으로 바꿨다는 정부 설명과 달리 실제 기업이 체감할 변화는 거의 없다”며 “이번 개편은 ‘혁신 유도’라기보다 ‘가산 지급 기준 강화’에 가깝다”고 지적했다. 그는 “이 상태라면 R&D 투자 확대나 필수의약품 공급 강화라는 정부 목표는 달성하기 어렵다”며 “산업계 현실을 반영한 재검토가 필요하다”고 강조했다.2025-12-01 06:06:14김진구 기자
"현행과 큰 차이 없는데"...제약업계 '약가가산 개편'에 분통정부가 약가가산 제도 전반을 손보는 개편안을 내놨지만, 제약바이오업계에선 ‘보상 체계가 달라진 게 없다’는 반응이 지배적이다. 기업의 연구개발(R&D) 투자와 필수의약품 공급 기여도를 기준으로 정부가 확실한 우대를 제공한다고 밝혔지만, 실제 보상 수준은 현행 제도와 큰 차이가 없고 오히려 적용 요건만 복잡해졌다는 지적이 이어진다. R&D 비율 따라 최대 68% 가산…정부 “혁신 기업에 확실한 우대” 정부는 이번 개편안에서 약가 가산의 기준점을 기존 53.55%에서 40%대로 낮추는 대신, 혁신형 제약기업 여부와 R&D 투자 비중, 원료 직접 생산 여부 등을 기준으로 가산을 제공하는 구조로 바꾼다고 설명했다. 핵심은 ‘R&D 투자에 적극적인 기업에는 약가를 우대해준다’는 것이다. 기존에는 제네릭 최초 등재 시 1년간 기본가산 59.5%를 제공하고, 이듬해부터는 53.55%로 낮아지는 구조였다. 개편안에선 기본가산을 폐지하고, 제네릭 산정 기준점을 40%대로 낮춘다. 또한 혁신형 제약기업에 대한 약가 가산을 R&D 투자 비율에 따라 세분화한다. 구체적으로 ▲혁신형 제약기업 중 매출액 대비 R&D 비율이 상위 30%인 기업에 68%를 ▲하위 70% 기업엔 60%를 ▲국내 매출 500억원 미만이나 신약개발을 위한 임상 2상 승인 실적이 3년간 1건 이상인 기업에 55%를 각각 우대한다. 정부는 혁신형 제약기업 등 R&D 투자 수준에 따라 가산율을 차등하고, 가산이 적용되는 중에 R&D 투자 수준 변경이 발생하면, 이를 즉시 반영한다고 설명했다. 혁신형 제약기업 인증에서 탈락하거나, 투자 비율이 변경되면 즉시 약가가 떨어진다는 의미다. 정부는 “가산제도는 ‘혁신성’과 ‘수급안정 기여’ 중심으로 개편하되 정책적 우대를 확연히 체감할 수 있도록 할 예정“이라고 밝혔다. R&D 연계 가산이라더니 ‘현상 유지’…”약가 우대 아닌 선별적 허용“ 비판 표면적으로만 보면 기업의 혁신 노력에 대한 보상이 확대된 것처럼 보이지만, 세부 내용을 뜯어보면 ‘기존 제도와 똑같거나 오히려 적용 범위만 축소된 개편’이라는 평가가 나온다. 특히 현행 약가가산 수준과 비교하면 최고 우대 구간이 ‘68%’로 동일하다는 비판의 목소리가 크다. 현재도 혁신형 제약기업에는 68%의 약가 우대가 적용되고 있기 때문이다. 정부가 혁신 추구 기업엔 확연한 우대를 제공한다고 했지만, 잘해야 현상 유지에 그친다는 지적이다. 우대 대상도 제한적이다. 현재 혁신형 제약기업으로 지정된 업체는 총 49곳이다. 이 가운데 최고 우대 구간(68%)을 받는 업체는 R&D 투자 비율 상위 30%인 15곳에 그친다. 나머지 34곳은 60%를 적용받는다. 한 제약사 관계자는 “가산을 ‘주는 방식’으로 바꾼 것이 아니라 ‘주지 않을 이유’를 세분화한 것에 가깝다”며 “정부가 혁신 기업에 인센티브를 준다지만 실질적으로 현상을 유지하는 정도일 뿐, 혁신에 대한 인센티브라기엔 한계가 크다”고 지적했다. 혁신형 제약기업 가산 기간, ‘5년’서 ‘3년’으로 오히려 줄어들 가능성 가산 기간에 대한 우려도 커지고 있다. 현재는 혁신형 제약기업에 대해 68% 수준의 약가우대를 최대 ‘5년간’ 적용하고 있다. 개편안에선 55~68% 수준의 약가우대를 ‘3년+ α’로 제시했다. 정부안이 구체화되면 경우에 따라 가산기간이 되레 감소할 가능성이 있다. 투자 비율이 조금만 변동되더라도 약가 가산 구간이 즉시 재조정되는 방식도 문제로 지목된다. 기업 입장에선 분기별 실적 변동에 따라 약가가 수시로 달라질 수 있어 제품별 손익 예측이 불안정해지고, 현장에서도 약가 변동에 맞춘 청구·정산 과정이 반복되면서 업무 혼선이 불가피하다는 지적이다. 한 업계 관계자는 “보상 수준은 그대로면서 오히려 변동성만 커진 구조”라며 “가산 기간을 늘렸다는 정부 발표는 실효성 없는 숫자 조정에 불과하다”고 목소리를 높였다. ‘필수의약품 수급 안정’ 가산도 현행과 동일…정책 의지 의심하는 업계 정부가 이번 발표에서 강조한 또 다른 축은 ‘필수의약품 수급 안정 기여’ 기업에 대한 가산이다. 원료 직접 생산 또는 국산원료 사용 국가필수의약품에 대한 가산을 제공해 공급 기반을 강화한다는 게 정부 방침이다. 그러나 제약업계에선 가산율(68%)과 가산 기간(5+5년)이 모두 예전과 동일하다고 지적한다. 기존 가산으로도 공급 부족 문제가 해결되지 않았던 만큼, 동일한 우대로는 실질적인 생산 확대를 기대하기 어렵다는 지적이다. 실제로 정부는 올해 3월부터 국산 원료를 사용하는 국가필수의약품에 약가 우대를 적용했지만, 7개월 동안 신청한 제약사는 한 곳도 없었다. 이 문제는 올해 국정감사에서 지적됐다. 백종헌 의원은 "7개월째 국산 원료 사용 국가필수약 약가우대 신청 제약사가 한 곳도 없다는 점은 이름뿐인 제도가 시행되고 있다는 방증"이라며 "복지부가 규정 현실화에 나서지 않는다면 국산 원료약 산업 육성 정책은 실패할 것"이라고 지적했다. 사정이 이렇다보니 제약업계에선 정부의 정책 의지를 의심하는 목소리도 제기된다. 한 원료의약품 업체 관계자는 “수급 안정에 대한 정부 의지가 보이지 않는다. 현재와 같은 수준의 가산으로는 어떠한 기업도 생산 확대에 나서지 않을 것”이라고 전망했다. 한 중견제약사 관계자는 “가산 구조를 혁신적으로 바꿨다는 정부 설명과 달리 실제 기업이 체감할 변화는 거의 없다”며 “이번 개편은 ‘혁신 유도’라기보다 ‘가산 지급 기준 강화’에 가깝다”고 지적했다. 그는 “이 상태라면 R&D 투자 확대나 필수의약품 공급 강화라는 정부 목표는 달성하기 어렵다”며 “산업계 현실을 반영한 재검토가 필요하다”고 강조했다.2025-12-01 06:06:14김진구 기자 -
 제네릭 약가 산정 40% 수준으로…2012년 일괄인하 품목부터보건복지부가 제약산업 혁신 촉진과 환자 치료제 접근성 강화, 약제비 부담 완화를 타깃으로 신약·제네릭 모두를 담은 약가제도 개편에 나선다.시행 시점은 내년(2026년) 7월부터인데, 2012년 당해년도 일괄 약가인하 된 기등재 제네릭에 대해서만 향후 3년에 걸쳐 1차적으로 약가인하 하는 내용도 담겼다. 국내 제약사들은 신약 R&D(연구개발) 캐시카우인 기등재 제네릭 약가인하로 매출 타격이 불가피하다는 입장이다.개편안 시행 시점인 내년 7월 이후 건강보험 약제급여 등재되는 제네릭부터 변경될 약가제도를 적용해 달라는 게 국내 제약업계 요구사항이다.반면 복지부는 2012년도 일괄 약가인하 당시 깎인 제네릭 약가가 13년 뒤인 현재까지도 전혀 깎이지 않은 의약품에 대해서만 제한적으로 약가를 손질(인하)하는 것으로, 이론의 여지가 없는 행정이란 입장이다.28일 복지부는 2025년 제22차 건강보험정책심의위원회를 개최하고 약가제도 개선방안을 논의했다.복지부가 예고한 약가제도 개편안의 큰 틀은 일괄 약가인하 당시인 '2012년 당해년도 제네릭'에 대해서만 현재와 비교해 약가가 충분히 깎이지 않은 의약품을 타깃으로 내년부터 2029년까지 순차적으로 인하하는 내용이다.신약개발 생태계 조성복지부는 첫 번째 약가제도 개편 이유로 신약개발 생태계 조성을 꼽았다. 혁신 치료제 환자 접근성은 높이고, 국내 제약산업이 보다 혁신지향적으로 나아갈 수 있게 제도적 뒷받침을 강화한다.먼저 내년부터 희귀질환 치료제 등재 기간을 획기적으로 단축한다. 현재 240일인 등재 기간을 100일 이내로 줄일 방침이다.특히 중증·난치치료제 등 혁신 신약 가치를 평가·조정하는 평가 체계도 단계적으로 고도화한다.단기적으로는 ICER값 가중치 모델 도입 등 임계값을 적정 수준으로 상향하고 중장기적으로는 AI 등 디지털 헬스케어 기술을 접목해 임상 성과를 평가·반영하는 신규 모델을 정립한다.또 혁신 의약품이 국내 신속 도입되고 해외 시장에서 경쟁력을 가질 수 있게 약가유인계약제 적용 대상을 내년 1분기부터 대폭 확대한다.약가유연계약제는 일명 이중약가제로 불리는데, 이중약가제의 부정적 어감을 해소하기 위해 복지부가 만든 명칭이다.환자 접근성 강화를 위해 건보공단과 제약사 간 별도 계약으로 건보 신속·안정 등재를 지원하는 게 유연계약제 목표다.확대 대상은 신규등재 신약, 특허만료 오리지널, 위험분담제 환급 종료 신약, 바이오시밀러 등이다.특히 R&D에 적극 투자한 기업(혁신형 제약기업 등)에 대한 보상 체계는 혁신 창출 노력 정도에 비례해 보상하도록 정교화 해 내년 하반기부터 적용한다.약가 가산제도 개편 세부안은국내 제약사가 반발중인 제네릭 약가 가산제도 개편안은 현행 제네릭 산정률인 53.55%를 40%대 까지 낮추고, 혁신성, 수급 안정 기여 조건에 따라 우대해주는 게 골자다. 우리나라 약제비 구조와 주요국 사례를 분석한 결과가 40%대로 인하하는 근거다.적용 대상은 약가제도 개편안 시행일 이후인 내년 하반기부터 신규 등재되는 제네릭과 2012년도 일괄 약가인하 이후에도 현재까지 약가인하 없이 최초 산정가격인 53.55% 수준이 유지되고 있는 약제만 3~4년에 걸쳐 2030년까지 단계적으로 약가인하를 추진한다는 게 복지부 입장이다.2012년 4월 일괄 인하 이후부터 2026년 하반기 개편안 시행 직전까지 등재된 제네릭은 40%대 약가인하 개편안을 적용하지 않겠다는 얘기다.현재 복지부가 시행중인 제네릭 약가제도현행 제네릭 약가제도는 오리지널 특허 만료 후 최초 등재되는 퍼스트 제네릭은 59.5%, 나머지 제네릭은 53.55% 약가를 적용한다. 오리지널은 제네릭 최초 등재 시 70%로 약가를 깎고 이를 1년 유지해 가산한다.이 중 혁신형 제약기업과 원료 직접생산, 국산원료 사용 국가필수의약품은 68%까지 가산해 우대하는 게 현행 제네릭 가산제도다.복지부는 현행 가산제도에서 제네릭 약가 산정률을 53.55%에서 40%대로 크게 낮추고 퍼스트 제네릭에 부여했던 기본 가산 59.5%는 폐지한다. 특허만료 오리지널 약가 70% 적용은 변동없이 유지한다.눈 여겨 봐야 할 부분은 혁신형 제약사와 비혁신형 제약사에 대한 혁신성 약가 가산 기준 변경과 수급 안정 기여 조건 변경이다.혁신성 약가 가산의 경우, 혁신형 인증 제약사 중에서도 R&D 성과에 따라 약가 가산율·우대율을 차등한다.혁신형 제약사 가운데 매출액 대비 의약품 R&D 비율이 상위 30%인 제약사는 68%까지 약가를 우대해 가산하고, 혁신 제약사 중 나머지 즉 R&D 비율이 하위 70%인 경우엔 60%까지 우대 가산한다.복지부는 혁신형 제약사가 아닌 경우에도 제네릭 약가를 우대하는 기준도 마련했다.국내 매출 500억원 미만인 제약사 중에서 신약개발을 위한 임상2상 승인 실적이 3년 간 1건 이상인 제약사는 약가를 40%대에서 55%까지 가산한다. 단 임상1상이 결합된 복합임상 승인 건수는 가산 기준에서 제외된다.수급 안정에 기여한 제약사도 가산한다. 의약품 원료를 직접 생산한 제약사와 국산원료를 쓴 국가필수의약품 생산 제약사는 68%까지 약가를 우대한다.가산 기간도 늘린다. 퍼스트 제네릭 등재 때 오리지널에게 부여하는 가산률 70%는 현행 1년에서 3년으로 늘린다.혁신형 제약사와 비혁신형 제약사 중 임상2상 실적 우수 제약사는 각각 우대 가산 기간을 최소 3년을 보장하고 이후 조건에 따라 추가 가산 기간을 부여한다. '3+알파' 규정인데, 구체적인 가산 기준이나 기간은 아직 미정이라는 게 복지부 설명이다.원료 직접 생산 제약사와 국산원료 사용 국가필수약 가산 기간은 최소 5년, 이후 기준 충족 시 5년을 더 가산한다. 최대 10년 가산하는 셈이다.복지부는 혁신성과 수급안정 기여를 중심으로 가산제도를 개편하되, 정책적 우대를 확실히 체감할 수 있도록 한다는 의지다.품질이 낮은 제네릭이 무분별히 늘어나지 않게 계단식 인하와 다품목 등재 관리는 더 엄격히 강화한다는 계획이다.쉽게 말해 계단식 인하는 동일성분 11번째 품목부터 5%p씩 약가인하하고, 다품목 등재는 최초 제네릭 진입 시 10개 이상 제품이 등재되면 1년 경과 후 11번째 제제 약가로 일괄 조정한다는 얘기다.필수약 안정 공급체계 마련복지부는 필수약 수급 안정화를 위해 약가제도를 연계한다.장기간 개선 없이 운영된 퇴장방지약은 안정적으로 공급될 수 있게 지정기준을 상향하고 원가보전 기준 현실화 등 방안을 내년 하반기부터 시행한다.국가필수약 대상 약가 정책이 공급을 유도할 수 있도록 수급 친화적으로 개선한다. 적용 대상을 확대하고 우대기간을 안정적으로 보장하는 정책을 내년 1분기부터 신속 시행한다.또 민관 협력 대응체계를 기반으로 수급불안정 약제는 선제적으로 모니터링하고 원인별 맞춤 조치를 실시한다.사후관리제도 정비복지부는 기존 사후관리제도를 약가 조정 예측 가능성과 제도 운영 실효성을 높이는 방향으로 정비한다.사용범위 확대 약가인하와 사용량-약가 연동 약가인하 시기를 일치시키는 동시에 정례화한다.실거래가 조사 약가인하는 시장경쟁과 연동시켜 인센티브를 기반으로 실거래가 인하가 촉진되는 방향으로 재편하는 방안을 2027년부터 도입한다.급여적정성 재평가는 선별등재 이후 약제 역시 대상에 포함하되 임상 유용성 재검토 필요성이 확인된 약제 중심으로 평가한다.종합적 약가 평가·조정 기전을 내년안에 마련해 2027년부터 3~5년주기로 적용한다. 약가 운영 예측가능성은 높이고 약제비는 합리적으로 관리하는 체계 구축을 위해서다.약가제도 개편안은 이번 건정심 보고 후 추가 의견 수렴을 거쳐 최종 확정된다.2025-11-28 17:36:57이정환 기자
제네릭 약가 산정 40% 수준으로…2012년 일괄인하 품목부터보건복지부가 제약산업 혁신 촉진과 환자 치료제 접근성 강화, 약제비 부담 완화를 타깃으로 신약·제네릭 모두를 담은 약가제도 개편에 나선다.시행 시점은 내년(2026년) 7월부터인데, 2012년 당해년도 일괄 약가인하 된 기등재 제네릭에 대해서만 향후 3년에 걸쳐 1차적으로 약가인하 하는 내용도 담겼다. 국내 제약사들은 신약 R&D(연구개발) 캐시카우인 기등재 제네릭 약가인하로 매출 타격이 불가피하다는 입장이다.개편안 시행 시점인 내년 7월 이후 건강보험 약제급여 등재되는 제네릭부터 변경될 약가제도를 적용해 달라는 게 국내 제약업계 요구사항이다.반면 복지부는 2012년도 일괄 약가인하 당시 깎인 제네릭 약가가 13년 뒤인 현재까지도 전혀 깎이지 않은 의약품에 대해서만 제한적으로 약가를 손질(인하)하는 것으로, 이론의 여지가 없는 행정이란 입장이다.28일 복지부는 2025년 제22차 건강보험정책심의위원회를 개최하고 약가제도 개선방안을 논의했다.복지부가 예고한 약가제도 개편안의 큰 틀은 일괄 약가인하 당시인 '2012년 당해년도 제네릭'에 대해서만 현재와 비교해 약가가 충분히 깎이지 않은 의약품을 타깃으로 내년부터 2029년까지 순차적으로 인하하는 내용이다.신약개발 생태계 조성복지부는 첫 번째 약가제도 개편 이유로 신약개발 생태계 조성을 꼽았다. 혁신 치료제 환자 접근성은 높이고, 국내 제약산업이 보다 혁신지향적으로 나아갈 수 있게 제도적 뒷받침을 강화한다.먼저 내년부터 희귀질환 치료제 등재 기간을 획기적으로 단축한다. 현재 240일인 등재 기간을 100일 이내로 줄일 방침이다.특히 중증·난치치료제 등 혁신 신약 가치를 평가·조정하는 평가 체계도 단계적으로 고도화한다.단기적으로는 ICER값 가중치 모델 도입 등 임계값을 적정 수준으로 상향하고 중장기적으로는 AI 등 디지털 헬스케어 기술을 접목해 임상 성과를 평가·반영하는 신규 모델을 정립한다.또 혁신 의약품이 국내 신속 도입되고 해외 시장에서 경쟁력을 가질 수 있게 약가유인계약제 적용 대상을 내년 1분기부터 대폭 확대한다.약가유연계약제는 일명 이중약가제로 불리는데, 이중약가제의 부정적 어감을 해소하기 위해 복지부가 만든 명칭이다.환자 접근성 강화를 위해 건보공단과 제약사 간 별도 계약으로 건보 신속·안정 등재를 지원하는 게 유연계약제 목표다.확대 대상은 신규등재 신약, 특허만료 오리지널, 위험분담제 환급 종료 신약, 바이오시밀러 등이다.특히 R&D에 적극 투자한 기업(혁신형 제약기업 등)에 대한 보상 체계는 혁신 창출 노력 정도에 비례해 보상하도록 정교화 해 내년 하반기부터 적용한다.약가 가산제도 개편 세부안은국내 제약사가 반발중인 제네릭 약가 가산제도 개편안은 현행 제네릭 산정률인 53.55%를 40%대 까지 낮추고, 혁신성, 수급 안정 기여 조건에 따라 우대해주는 게 골자다. 우리나라 약제비 구조와 주요국 사례를 분석한 결과가 40%대로 인하하는 근거다.적용 대상은 약가제도 개편안 시행일 이후인 내년 하반기부터 신규 등재되는 제네릭과 2012년도 일괄 약가인하 이후에도 현재까지 약가인하 없이 최초 산정가격인 53.55% 수준이 유지되고 있는 약제만 3~4년에 걸쳐 2030년까지 단계적으로 약가인하를 추진한다는 게 복지부 입장이다.2012년 4월 일괄 인하 이후부터 2026년 하반기 개편안 시행 직전까지 등재된 제네릭은 40%대 약가인하 개편안을 적용하지 않겠다는 얘기다.현재 복지부가 시행중인 제네릭 약가제도현행 제네릭 약가제도는 오리지널 특허 만료 후 최초 등재되는 퍼스트 제네릭은 59.5%, 나머지 제네릭은 53.55% 약가를 적용한다. 오리지널은 제네릭 최초 등재 시 70%로 약가를 깎고 이를 1년 유지해 가산한다.이 중 혁신형 제약기업과 원료 직접생산, 국산원료 사용 국가필수의약품은 68%까지 가산해 우대하는 게 현행 제네릭 가산제도다.복지부는 현행 가산제도에서 제네릭 약가 산정률을 53.55%에서 40%대로 크게 낮추고 퍼스트 제네릭에 부여했던 기본 가산 59.5%는 폐지한다. 특허만료 오리지널 약가 70% 적용은 변동없이 유지한다.눈 여겨 봐야 할 부분은 혁신형 제약사와 비혁신형 제약사에 대한 혁신성 약가 가산 기준 변경과 수급 안정 기여 조건 변경이다.혁신성 약가 가산의 경우, 혁신형 인증 제약사 중에서도 R&D 성과에 따라 약가 가산율·우대율을 차등한다.혁신형 제약사 가운데 매출액 대비 의약품 R&D 비율이 상위 30%인 제약사는 68%까지 약가를 우대해 가산하고, 혁신 제약사 중 나머지 즉 R&D 비율이 하위 70%인 경우엔 60%까지 우대 가산한다.복지부는 혁신형 제약사가 아닌 경우에도 제네릭 약가를 우대하는 기준도 마련했다.국내 매출 500억원 미만인 제약사 중에서 신약개발을 위한 임상2상 승인 실적이 3년 간 1건 이상인 제약사는 약가를 40%대에서 55%까지 가산한다. 단 임상1상이 결합된 복합임상 승인 건수는 가산 기준에서 제외된다.수급 안정에 기여한 제약사도 가산한다. 의약품 원료를 직접 생산한 제약사와 국산원료를 쓴 국가필수의약품 생산 제약사는 68%까지 약가를 우대한다.가산 기간도 늘린다. 퍼스트 제네릭 등재 때 오리지널에게 부여하는 가산률 70%는 현행 1년에서 3년으로 늘린다.혁신형 제약사와 비혁신형 제약사 중 임상2상 실적 우수 제약사는 각각 우대 가산 기간을 최소 3년을 보장하고 이후 조건에 따라 추가 가산 기간을 부여한다. '3+알파' 규정인데, 구체적인 가산 기준이나 기간은 아직 미정이라는 게 복지부 설명이다.원료 직접 생산 제약사와 국산원료 사용 국가필수약 가산 기간은 최소 5년, 이후 기준 충족 시 5년을 더 가산한다. 최대 10년 가산하는 셈이다.복지부는 혁신성과 수급안정 기여를 중심으로 가산제도를 개편하되, 정책적 우대를 확실히 체감할 수 있도록 한다는 의지다.품질이 낮은 제네릭이 무분별히 늘어나지 않게 계단식 인하와 다품목 등재 관리는 더 엄격히 강화한다는 계획이다.쉽게 말해 계단식 인하는 동일성분 11번째 품목부터 5%p씩 약가인하하고, 다품목 등재는 최초 제네릭 진입 시 10개 이상 제품이 등재되면 1년 경과 후 11번째 제제 약가로 일괄 조정한다는 얘기다.필수약 안정 공급체계 마련복지부는 필수약 수급 안정화를 위해 약가제도를 연계한다.장기간 개선 없이 운영된 퇴장방지약은 안정적으로 공급될 수 있게 지정기준을 상향하고 원가보전 기준 현실화 등 방안을 내년 하반기부터 시행한다.국가필수약 대상 약가 정책이 공급을 유도할 수 있도록 수급 친화적으로 개선한다. 적용 대상을 확대하고 우대기간을 안정적으로 보장하는 정책을 내년 1분기부터 신속 시행한다.또 민관 협력 대응체계를 기반으로 수급불안정 약제는 선제적으로 모니터링하고 원인별 맞춤 조치를 실시한다.사후관리제도 정비복지부는 기존 사후관리제도를 약가 조정 예측 가능성과 제도 운영 실효성을 높이는 방향으로 정비한다.사용범위 확대 약가인하와 사용량-약가 연동 약가인하 시기를 일치시키는 동시에 정례화한다.실거래가 조사 약가인하는 시장경쟁과 연동시켜 인센티브를 기반으로 실거래가 인하가 촉진되는 방향으로 재편하는 방안을 2027년부터 도입한다.급여적정성 재평가는 선별등재 이후 약제 역시 대상에 포함하되 임상 유용성 재검토 필요성이 확인된 약제 중심으로 평가한다.종합적 약가 평가·조정 기전을 내년안에 마련해 2027년부터 3~5년주기로 적용한다. 약가 운영 예측가능성은 높이고 약제비는 합리적으로 관리하는 체계 구축을 위해서다.약가제도 개편안은 이번 건정심 보고 후 추가 의견 수렴을 거쳐 최종 확정된다.2025-11-28 17:36:57이정환 기자 -
 전자처방부터 조제약 인도까지…약국 뭐가 달라질까[데일리팜=김지은 기자] 수년간 시범사업으로 진행돼 온 비대면진료가 이르면 내년 하반기부터는 제도권 안에 편입될 예정이다.지난 18일 국회 법안 소위를 통과한 비대면진료 제도화를 위한 모법인 의료법 개정안이 내주 본회의 통과를 앞두고 있다.그간 관련 의료법, 약사법 개정에 적극 의견을 개진해 왔던 약사회로서는 이제 제도 시행의 세부 운영 기준이 될 하위법령 등 후속 조치에 총력을 기울일 상황이 됐다.당장 모법에 담긴 의약품 처방과 처방전 인도, 수령 등에 있어 최선의 안전장치를 마련해야 하는 동시에 공적 전자처방 전달 시스템 세팅 등 정부와 적극 협상할 아젠다들이 남아있기 때문이다.◆비대면진료 의료법 개정안, 핵심 내용은=이번 비대면진료 의료법 개정안에는 대면 진료를 원칙으로 한다는 규정이 담겼다.대상환자는 재진환자가 주 대상이며 초진 환자인 경우 지역·처방을 제한하도록 했다. 단, 희귀질환자나 제1형 당뇨병 환자 등은 지역 제한에서 예외다. 여기서 초진 환자의 진료 가능 권역 범위의 경우 하위법령에 위임해 놨는데, 현재로서는 광역 권역으로 설정하는 방안이 논의되고 있는 것으로 알려졌다.처방 제한 규정도 담겼는데 DUR의무화법이 병합 심리돼 마약류 처방 조제 시에는 대면, 비대면 상관 없이 DUR 확인을 의무화한다는 규정이 담겼다. 희귀질환자의 경우는 마약류 등의 처방 제한에서 예외를 두는 조항도 포함됐다.처방 제한 의약품을 습관적으로 또는 무의식적으로 처방해 형사처벌을 받는 것을 방지하기 위해 의료기관 EMR 시스템 상에 처방이 안되도록 장치를 마련, 비의도적인 의료행위에 대해 처벌할 수 없도록 하는 조항도 추가됐다.수행 의료기관의 경우 의원급을 원칙으로 하되 일부 환자군에 한해 병원급을 예외적으로 허용하는 안이 담겼다. 의원의 경우 전담기관을 금지하는 규정이 모법에 담겼으며, 비급여 진료 내역을 복지부장관에게 의무적으로 제출하도록 하는 규정도 포함됐다.중개 플랫폼 규제방안도 모법에 담겼다. 플랫폼은 신고제를 유지하도록 했는데, 중개매체의 기본 요건을 갖추지 않으면 도입할 수 없도록 전제의 신고제를 말한다.가입자 수가 일정 규모 이상인 중개매체의 경우 인증을 의무화하도록 하는 규정도 포함됐다. 이들 중개매체의 개인정보보호 등 중요한 문제들에 대한 조치 규정 마련과 더불어 공공 중개매체에 대한 근거를 마련해 운영할 수 있도록 근거 조항 포함도 주목되는 부분이다.비대면진료 지원 시스템 구축·운영에 대한 근거가 모범에 마련됐으며, 비대면진료 전자처방전 전달시스템 구축, 운영 근거도 이번 개정안에 함께 담겼다. 관계 전문기관 위탁 등이 근거 법률에 직접 규정됨에 따라 약사회는 공공기관인 건강보험공단이나 심사평가원, 복지부 산하 보건의료정보원 등에 관련 운영 근거를 위임할 수 있도록 하는 부분이 이번 의료법 개정안에 담긴 것으로 볼 수 있다고 평가했다.약사사회 최대 쟁점이었던 처방약 인도(수령)의 경우도 이번 의료법 개정안에 포함됐다. 현 시범사업에서 허용 중인 대상자에 한정해 재택수령을 허용했는데 ▲섬·벽지 등 의료접근이 어려운 지역 거주자 ▲65세 이상이면서 장기요양 등급자인 노인 ▲장애인 ▲감염병 확진자 등 격리 또는 접근 제한 상태에 있는 자 ▲희귀질환자 등이 대상이다.다만 재택수령을 원하는 대상자는 복지부령으로 환자가 거주자는 지역 내 약국에서만 약의 인도를 요청할 수 있도록 하는 내용의 지역 제한 규정도 포함됐다.◆하위법령 규정, 약사사회 쟁점은=약사회는 우선 처방 제한 의약품을 현재 시범사업에서 적용 중인 품목보다 확대하는 내용을 세부규정에 담아야 한다는 입장이다.현재 시범사업에서는 ▲마약류 ▲오·남용 우려 의약품(오·남용 우려 의약품 지정에 관한 규정 제2조에 따른 23개 성분) ▲사후 피임약 ▲비만치료제에 한해 처방이 제한돼 있다.약사회는 하위법령에 이들 의약품과 더불어 탈모약, 여드름약 등 비급여 의약품을 추가하는 방안을 현재 복지부와 논의 중이라고 밝혔다.비대면진료 전담약국 제한 장치도 약사회가 주목하고 있는 부분이다. 현재 의료기관의 경우 전담기관 금지 규정이 담겼지만, 약국에 대해서는 별도 규정이 마련돼 있지 않은 만큼, 하위 규정에서 전담약국에 대해서도 제한장치를 마련하겠다는 방침이다.현재 정부는 전담기관 방지를 위한 장치로 비대면진료 비율을 제한하는 방침을 강구 중인 만큼 약국도 유사한 방식으로 갈지, 처방전 수로 따질지 등에 대해 정부와 논의해 갈 예정이다.공적 전자처방전도 약사회가 추후 정부와의 논의를 통해 풀어가야 할 과제다. 의사회의 극려란 반대에도 불구하고 이번 의료법 개정을 통해 비대면진료에 한해서는 공적 전자처방전 도입이 가능하도록 된 상황. 추후 대면진료까지 확대될 수 있다고 가정하면 정부와 약사회 간 논의 결과가 추후 처방전달 시스템 변화의 중심이 될 예정이다.약사회는 현재 복지부에 전자처방전 관련 실무협의체 구성을 제안한 상태이며, 이번 의료법 개정안이 통과되면 관련 논의가 급물살을 탈 것으로 예상했다.이광민 대한약사회 부회장은 “1년 후 시행이 예상되는 상황에서 전자처방 시스템을 제대로 갖추기 까지 시간이 빠듯할 것으로 보인다”며 “현재로서는 수행 기관보다는 어떻게 시스템을 세팅할 지가 관건이라고 본다. 이 부분에 대해 복지부와 심도있게 논의하려고 한다”고 말했다.처방의약품 재택수령의 구체적 방안도 남아있는 과제다. 대상 환자의 경우 모법에서 제한됐지만 추후 재택수령 가능 지역 범위, 전달 방식, 복약지도 방식 등 세부적인 규정 마련이 남아있는 상태다.이 부회장은 “모법에 재택수령 대상자는 복지부령으로 환자가 거주하는 지역 내 약국에서만 약의 인도를 요청할 수 있도록 하는 내용의 지역 제한 규정이 포함됐다”며 “구체적으로 지역 제한을 시군구로 할지, 읍면동으로 할지는 하위법령에 위임돼 있는 만큼 향후 환자군에 따라 복지부와 제한 범위를 협의해 결정할 사안”이라고 했다.이어 “구체적 실행 방안에 해당하는 하위법령이나 고시, 가이드라인에 최대한 안전장치를 담아내는 것이 중요한 과제로 남아있다”면서 “모법 개정에 있어서도 그랬듯이 향후 하위법령 정비 과정에서도 약사 전문성과 현장 경험이 충분히 반영될 수 있도록 모든 협의 절차에 적극 참여하겠다”고 말했다.2025-11-26 06:13:40김지은
전자처방부터 조제약 인도까지…약국 뭐가 달라질까[데일리팜=김지은 기자] 수년간 시범사업으로 진행돼 온 비대면진료가 이르면 내년 하반기부터는 제도권 안에 편입될 예정이다.지난 18일 국회 법안 소위를 통과한 비대면진료 제도화를 위한 모법인 의료법 개정안이 내주 본회의 통과를 앞두고 있다.그간 관련 의료법, 약사법 개정에 적극 의견을 개진해 왔던 약사회로서는 이제 제도 시행의 세부 운영 기준이 될 하위법령 등 후속 조치에 총력을 기울일 상황이 됐다.당장 모법에 담긴 의약품 처방과 처방전 인도, 수령 등에 있어 최선의 안전장치를 마련해야 하는 동시에 공적 전자처방 전달 시스템 세팅 등 정부와 적극 협상할 아젠다들이 남아있기 때문이다.◆비대면진료 의료법 개정안, 핵심 내용은=이번 비대면진료 의료법 개정안에는 대면 진료를 원칙으로 한다는 규정이 담겼다.대상환자는 재진환자가 주 대상이며 초진 환자인 경우 지역·처방을 제한하도록 했다. 단, 희귀질환자나 제1형 당뇨병 환자 등은 지역 제한에서 예외다. 여기서 초진 환자의 진료 가능 권역 범위의 경우 하위법령에 위임해 놨는데, 현재로서는 광역 권역으로 설정하는 방안이 논의되고 있는 것으로 알려졌다.처방 제한 규정도 담겼는데 DUR의무화법이 병합 심리돼 마약류 처방 조제 시에는 대면, 비대면 상관 없이 DUR 확인을 의무화한다는 규정이 담겼다. 희귀질환자의 경우는 마약류 등의 처방 제한에서 예외를 두는 조항도 포함됐다.처방 제한 의약품을 습관적으로 또는 무의식적으로 처방해 형사처벌을 받는 것을 방지하기 위해 의료기관 EMR 시스템 상에 처방이 안되도록 장치를 마련, 비의도적인 의료행위에 대해 처벌할 수 없도록 하는 조항도 추가됐다.수행 의료기관의 경우 의원급을 원칙으로 하되 일부 환자군에 한해 병원급을 예외적으로 허용하는 안이 담겼다. 의원의 경우 전담기관을 금지하는 규정이 모법에 담겼으며, 비급여 진료 내역을 복지부장관에게 의무적으로 제출하도록 하는 규정도 포함됐다.중개 플랫폼 규제방안도 모법에 담겼다. 플랫폼은 신고제를 유지하도록 했는데, 중개매체의 기본 요건을 갖추지 않으면 도입할 수 없도록 전제의 신고제를 말한다.가입자 수가 일정 규모 이상인 중개매체의 경우 인증을 의무화하도록 하는 규정도 포함됐다. 이들 중개매체의 개인정보보호 등 중요한 문제들에 대한 조치 규정 마련과 더불어 공공 중개매체에 대한 근거를 마련해 운영할 수 있도록 근거 조항 포함도 주목되는 부분이다.비대면진료 지원 시스템 구축·운영에 대한 근거가 모범에 마련됐으며, 비대면진료 전자처방전 전달시스템 구축, 운영 근거도 이번 개정안에 함께 담겼다. 관계 전문기관 위탁 등이 근거 법률에 직접 규정됨에 따라 약사회는 공공기관인 건강보험공단이나 심사평가원, 복지부 산하 보건의료정보원 등에 관련 운영 근거를 위임할 수 있도록 하는 부분이 이번 의료법 개정안에 담긴 것으로 볼 수 있다고 평가했다.약사사회 최대 쟁점이었던 처방약 인도(수령)의 경우도 이번 의료법 개정안에 포함됐다. 현 시범사업에서 허용 중인 대상자에 한정해 재택수령을 허용했는데 ▲섬·벽지 등 의료접근이 어려운 지역 거주자 ▲65세 이상이면서 장기요양 등급자인 노인 ▲장애인 ▲감염병 확진자 등 격리 또는 접근 제한 상태에 있는 자 ▲희귀질환자 등이 대상이다.다만 재택수령을 원하는 대상자는 복지부령으로 환자가 거주자는 지역 내 약국에서만 약의 인도를 요청할 수 있도록 하는 내용의 지역 제한 규정도 포함됐다.◆하위법령 규정, 약사사회 쟁점은=약사회는 우선 처방 제한 의약품을 현재 시범사업에서 적용 중인 품목보다 확대하는 내용을 세부규정에 담아야 한다는 입장이다.현재 시범사업에서는 ▲마약류 ▲오·남용 우려 의약품(오·남용 우려 의약품 지정에 관한 규정 제2조에 따른 23개 성분) ▲사후 피임약 ▲비만치료제에 한해 처방이 제한돼 있다.약사회는 하위법령에 이들 의약품과 더불어 탈모약, 여드름약 등 비급여 의약품을 추가하는 방안을 현재 복지부와 논의 중이라고 밝혔다.비대면진료 전담약국 제한 장치도 약사회가 주목하고 있는 부분이다. 현재 의료기관의 경우 전담기관 금지 규정이 담겼지만, 약국에 대해서는 별도 규정이 마련돼 있지 않은 만큼, 하위 규정에서 전담약국에 대해서도 제한장치를 마련하겠다는 방침이다.현재 정부는 전담기관 방지를 위한 장치로 비대면진료 비율을 제한하는 방침을 강구 중인 만큼 약국도 유사한 방식으로 갈지, 처방전 수로 따질지 등에 대해 정부와 논의해 갈 예정이다.공적 전자처방전도 약사회가 추후 정부와의 논의를 통해 풀어가야 할 과제다. 의사회의 극려란 반대에도 불구하고 이번 의료법 개정을 통해 비대면진료에 한해서는 공적 전자처방전 도입이 가능하도록 된 상황. 추후 대면진료까지 확대될 수 있다고 가정하면 정부와 약사회 간 논의 결과가 추후 처방전달 시스템 변화의 중심이 될 예정이다.약사회는 현재 복지부에 전자처방전 관련 실무협의체 구성을 제안한 상태이며, 이번 의료법 개정안이 통과되면 관련 논의가 급물살을 탈 것으로 예상했다.이광민 대한약사회 부회장은 “1년 후 시행이 예상되는 상황에서 전자처방 시스템을 제대로 갖추기 까지 시간이 빠듯할 것으로 보인다”며 “현재로서는 수행 기관보다는 어떻게 시스템을 세팅할 지가 관건이라고 본다. 이 부분에 대해 복지부와 심도있게 논의하려고 한다”고 말했다.처방의약품 재택수령의 구체적 방안도 남아있는 과제다. 대상 환자의 경우 모법에서 제한됐지만 추후 재택수령 가능 지역 범위, 전달 방식, 복약지도 방식 등 세부적인 규정 마련이 남아있는 상태다.이 부회장은 “모법에 재택수령 대상자는 복지부령으로 환자가 거주하는 지역 내 약국에서만 약의 인도를 요청할 수 있도록 하는 내용의 지역 제한 규정이 포함됐다”며 “구체적으로 지역 제한을 시군구로 할지, 읍면동으로 할지는 하위법령에 위임돼 있는 만큼 향후 환자군에 따라 복지부와 제한 범위를 협의해 결정할 사안”이라고 했다.이어 “구체적 실행 방안에 해당하는 하위법령이나 고시, 가이드라인에 최대한 안전장치를 담아내는 것이 중요한 과제로 남아있다”면서 “모법 개정에 있어서도 그랬듯이 향후 하위법령 정비 과정에서도 약사 전문성과 현장 경험이 충분히 반영될 수 있도록 모든 협의 절차에 적극 참여하겠다”고 말했다.2025-11-26 06:13:40김지은 -
 제약바이오 미국 수출 껑충…삼바 2배·셀트리온 3배↑[데일리팜=김진구 기자] 주요 상장 제약바이오기업 20곳 중 18곳의 3분기 누적 수출실적이 전년대비 증가한 것으로 나타났다.특히 미국으로의 수출실적이 큰 폭으로 늘었다. 삼성바이오로직스는 1년 새 미국으로의 수출실적이 2배 이상, 셀트리온은 3배 이상 각각 증가했다. 미국 정부의 관세 부과 우려에 대비해 현지에 재고를 확보해두려는 움직임이 두드러졌기 때문이라는 분석이다.제약업계에선 최대 변수였던 미국과의 관세 협상의 최종 타결로 불확실성이 해소됨에 따라, 주요 제약바이오기업들의 의약품 수출 호조가 지속될 것이란 전망이 나온다.제약 20곳 중 18곳, 3분기 누적 수출실적 증가24일 금융감독원에 따르면 지난 3분기 누적 주요 제약바이오기업 20곳 중 18곳의 수출실적이 전년동기 대비 증가했다.유가증권시장(코스피)과 코스닥시장 상장 제약바이오기업 중 3분기 누적 수출실적이 300억원 이상인 20곳을 대상으로 집계한 결과다. 지주사는 집계에서 제외했다. SK바이오팜·녹십자·SK바이오사이언스·유한양행·에스티팜·파마리서치·HK이노엔·경보제약의 수출실적이 1년 새 30% 이상 증가했다. 삼성바이오로직스·셀트리온·대웅제약·휴온스는 20% 이상 늘었고, 휴젤·동아에스티·메디톡스·동화약품·일양약품도 각각 전년대비 증가한 것으로 나타났다. 한미약품은 전년대비 소폭 늘었고, 종근당바이오와 동국제약은 감소했다.이들의 합산 수출실적은 작년 3분기 누적 6조7119억원에서 올해 3분기 누적 9조354억원으로 35% 증가했다.관세 불안에 미국 수출 급증…삼바 2.1배·셀트리온 3.4배 쑥주요 기업의 미국 수출실적이 큰 폭으로 증가하면서 전반적인 수출 호조에 기여했다.삼성바이오로직스는 미국으로의 수출실적이 1년 새 7881억원에서 1조6482억원으로 109% 증가했다. 전체 수출실적에서 미국이 차지하는 비중은 작년 3분기 24%에서 올해 3분기 39%로 1년 새 15%포인트 확대됐다.미국 수출이 크게 늘면서 삼성바이오로직스의 전체 수출실적은 3조1824억원에서 4조1167억원으로 29% 증가했다. 미국 외에 유럽으로의 수출실적이 2조1726억원에서 2조2409억원으로 3% 늘었고, 기타 국가로의 수출은 2217억원에서 2276억원으로 소폭 증가했다.셀트리온은 미국 수출실적이 3배 이상 급증했다. 작년 3분기 누적 778억원에 그쳤으나 1년 만에 2650억원으로 치솟았다. 3분기 누적 수출실적만으로 이미 지난해 전체 미국 수출액 1조681억원을 크게 넘어섰다.미국 외 지역으로의 수출도 호조를 보였다. 유럽으로의 수출은 1조856억원에서 1조2904억원으로 19%, 아시아 수출은 1356억원에서 1753억원으로 29% 증가했다. 이를 포함해 전체 수출실적은 2조4937억원에서 2조8323억원으로 14% 늘었다.SK바이오팜은 미국 수출실적이 1년 새 3094억원에서 4718억원으로 53% 증가했다. 뇌전증 치료제 ‘엑스코프리(세노바메이트)’의 미국시장 판매 호조가 실적 확대에 긍정적으로 작용했다. SK바이오팜은 지난 2020년 5월 엑스코프리를 현지 발매했다. 이후 꾸준히 현지 매출이 증가하고 있다. 미국을 포함한 전체 수출실적은 3786억원에서 5123억원으로 35% 늘었다. 전체 수출실적에서 미국이 차지하는 비중은 82%에서 92%로 확대됐다.GC녹십자는 GC녹십자는 ‘알리글로’를 중심으로 한 혈액제제의 수출실적이 1년 새 1030억원에서 3036억원으로 3배 가까이 늘었다. 특히 미국으로의 알리글로 수출이 크게 늘었다는 분석이다. 미국에서 알리글로의 판매를 담당하는 GC바이오파마 USA(GC BIOPHARMA USA)는 올해 3분기 누적 790억원의 매출이 신규로 발생했다. 주요 기업들의 미국 수출실적 증가는 트럼프 정부의 의약품 관세 부과 우려에 적극 대응한 결과라는 분석이다. 이들은 관세 부과 우려에 대비해 현지에 재고를 비축해두는 방식으로 대응한 바 있다.제약업계에선 최대 변수였던 미국과의 의약품 관세 협상이 최근 타결됨에 따라 미국을 중심으로 한 의약품 수출 호조세가 이어질 것이란 전망이 나온다.한미 양국은 지난달 29일 경주 아시아태평양경제협력체(APEC) 정상회의에서 의약품 분야 최대국대우(MFN) 적용에 합의했다. 미국에서 국산 의약품이 일본·EU와 같이 최혜국대우를 적용받아, 최대 15%의 관세율이 부과되는 내용이 골자다.지난 14일엔 관세 후속 협상 타결에 따른 합의 세부 내용을 공개했다. 미국 백악관은 한국산 의약품에 대한 관세가 최대 15%를 넘지 않도록 합의했다는 내용을 담은 한·미 정상회담 조인트 팩트시트(JFS)를 발표했다. 의약품에 부과되는 어떠한 관세의 경우도 15%의 관세율을 초과하지 않기로 확정했다. 제네릭에 대해선 무관세를 적용키로 했다.다만 여전히 관세 변수가 남아있다는 게 업계 평가다. 이번 팩트시트에는 바이오시밀러의 관세 범위가 정확히 명시되지 않았다. 바이오시밀러가 제네릭 범주로 포함돼 무관세를 적용받을지, 별도 판단을 받을지 확정되지 않았다.SK바사·파마리서치·HK이노엔·에스티팜 수출 호조 지속이밖에 SK바이오사이언스와 파마리서치, HK이노엔, 에스티팜의 수출실적 증가가 두드러졌다.SK바이오사이언스의 3분기 누적 수출액은 3706억원으로 전년동기 190억원 대비 약 20배 증가했다. 지난해 인수한 독일 CDMO 기업 IDT 바이오로지카의 실적이 수출실적으로 반영된 결과로 풀이된다.SK바이오사이언스는 지난해 10월 독일 IDT 바이오로지카를 3564억원에 인수한 바 있다. 이어 작년 4분기부터 IDT 바이오로지카의 실적이 본격 반영됐다. 이 회사의 수출실적은 작년 1~3분기 70억원 미만이었으나, 4분기 1170억원으로 급등했다. 올해 들어선 1분기 1297억원, 2분기 1393억원. 3분기 1017억원 등을 기록했다.파마리서치의 수출실적은 897억원에서 1477억원으로 65% 증가했다. ‘리쥬란’을 중심으로 한 의료기기 수출이 365억원에서 650억원으로 78% 늘었고, 화장품 부문 수출은 319억원에서 587억원으로 84% 증가했다.HK이노엔의 경우 위식도역류질환 치료제 ‘케이캡’을 중심으로 수출실적이 307억원에서 446억원으로 45% 증가했다. 이 기간 케이캡의 수출액은 43억원에서 76억원으로 1년 새 77% 증가했다.대웅제약의 수출은 1415억원에서 1737억원으로 23% 증가했다. 보툴리눔톡신 제제 ‘나보타’의 수출이 1157억원에서 1452억원으로 25%, 위식도역류질환 치료제 ‘펙수클루’의 수출이 27억원에서 36억원으로 34% 각각 늘었다.에스티팜은 1433억원이던 수출실적이 1942억원으로 36% 늘었다. 회사의 새 주력 사업으로 떠오른 올리고유클레오타이드 원료를 중심으로 한 신약 API 부문의 수출실적이 995억원으로 1288억원으로 29% 증가했다.2025-11-24 06:20:08김진구
제약바이오 미국 수출 껑충…삼바 2배·셀트리온 3배↑[데일리팜=김진구 기자] 주요 상장 제약바이오기업 20곳 중 18곳의 3분기 누적 수출실적이 전년대비 증가한 것으로 나타났다.특히 미국으로의 수출실적이 큰 폭으로 늘었다. 삼성바이오로직스는 1년 새 미국으로의 수출실적이 2배 이상, 셀트리온은 3배 이상 각각 증가했다. 미국 정부의 관세 부과 우려에 대비해 현지에 재고를 확보해두려는 움직임이 두드러졌기 때문이라는 분석이다.제약업계에선 최대 변수였던 미국과의 관세 협상의 최종 타결로 불확실성이 해소됨에 따라, 주요 제약바이오기업들의 의약품 수출 호조가 지속될 것이란 전망이 나온다.제약 20곳 중 18곳, 3분기 누적 수출실적 증가24일 금융감독원에 따르면 지난 3분기 누적 주요 제약바이오기업 20곳 중 18곳의 수출실적이 전년동기 대비 증가했다.유가증권시장(코스피)과 코스닥시장 상장 제약바이오기업 중 3분기 누적 수출실적이 300억원 이상인 20곳을 대상으로 집계한 결과다. 지주사는 집계에서 제외했다. SK바이오팜·녹십자·SK바이오사이언스·유한양행·에스티팜·파마리서치·HK이노엔·경보제약의 수출실적이 1년 새 30% 이상 증가했다. 삼성바이오로직스·셀트리온·대웅제약·휴온스는 20% 이상 늘었고, 휴젤·동아에스티·메디톡스·동화약품·일양약품도 각각 전년대비 증가한 것으로 나타났다. 한미약품은 전년대비 소폭 늘었고, 종근당바이오와 동국제약은 감소했다.이들의 합산 수출실적은 작년 3분기 누적 6조7119억원에서 올해 3분기 누적 9조354억원으로 35% 증가했다.관세 불안에 미국 수출 급증…삼바 2.1배·셀트리온 3.4배 쑥주요 기업의 미국 수출실적이 큰 폭으로 증가하면서 전반적인 수출 호조에 기여했다.삼성바이오로직스는 미국으로의 수출실적이 1년 새 7881억원에서 1조6482억원으로 109% 증가했다. 전체 수출실적에서 미국이 차지하는 비중은 작년 3분기 24%에서 올해 3분기 39%로 1년 새 15%포인트 확대됐다.미국 수출이 크게 늘면서 삼성바이오로직스의 전체 수출실적은 3조1824억원에서 4조1167억원으로 29% 증가했다. 미국 외에 유럽으로의 수출실적이 2조1726억원에서 2조2409억원으로 3% 늘었고, 기타 국가로의 수출은 2217억원에서 2276억원으로 소폭 증가했다.셀트리온은 미국 수출실적이 3배 이상 급증했다. 작년 3분기 누적 778억원에 그쳤으나 1년 만에 2650억원으로 치솟았다. 3분기 누적 수출실적만으로 이미 지난해 전체 미국 수출액 1조681억원을 크게 넘어섰다.미국 외 지역으로의 수출도 호조를 보였다. 유럽으로의 수출은 1조856억원에서 1조2904억원으로 19%, 아시아 수출은 1356억원에서 1753억원으로 29% 증가했다. 이를 포함해 전체 수출실적은 2조4937억원에서 2조8323억원으로 14% 늘었다.SK바이오팜은 미국 수출실적이 1년 새 3094억원에서 4718억원으로 53% 증가했다. 뇌전증 치료제 ‘엑스코프리(세노바메이트)’의 미국시장 판매 호조가 실적 확대에 긍정적으로 작용했다. SK바이오팜은 지난 2020년 5월 엑스코프리를 현지 발매했다. 이후 꾸준히 현지 매출이 증가하고 있다. 미국을 포함한 전체 수출실적은 3786억원에서 5123억원으로 35% 늘었다. 전체 수출실적에서 미국이 차지하는 비중은 82%에서 92%로 확대됐다.GC녹십자는 GC녹십자는 ‘알리글로’를 중심으로 한 혈액제제의 수출실적이 1년 새 1030억원에서 3036억원으로 3배 가까이 늘었다. 특히 미국으로의 알리글로 수출이 크게 늘었다는 분석이다. 미국에서 알리글로의 판매를 담당하는 GC바이오파마 USA(GC BIOPHARMA USA)는 올해 3분기 누적 790억원의 매출이 신규로 발생했다. 주요 기업들의 미국 수출실적 증가는 트럼프 정부의 의약품 관세 부과 우려에 적극 대응한 결과라는 분석이다. 이들은 관세 부과 우려에 대비해 현지에 재고를 비축해두는 방식으로 대응한 바 있다.제약업계에선 최대 변수였던 미국과의 의약품 관세 협상이 최근 타결됨에 따라 미국을 중심으로 한 의약품 수출 호조세가 이어질 것이란 전망이 나온다.한미 양국은 지난달 29일 경주 아시아태평양경제협력체(APEC) 정상회의에서 의약품 분야 최대국대우(MFN) 적용에 합의했다. 미국에서 국산 의약품이 일본·EU와 같이 최혜국대우를 적용받아, 최대 15%의 관세율이 부과되는 내용이 골자다.지난 14일엔 관세 후속 협상 타결에 따른 합의 세부 내용을 공개했다. 미국 백악관은 한국산 의약품에 대한 관세가 최대 15%를 넘지 않도록 합의했다는 내용을 담은 한·미 정상회담 조인트 팩트시트(JFS)를 발표했다. 의약품에 부과되는 어떠한 관세의 경우도 15%의 관세율을 초과하지 않기로 확정했다. 제네릭에 대해선 무관세를 적용키로 했다.다만 여전히 관세 변수가 남아있다는 게 업계 평가다. 이번 팩트시트에는 바이오시밀러의 관세 범위가 정확히 명시되지 않았다. 바이오시밀러가 제네릭 범주로 포함돼 무관세를 적용받을지, 별도 판단을 받을지 확정되지 않았다.SK바사·파마리서치·HK이노엔·에스티팜 수출 호조 지속이밖에 SK바이오사이언스와 파마리서치, HK이노엔, 에스티팜의 수출실적 증가가 두드러졌다.SK바이오사이언스의 3분기 누적 수출액은 3706억원으로 전년동기 190억원 대비 약 20배 증가했다. 지난해 인수한 독일 CDMO 기업 IDT 바이오로지카의 실적이 수출실적으로 반영된 결과로 풀이된다.SK바이오사이언스는 지난해 10월 독일 IDT 바이오로지카를 3564억원에 인수한 바 있다. 이어 작년 4분기부터 IDT 바이오로지카의 실적이 본격 반영됐다. 이 회사의 수출실적은 작년 1~3분기 70억원 미만이었으나, 4분기 1170억원으로 급등했다. 올해 들어선 1분기 1297억원, 2분기 1393억원. 3분기 1017억원 등을 기록했다.파마리서치의 수출실적은 897억원에서 1477억원으로 65% 증가했다. ‘리쥬란’을 중심으로 한 의료기기 수출이 365억원에서 650억원으로 78% 늘었고, 화장품 부문 수출은 319억원에서 587억원으로 84% 증가했다.HK이노엔의 경우 위식도역류질환 치료제 ‘케이캡’을 중심으로 수출실적이 307억원에서 446억원으로 45% 증가했다. 이 기간 케이캡의 수출액은 43억원에서 76억원으로 1년 새 77% 증가했다.대웅제약의 수출은 1415억원에서 1737억원으로 23% 증가했다. 보툴리눔톡신 제제 ‘나보타’의 수출이 1157억원에서 1452억원으로 25%, 위식도역류질환 치료제 ‘펙수클루’의 수출이 27억원에서 36억원으로 34% 각각 늘었다.에스티팜은 1433억원이던 수출실적이 1942억원으로 36% 늘었다. 회사의 새 주력 사업으로 떠오른 올리고유클레오타이드 원료를 중심으로 한 신약 API 부문의 수출실적이 995억원으로 1288억원으로 29% 증가했다.2025-11-24 06:20:08김진구 -
 '코센틱스', 재수 1년만에 화농성한선염 급여 성공[데일리팜=어윤호 기자] '휴미라' 이후 10년 만에 등장한 화농성한선염 치료옵션 '코센틱스'가 재도전 1년 만에 급여 확대에 성공했다.보건복지부는 최근 '요양급여의 적용기준 및 방법에 관한 세부사항' 일부 개정안을 통해 한국노바티스의 인터루킨(IL)-17A억제제 코센틱스(세쿠키누맙)의 화농성한선염(HS, Hidradenitis suppurativa) 급여 기준을 내달(12월)부터 확대한다고 밝혔다.구체적인 급여 기준은 ▲진단 후 1년 이상 경과한 성인 ▲2개 이상의 각기 다른 부위에 병변이 있고, 농양과 염증성 결절수의 합이 3개 이상인 경우 ▲3개월 이상의 항생제 치료에도 치료 효과가 미흡하거나 부작용이 있는 경우이다.코센틱스의 급여 확대 과정은 순탄치 않았다. 노바티스는 본래 2023년 코센틱스의 화농성한선염 적응증 확대 후 급여 신청을 제출했지만 별다른 진전이 없자 자진취하했다.이후 2024년 유럽피부과학회 연례학술대회(EADV 2024)에서 발표된 유럽화농성한선염재단(EHSF) 가이드라인에서 중등도~중증 화농성 한선염 환자 및 기존 전신 치료에 반응이 불충분한 환자의 1차 생물학적 제제 치료옵션으로 코센틱스가 권고되면서 같은해 11월 다시 급여 확대 신청을 제출했으며 재신청 1년 만에 성과를 냈다.지금까지 화농성한선염 영역에서는 한국애브비의 휴미라(아달리무맙)이 사실상 유일한 치료옵션이었다.이같은 상황에서 작용기전이 다른 IL제제이며 1차치료제로 권고된 코센틱스는 화농성한선염 관리에서 충분히 유용한 옵션이 될 수 있다.한편 코센틱스는 중등도~중증 화농성 한선염 환자 1084명을 대상으로 진행한 임상3상 SUNNY 연구(SUNSHINE, SUNRISE)를 통해 임상적 유용성을 입증했다.연구 결과, 치료 16주차 시점에 약물을 2주마다 투여할 때 코센틱스 투여군의 HiSCR 달성률은 SUNSHINE 연구에서 45%, SUNRISE 연구에서 42%로 나타나 위약군 각각 34%, 31% 대비 유의미한 증상 개선을 확인했다.SUNRISE 연구에서 약물을 4주마다 투여했을 때도 코센틱스의 HiSCR 달성률은 46%로, 위약군 31% 대비 치료 효과가 유의하게 높았으며 코센틱스의 HiSCR 달성률은 치료 52주차까지 꾸준하게 개선됐다.코센틱스는 환자의 통증 개선에도 유의한 효과를 보였다. SUNNY 연구 결과, 치료 16주차 시점에 NRS30 달성률은 코센틱스를 2주마다 투여한 군에서는 39%, 4주마다 투여한 군에서는 36%로 집계됐다. 반면 위약군은 27%에 불과했다. 또 치료 52주차까지 코센틱스 2주마다 투여군의 79.6%, 4주마다 투여군의 72.7%는 질환 악화를 경험하지 않은 것으로 나타났다.2025-11-21 06:00:01어윤호
'코센틱스', 재수 1년만에 화농성한선염 급여 성공[데일리팜=어윤호 기자] '휴미라' 이후 10년 만에 등장한 화농성한선염 치료옵션 '코센틱스'가 재도전 1년 만에 급여 확대에 성공했다.보건복지부는 최근 '요양급여의 적용기준 및 방법에 관한 세부사항' 일부 개정안을 통해 한국노바티스의 인터루킨(IL)-17A억제제 코센틱스(세쿠키누맙)의 화농성한선염(HS, Hidradenitis suppurativa) 급여 기준을 내달(12월)부터 확대한다고 밝혔다.구체적인 급여 기준은 ▲진단 후 1년 이상 경과한 성인 ▲2개 이상의 각기 다른 부위에 병변이 있고, 농양과 염증성 결절수의 합이 3개 이상인 경우 ▲3개월 이상의 항생제 치료에도 치료 효과가 미흡하거나 부작용이 있는 경우이다.코센틱스의 급여 확대 과정은 순탄치 않았다. 노바티스는 본래 2023년 코센틱스의 화농성한선염 적응증 확대 후 급여 신청을 제출했지만 별다른 진전이 없자 자진취하했다.이후 2024년 유럽피부과학회 연례학술대회(EADV 2024)에서 발표된 유럽화농성한선염재단(EHSF) 가이드라인에서 중등도~중증 화농성 한선염 환자 및 기존 전신 치료에 반응이 불충분한 환자의 1차 생물학적 제제 치료옵션으로 코센틱스가 권고되면서 같은해 11월 다시 급여 확대 신청을 제출했으며 재신청 1년 만에 성과를 냈다.지금까지 화농성한선염 영역에서는 한국애브비의 휴미라(아달리무맙)이 사실상 유일한 치료옵션이었다.이같은 상황에서 작용기전이 다른 IL제제이며 1차치료제로 권고된 코센틱스는 화농성한선염 관리에서 충분히 유용한 옵션이 될 수 있다.한편 코센틱스는 중등도~중증 화농성 한선염 환자 1084명을 대상으로 진행한 임상3상 SUNNY 연구(SUNSHINE, SUNRISE)를 통해 임상적 유용성을 입증했다.연구 결과, 치료 16주차 시점에 약물을 2주마다 투여할 때 코센틱스 투여군의 HiSCR 달성률은 SUNSHINE 연구에서 45%, SUNRISE 연구에서 42%로 나타나 위약군 각각 34%, 31% 대비 유의미한 증상 개선을 확인했다.SUNRISE 연구에서 약물을 4주마다 투여했을 때도 코센틱스의 HiSCR 달성률은 46%로, 위약군 31% 대비 치료 효과가 유의하게 높았으며 코센틱스의 HiSCR 달성률은 치료 52주차까지 꾸준하게 개선됐다.코센틱스는 환자의 통증 개선에도 유의한 효과를 보였다. SUNNY 연구 결과, 치료 16주차 시점에 NRS30 달성률은 코센틱스를 2주마다 투여한 군에서는 39%, 4주마다 투여한 군에서는 36%로 집계됐다. 반면 위약군은 27%에 불과했다. 또 치료 52주차까지 코센틱스 2주마다 투여군의 79.6%, 4주마다 투여군의 72.7%는 질환 악화를 경험하지 않은 것으로 나타났다.2025-11-21 06:00:01어윤호 -
 비대면진료·공적처방전·플랫폼 도매금지법, 복지위 통과[데일리팜=이정환 기자] 비대면진료를 정식 제도화하고 비대면진료 때 공적 전자처방전 사용을 의무화하는 의료법 개정안이 20일 오전 국회 보건복지위원회를 통과했다.마약류 향정신성의약품에 대한 의사, 약사의 DUR(의약품안전사용서비스) 확인 의무를 부과하고 이를 위반하면 처벌하는 조항과 의·약사는 물론 비대면진료 중개 플랫폼에게도 불법 리베이트 쌍벌제를 적용하는 조항도 포함됐다.이와 함께 비대면진료 중개 플랫폼이 의약품 도매상을 설립해 직접 의약품 공급·유통하지 못하게 금지하는 내용의 약사법 개정안도 복지위 문턱을 넘었다.김윤 더불어민주당 의원은 해당 법안을 '닥터나우 비진약품 설립·운영 금지법'으로 규정하고 플랫폼이 편법·불법으로 의약품 유통에 개입하는 등 신종 리베이트를 차단하겠다는 의지다.플랫폼을 의약품 유통업 결격사유로 규정하지 않으면 자칫 비대면진료가 특정 의약품을 처방하도록 유도하는 리베이트 창구로 악용될 수 있다는 게 김 의원 문제의식이다.복지위 통과 법안들은 법제사법위원회 체계·자구 심사를 거쳐 본회의를 통과한 뒤 정부 이송·공포되면 최종 입법에 성공한다.비대면진료 제도화 법안과 플랫폼의 도매상 설립·운영 금지 법안의 시행 시점은 '정부 공포 후 1년 뒤'다.만약 이번 달 법안이 국회 본회의를 통과하고 국무회의 의결 절차를 거쳐 공포될 경우를 가정하면 빠르면 내년 11월부터 비대면진료가 정식 제도화되고 플랫폼의 의약품 유통업이 본격적으로 금지된다.비대면진료 정의·원칙·방식, 의료법에 명시복지위 통과 법안은 의사, 의료진 간 원격으로 환자 진료에 협력하는 행위를 '원격의료'에서 '비대면협진'으로 용어를 수정·변경했다.(제34조)의사와 환자 간 대면하지 않고 진료하는 행위를 '비대면진료'로 규정(제34조의2)하고 1항에서 의사는 환자를 대면해 진료하는 것을 원칙으로 정했다.2항은 대면진료 원칙에도 불구하고 비대면진료를 허용하는 대상을 규정했다.환자가 해당 의료기관에서 일정 기간 내 동일 증상으로 대면진료를 받은 기록이 있는 경우 즉, 재진환자는 마약류 향정신성 의약품 처방 금지를 제외하면 별다른 규제없이 전국 단위 비대면진료를 받을 수 있다.초진의 경우 환자 거주지와 의료기관 소재지가 동일 지역에 위치해야 비대면진료가 가능하다. 환자 집 근처에서만 초진 비대면진료를 신청할 수 있게 지역을 규제하는 조항이다.특히 초진 비대면진료 때 의사는 의약품 종류, 처방일 수 등이 제한된 범위에서만 약을 처방할 수 있다. 초진 비대면진료 신청 환자 지역과 제한된 의약품 처방일 수 범위 등은 복지부령으로 정하도록 했다.비대면진료는 의원급 의료기관에서만 실시하되, 희귀질환자, 1형 당뇨환자, 교정시설 수용자, 수술 후 경과 관찰이 필요한 환자 등 불가피한 경우 병원급에서도 실시할 수 있다.희귀질환자, 제1형 당뇨병 환자 등 환자 집 근처가 아닌 전국 단위에서 비대면진료를 받을 필요성이 인정되는 경우엔 초진 비대면진료를 허용했다.비대면진료 실시 의료인은 처방전을 작성해 환자가 지정한 약국에 발송할 수 있다.의료기관 장(의사)은 전체 진료 건수 대비 비대면진료 건수가 일정 비율을 초과해선 안 된다. 비대면진료 전문 의료기관 금지 조항이다.법안은 의사가 비대면진료 때 마약, 향정신성약, 오·남용 우려 의약품 등을 처방하지 못하도록 했다. 단, 희귀질환자에게 필요한 마약류 등 불가피한 경우엔 비대면진료 때도 처방이 가능하다.의사·치과의사는 대면·비대면진료 때 모두 향정신성의약품을 처방하거나 직접 조제하는 경우 환자에게 처방·투여되고 있는 마약 또는 향정신성의약품 등 정보를 DUR을 통해 미리 확인해야 한다.약국 외 의약품 인도·공공 플랫폼·공적처방전 법제화약사(약국개설자)는 의사가 발급한 비대면진료 환자 처방전에 따라 약을 조제할 때 '복지부가 정한 지역 안'에서 약국 외 장소로 처방약을 인도할 수 있다.섬·벽지 거주자, 장기요양급여 수급자, 장애인, 1급·2급 감염병 환자, 희귀질환자가 비대면진료 처방약 약국 외 장소 인도 가능 대상이다.현행 시범사업이 허용하는 수준의 재택수령 대상을 준용하고, 지역 규제를 적용해 안전성을 확보한 셈이다. 비대면진료지원시스템과 전자처방전전달시스템도 법제화됐다. 복지부 장관은 안전하고 효율적인 비대면진료를 위해 비대면진료지원시스템을 구축·운영할 수 있다.공공 플랫폼 조항으로, 민간 플랫폼 일탈행위 관리·감독·제어가 목표다. 다만 공공 플랫폼이 비대면진료 제도화 때 성공할 수 있을지는 불확실하다. 비대면진료 이용 환자들의 선택을 받을 수 있을지 예단이 어렵기 때문이다.복지부 장관은 비대면진료 때 전자처방전전달시스템을 구축·운영할 수 있다. 공적전자처방전 조항으로, 대면진료 땐 적용되지 않는다. 의료계 요구 사항을 일부 수용한 결과다.비대면진료 중개 플랫폼·규제 법제화비대면진료 중개매체(이하 플랫폼)를 제공·운영하려는 자는 복지부 장관에게 신고해야 한다. 플랫폼 의무 신고제에 해당한다.플랫폼은 의사의 비대면진료와 의료적 판단에 개입해선 안 되며 의료서비스·의약품 오·남용 조장 행위도 금지된다.플랫폼이 약사법 상 담합 행위를 알선·유인·사주해서도 안 되며 직접 또는 제3자를 통해 의료기관이나 의료인, 약국, 약국 개설자·종사자에게 환자 또는 처방전을 가진 사람을 소개·알선·유인하는 대가로 금전, 물품, 편익, 노무, 향응 그 밖의 경제적 이익을 요구하거나 의료기관으로부터 이를 받는 행위도 금지된다. 플랫폼 리베이트 쌍벌제 규정이다.환자·보호자·처방전 보유자에게 특정 의료기관이나 약국, 의약품·의료기기 등을 추천하거나 선택하도록 유도하는 행위 역시 플랫폼 금지 사항이다.플랫폼은 복지부가 정해 고시한 통계를 분기별로 보고해야 한다.부칙에서는 플랫폼 신고·인증 경과조치를 규정했는데, 비대면진료 법 시행일부터 3개월 이내에 복지부 신고 절차를 완료해야 한다. 가입자 수가 일정 규모 이상인 플랫폼으로 복지부 인증 신청 의무가 있는 경우엔 6개월 이내 신고를 완료하도록 정했다.플랫폼, 의약품 도매상 허가·운영 금지의료법 개정안과 함께 복지위를 통과한 약사법 개정안은 비대면진료 중개 플랫폼을 '한약업사 또는 의약품 도매상 허가 결격사유'에 추가했다. 의약품 판매질서 확립이 목표다.특히 의약품 도매상이 특수한 관계에 있는 비대면진료 중개 플랫폼과 이용계약을 체결한 약국에 직접 또는 다른 의약품 도매상을 통해 약을 판매하지 못하게 막으려는 취지도 있다.김윤 의원은 해당 조항을 통해 닥터나우가 자회사로 비진약품을 허가받아 의약품 유통에 개입하고 이를 토대로 한 비대면진료 중개 서비스를 개발하는 등 행위를 막을 필요성이 크다는 입장이다. 이를 허용하면 플랫폼의 불법 리베이트 가능성을 키우고 편법 경영 위험도 급증한다는 이유에서다.해당 약사법에는 약사의 마약류DUR 확인 의무 조항도 포함됐다. 약사는 마약이나 향정신성약을 조제할 때 DUR에서 환자에게 처방·투여되고 있는 마약 또는 향정약 정보를 확인해야 한다.2025-11-20 10:47:13이정환
비대면진료·공적처방전·플랫폼 도매금지법, 복지위 통과[데일리팜=이정환 기자] 비대면진료를 정식 제도화하고 비대면진료 때 공적 전자처방전 사용을 의무화하는 의료법 개정안이 20일 오전 국회 보건복지위원회를 통과했다.마약류 향정신성의약품에 대한 의사, 약사의 DUR(의약품안전사용서비스) 확인 의무를 부과하고 이를 위반하면 처벌하는 조항과 의·약사는 물론 비대면진료 중개 플랫폼에게도 불법 리베이트 쌍벌제를 적용하는 조항도 포함됐다.이와 함께 비대면진료 중개 플랫폼이 의약품 도매상을 설립해 직접 의약품 공급·유통하지 못하게 금지하는 내용의 약사법 개정안도 복지위 문턱을 넘었다.김윤 더불어민주당 의원은 해당 법안을 '닥터나우 비진약품 설립·운영 금지법'으로 규정하고 플랫폼이 편법·불법으로 의약품 유통에 개입하는 등 신종 리베이트를 차단하겠다는 의지다.플랫폼을 의약품 유통업 결격사유로 규정하지 않으면 자칫 비대면진료가 특정 의약품을 처방하도록 유도하는 리베이트 창구로 악용될 수 있다는 게 김 의원 문제의식이다.복지위 통과 법안들은 법제사법위원회 체계·자구 심사를 거쳐 본회의를 통과한 뒤 정부 이송·공포되면 최종 입법에 성공한다.비대면진료 제도화 법안과 플랫폼의 도매상 설립·운영 금지 법안의 시행 시점은 '정부 공포 후 1년 뒤'다.만약 이번 달 법안이 국회 본회의를 통과하고 국무회의 의결 절차를 거쳐 공포될 경우를 가정하면 빠르면 내년 11월부터 비대면진료가 정식 제도화되고 플랫폼의 의약품 유통업이 본격적으로 금지된다.비대면진료 정의·원칙·방식, 의료법에 명시복지위 통과 법안은 의사, 의료진 간 원격으로 환자 진료에 협력하는 행위를 '원격의료'에서 '비대면협진'으로 용어를 수정·변경했다.(제34조)의사와 환자 간 대면하지 않고 진료하는 행위를 '비대면진료'로 규정(제34조의2)하고 1항에서 의사는 환자를 대면해 진료하는 것을 원칙으로 정했다.2항은 대면진료 원칙에도 불구하고 비대면진료를 허용하는 대상을 규정했다.환자가 해당 의료기관에서 일정 기간 내 동일 증상으로 대면진료를 받은 기록이 있는 경우 즉, 재진환자는 마약류 향정신성 의약품 처방 금지를 제외하면 별다른 규제없이 전국 단위 비대면진료를 받을 수 있다.초진의 경우 환자 거주지와 의료기관 소재지가 동일 지역에 위치해야 비대면진료가 가능하다. 환자 집 근처에서만 초진 비대면진료를 신청할 수 있게 지역을 규제하는 조항이다.특히 초진 비대면진료 때 의사는 의약품 종류, 처방일 수 등이 제한된 범위에서만 약을 처방할 수 있다. 초진 비대면진료 신청 환자 지역과 제한된 의약품 처방일 수 범위 등은 복지부령으로 정하도록 했다.비대면진료는 의원급 의료기관에서만 실시하되, 희귀질환자, 1형 당뇨환자, 교정시설 수용자, 수술 후 경과 관찰이 필요한 환자 등 불가피한 경우 병원급에서도 실시할 수 있다.희귀질환자, 제1형 당뇨병 환자 등 환자 집 근처가 아닌 전국 단위에서 비대면진료를 받을 필요성이 인정되는 경우엔 초진 비대면진료를 허용했다.비대면진료 실시 의료인은 처방전을 작성해 환자가 지정한 약국에 발송할 수 있다.의료기관 장(의사)은 전체 진료 건수 대비 비대면진료 건수가 일정 비율을 초과해선 안 된다. 비대면진료 전문 의료기관 금지 조항이다.법안은 의사가 비대면진료 때 마약, 향정신성약, 오·남용 우려 의약품 등을 처방하지 못하도록 했다. 단, 희귀질환자에게 필요한 마약류 등 불가피한 경우엔 비대면진료 때도 처방이 가능하다.의사·치과의사는 대면·비대면진료 때 모두 향정신성의약품을 처방하거나 직접 조제하는 경우 환자에게 처방·투여되고 있는 마약 또는 향정신성의약품 등 정보를 DUR을 통해 미리 확인해야 한다.약국 외 의약품 인도·공공 플랫폼·공적처방전 법제화약사(약국개설자)는 의사가 발급한 비대면진료 환자 처방전에 따라 약을 조제할 때 '복지부가 정한 지역 안'에서 약국 외 장소로 처방약을 인도할 수 있다.섬·벽지 거주자, 장기요양급여 수급자, 장애인, 1급·2급 감염병 환자, 희귀질환자가 비대면진료 처방약 약국 외 장소 인도 가능 대상이다.현행 시범사업이 허용하는 수준의 재택수령 대상을 준용하고, 지역 규제를 적용해 안전성을 확보한 셈이다. 비대면진료지원시스템과 전자처방전전달시스템도 법제화됐다. 복지부 장관은 안전하고 효율적인 비대면진료를 위해 비대면진료지원시스템을 구축·운영할 수 있다.공공 플랫폼 조항으로, 민간 플랫폼 일탈행위 관리·감독·제어가 목표다. 다만 공공 플랫폼이 비대면진료 제도화 때 성공할 수 있을지는 불확실하다. 비대면진료 이용 환자들의 선택을 받을 수 있을지 예단이 어렵기 때문이다.복지부 장관은 비대면진료 때 전자처방전전달시스템을 구축·운영할 수 있다. 공적전자처방전 조항으로, 대면진료 땐 적용되지 않는다. 의료계 요구 사항을 일부 수용한 결과다.비대면진료 중개 플랫폼·규제 법제화비대면진료 중개매체(이하 플랫폼)를 제공·운영하려는 자는 복지부 장관에게 신고해야 한다. 플랫폼 의무 신고제에 해당한다.플랫폼은 의사의 비대면진료와 의료적 판단에 개입해선 안 되며 의료서비스·의약품 오·남용 조장 행위도 금지된다.플랫폼이 약사법 상 담합 행위를 알선·유인·사주해서도 안 되며 직접 또는 제3자를 통해 의료기관이나 의료인, 약국, 약국 개설자·종사자에게 환자 또는 처방전을 가진 사람을 소개·알선·유인하는 대가로 금전, 물품, 편익, 노무, 향응 그 밖의 경제적 이익을 요구하거나 의료기관으로부터 이를 받는 행위도 금지된다. 플랫폼 리베이트 쌍벌제 규정이다.환자·보호자·처방전 보유자에게 특정 의료기관이나 약국, 의약품·의료기기 등을 추천하거나 선택하도록 유도하는 행위 역시 플랫폼 금지 사항이다.플랫폼은 복지부가 정해 고시한 통계를 분기별로 보고해야 한다.부칙에서는 플랫폼 신고·인증 경과조치를 규정했는데, 비대면진료 법 시행일부터 3개월 이내에 복지부 신고 절차를 완료해야 한다. 가입자 수가 일정 규모 이상인 플랫폼으로 복지부 인증 신청 의무가 있는 경우엔 6개월 이내 신고를 완료하도록 정했다.플랫폼, 의약품 도매상 허가·운영 금지의료법 개정안과 함께 복지위를 통과한 약사법 개정안은 비대면진료 중개 플랫폼을 '한약업사 또는 의약품 도매상 허가 결격사유'에 추가했다. 의약품 판매질서 확립이 목표다.특히 의약품 도매상이 특수한 관계에 있는 비대면진료 중개 플랫폼과 이용계약을 체결한 약국에 직접 또는 다른 의약품 도매상을 통해 약을 판매하지 못하게 막으려는 취지도 있다.김윤 의원은 해당 조항을 통해 닥터나우가 자회사로 비진약품을 허가받아 의약품 유통에 개입하고 이를 토대로 한 비대면진료 중개 서비스를 개발하는 등 행위를 막을 필요성이 크다는 입장이다. 이를 허용하면 플랫폼의 불법 리베이트 가능성을 키우고 편법 경영 위험도 급증한다는 이유에서다.해당 약사법에는 약사의 마약류DUR 확인 의무 조항도 포함됐다. 약사는 마약이나 향정신성약을 조제할 때 DUR에서 환자에게 처방·투여되고 있는 마약 또는 향정약 정보를 확인해야 한다.2025-11-20 10:47:13이정환 -
 HK이노엔 케이캡, 세계일류상품 선정…의약품 중 유일세계일류상품 인증서 수여식에서 산업통상부 최연우 중견기업정책관(사진 왼쪽)과 HK이노엔 R&D전략실 박현정 상무(사진 오른쪽)가 기념사진을 찍고 있다. [데일리팜=황병우 기자] HK이노엔은 위식도역류질환 신약 케이캡(성분명 테고프라잔)이 산업통상자원부와 KOTRA가 주관하는 세계일류상품 육성사업에서 '현재 세계일류상품'으로 선정됐다고 19일 밝혔다.올해 선정된 97개의 '현재 세계일류상품' 중 의약품으로는 케이캡이 유일하다.‘세계일류상품 육성사업’은 국내 우수 상품의 글로벌 시장 진출 확대와 수출 경쟁력 강화를 위해 2001년부터 산업통상자원부와 KOTRA가 운영 중인 인증사업이다.세계시장점유율 5% 이상, 세계 5위 이내이며 연간 수출 규모가 500만 달러 이상인 상품과 기업을 ‘현재 세계일류’로, 향후 7년 이내에 ‘현재 세계일류’ 전환 가능성이 있는 상품과 기업을 ‘차세대 세계일류’로 선정한다.선정된 기업은 해외 마케팅, 금융 지원, 수출 컨설팅 등 다양한 혜택을 통해 글로벌 시장에서의 경쟁력을 한층 강화할 수 있다.HK이노엔의 케이캡은 대한민국 제30호 신약으로, 위식도역류질환 치료 분야에서 새로운 표준을 제시한 P-CAB 계열 치료제다.현재 케이캡은 해외 53개국과 기술수출 또는 완제수출 계약을 체결했으며, 국내를 포함해 중국, 중남미 등 18개국에 출시돼 글로벌 시장에서 입지를 넓히고 있다.HK이노엔 관계자는 "케이캡이 세계일류상품으로 선정된 것은 글로벌 시장에서의 가능성을 인정받은 결과"라며, "앞으로도 혁신적인 신약 개발과 글로벌 시장 확대를 통해 대한민국 제약산업의 위상을 높이는 데 기여하겠다"고 밝혔다.한편 지난 해까지 전자제품, 자동차, 화학 및 소재, 의료기기, 식품 등 전 산업군 974개의 상품과 1094개의 생산기업이 세계일류상품으로 선정됐다.2025-11-19 10:28:38황병우
HK이노엔 케이캡, 세계일류상품 선정…의약품 중 유일세계일류상품 인증서 수여식에서 산업통상부 최연우 중견기업정책관(사진 왼쪽)과 HK이노엔 R&D전략실 박현정 상무(사진 오른쪽)가 기념사진을 찍고 있다. [데일리팜=황병우 기자] HK이노엔은 위식도역류질환 신약 케이캡(성분명 테고프라잔)이 산업통상자원부와 KOTRA가 주관하는 세계일류상품 육성사업에서 '현재 세계일류상품'으로 선정됐다고 19일 밝혔다.올해 선정된 97개의 '현재 세계일류상품' 중 의약품으로는 케이캡이 유일하다.‘세계일류상품 육성사업’은 국내 우수 상품의 글로벌 시장 진출 확대와 수출 경쟁력 강화를 위해 2001년부터 산업통상자원부와 KOTRA가 운영 중인 인증사업이다.세계시장점유율 5% 이상, 세계 5위 이내이며 연간 수출 규모가 500만 달러 이상인 상품과 기업을 ‘현재 세계일류’로, 향후 7년 이내에 ‘현재 세계일류’ 전환 가능성이 있는 상품과 기업을 ‘차세대 세계일류’로 선정한다.선정된 기업은 해외 마케팅, 금융 지원, 수출 컨설팅 등 다양한 혜택을 통해 글로벌 시장에서의 경쟁력을 한층 강화할 수 있다.HK이노엔의 케이캡은 대한민국 제30호 신약으로, 위식도역류질환 치료 분야에서 새로운 표준을 제시한 P-CAB 계열 치료제다.현재 케이캡은 해외 53개국과 기술수출 또는 완제수출 계약을 체결했으며, 국내를 포함해 중국, 중남미 등 18개국에 출시돼 글로벌 시장에서 입지를 넓히고 있다.HK이노엔 관계자는 "케이캡이 세계일류상품으로 선정된 것은 글로벌 시장에서의 가능성을 인정받은 결과"라며, "앞으로도 혁신적인 신약 개발과 글로벌 시장 확대를 통해 대한민국 제약산업의 위상을 높이는 데 기여하겠다"고 밝혔다.한편 지난 해까지 전자제품, 자동차, 화학 및 소재, 의료기기, 식품 등 전 산업군 974개의 상품과 1094개의 생산기업이 세계일류상품으로 선정됐다.2025-11-19 10:28:38황병우 -
 식약처 "청소년 비만치료제, 비만 환자만 사용 가능"[데일리팜=이탁순 기자] 식약처가 최근 청소년에도 승인된 비만치료제는 반드시 해당 나이대 비만 환자만 사용 가능하다고 강조했다.오남용 우려를 사전에 차단하기 위해 의약품 안전 정보 대국민 홍보해 나선 것으로 풀이된다.식약처는 14일 12세 이상 청소년에 투여 가능한 GLP-1 계열 비만치료제의 청소년 맞춤형 의약품 안전 정보를 안내한다고 밝혔다.GLP-1 계열은 포도당 의존적인 인슐린 분비 증가, 글루카곤 분비 저해, 허기 지연 및 체중 감소효과가 있는 글루카곤 유사 펩타이드(GLP-1) 성분 치료제이다.12세 이상 청소년에 투여 가능한 GLP-1 계열 비만치료제는 노보노디스크제약의 위고비(세마글루타이드)이다. 위고비는 지난 10월 25일 식약처로부터 12세 이상 청소년 비만 환자에도 허가를 받았다.이에반해 성인은 한 가지 이상의 체중 관련 동반질환이 있는 과체중 환자도 사용이 가능하다.청소년은 체질량지수(BMI)를 계산해 이를 성인 기준으로 환산한 값이 초기 30kg/m2 이상인 비만환자이면서 동시에 체중이 60kg을 초과해 의사로부터 비만으로 진단받은 12세 이상만 체중 관리를 위한 칼로리 저감 식이요법 및 신체활동 증대의 보조 목적으로 처방받을 수 있다.BMI는 몸무게(kg)를 키(m)를 두 번 곱한 값으로 나눈 값이다.임상시험 결과에 따르면 12세 이상 청소년 비만환자가 정상 투여하던 성인에 비해 담석증, 담낭염, 저혈압 등 부작용 발생률이 높았으며, 청소년 비만환자가 허가 범위 내에서 사용하더라도 구토, 설사, 복통 등 위장관계 이상사례를 포함한 다양한 부작용이 나타날 수 있다. 청소년은 성장이 완료되지 않은 단계이므로, 성장에 영향을 줄 수 있는 영양 섭취 부족 및 체중 감소와 위장관계 부작용으로 인한 탈수, 급성 췌장염 등에 대한 면밀한 관찰이 요구된다. 따라서, 반드시 의사의 처방 후 약사의 조제·복약지도에 따라 허가 범위 내에서 사용해야 한다고 식약처는 강조했다.식약처는 청소년 맞춤형 비만치료제의 올바른 사용방법 정보를 제공하기 위해 ▲비만치료제 사용 대상 ▲투여방법 및 투여시 주의사항 ▲보관·폐기방법 ▲이상사례(부작용) 및 보고방법 등을 담은 비만치료제 안전사용 리플릿을 전국 보건소, 의료기관 및 병원약사회 등 관련 단체를 대상으로 배포할 방침이다.아울러, 교육부와 함께 비만치료제 안전사용 리플릿을 각급 학교를 통해 각 가정에 안내하고, 함께학교·학부모On누리를 통해 카드뉴스 등을 게재해 비만치료제를 투여 또는 투여를 고려하고 있는 청소년과 학부모에게 정확한 정보를 지속적으로 전달한다고 밝혔다.또한, 성평등가족부와 협력하여 통합정보망 ‘청소년1388’, 청소년 활동정보 서비스 'e청소년', 국립청소년수련원 등 청소년이 많이 이용하는 누리집과 시설을 통해 비만치료제의 맞춤형 안전사용 정보를 제공해 비만치료제가 본래의 목적에 맞지 않게 사용되는 일이 없도록 홍보할 계획이다.식약처는 GLP-1 계열 비만치료제의 작년 하반기 출시 후 사용량이 증가함에 따라 부작용 보고 또한 지속적으로 증가하고 있어, '이상사례 집중 모니터링 대상'으로 지정해 한국의약품안전관리원과 함께 부작용을 지속적으로 모니터링하고 있다.특히, 청소년 사용 확대에 따라 비만치료제가 안전하게 사용될 수 있도록 오남용 방지 홍보 등을 더욱 강화할 예정이라고 밝혔다.2025-11-14 09:46:10이탁순
식약처 "청소년 비만치료제, 비만 환자만 사용 가능"[데일리팜=이탁순 기자] 식약처가 최근 청소년에도 승인된 비만치료제는 반드시 해당 나이대 비만 환자만 사용 가능하다고 강조했다.오남용 우려를 사전에 차단하기 위해 의약품 안전 정보 대국민 홍보해 나선 것으로 풀이된다.식약처는 14일 12세 이상 청소년에 투여 가능한 GLP-1 계열 비만치료제의 청소년 맞춤형 의약품 안전 정보를 안내한다고 밝혔다.GLP-1 계열은 포도당 의존적인 인슐린 분비 증가, 글루카곤 분비 저해, 허기 지연 및 체중 감소효과가 있는 글루카곤 유사 펩타이드(GLP-1) 성분 치료제이다.12세 이상 청소년에 투여 가능한 GLP-1 계열 비만치료제는 노보노디스크제약의 위고비(세마글루타이드)이다. 위고비는 지난 10월 25일 식약처로부터 12세 이상 청소년 비만 환자에도 허가를 받았다.이에반해 성인은 한 가지 이상의 체중 관련 동반질환이 있는 과체중 환자도 사용이 가능하다.청소년은 체질량지수(BMI)를 계산해 이를 성인 기준으로 환산한 값이 초기 30kg/m2 이상인 비만환자이면서 동시에 체중이 60kg을 초과해 의사로부터 비만으로 진단받은 12세 이상만 체중 관리를 위한 칼로리 저감 식이요법 및 신체활동 증대의 보조 목적으로 처방받을 수 있다.BMI는 몸무게(kg)를 키(m)를 두 번 곱한 값으로 나눈 값이다.임상시험 결과에 따르면 12세 이상 청소년 비만환자가 정상 투여하던 성인에 비해 담석증, 담낭염, 저혈압 등 부작용 발생률이 높았으며, 청소년 비만환자가 허가 범위 내에서 사용하더라도 구토, 설사, 복통 등 위장관계 이상사례를 포함한 다양한 부작용이 나타날 수 있다. 청소년은 성장이 완료되지 않은 단계이므로, 성장에 영향을 줄 수 있는 영양 섭취 부족 및 체중 감소와 위장관계 부작용으로 인한 탈수, 급성 췌장염 등에 대한 면밀한 관찰이 요구된다. 따라서, 반드시 의사의 처방 후 약사의 조제·복약지도에 따라 허가 범위 내에서 사용해야 한다고 식약처는 강조했다.식약처는 청소년 맞춤형 비만치료제의 올바른 사용방법 정보를 제공하기 위해 ▲비만치료제 사용 대상 ▲투여방법 및 투여시 주의사항 ▲보관·폐기방법 ▲이상사례(부작용) 및 보고방법 등을 담은 비만치료제 안전사용 리플릿을 전국 보건소, 의료기관 및 병원약사회 등 관련 단체를 대상으로 배포할 방침이다.아울러, 교육부와 함께 비만치료제 안전사용 리플릿을 각급 학교를 통해 각 가정에 안내하고, 함께학교·학부모On누리를 통해 카드뉴스 등을 게재해 비만치료제를 투여 또는 투여를 고려하고 있는 청소년과 학부모에게 정확한 정보를 지속적으로 전달한다고 밝혔다.또한, 성평등가족부와 협력하여 통합정보망 ‘청소년1388’, 청소년 활동정보 서비스 'e청소년', 국립청소년수련원 등 청소년이 많이 이용하는 누리집과 시설을 통해 비만치료제의 맞춤형 안전사용 정보를 제공해 비만치료제가 본래의 목적에 맞지 않게 사용되는 일이 없도록 홍보할 계획이다.식약처는 GLP-1 계열 비만치료제의 작년 하반기 출시 후 사용량이 증가함에 따라 부작용 보고 또한 지속적으로 증가하고 있어, '이상사례 집중 모니터링 대상'으로 지정해 한국의약품안전관리원과 함께 부작용을 지속적으로 모니터링하고 있다.특히, 청소년 사용 확대에 따라 비만치료제가 안전하게 사용될 수 있도록 오남용 방지 홍보 등을 더욱 강화할 예정이라고 밝혔다.2025-11-14 09:46:10이탁순 -
 첫 킬로미크론혈증 증후군 ASO 치료제 '올레자르센'아이오니스 파마슈티컬스(Ionis Pharmaceuticals)의 트린골자(TryngolzaⓇ, 성분명 올레자르센)는 APOC3 표적 antisense oligonucleotide(ASO) 제제로, 작년 미국 FDA, 올해 9월 유럽 EMA에서 성인 가족성 킬로미크론혈증 증후군(Familial Chylomicronemia Syndrome, FCS) 환자의 중성지방 감소를 위한 식이요법 보조 치료제로 최초 승인됐다.가족성 킬로미크론혈증 증후군(FCS)은 지단백분해효소(Lipoprotein Lipase, LPL) 또는 그 조절 인자의 결함으로 인해 소장에서 유래한 중성지방(TG) 풍부 지단백인 킬로미크론(chylomicron)이 적절히 분해되지 못하고 혈중에 병리적으로 축적되는 질환이다. 이로 인해 급성 췌장염(acute Pancreatitis)과 같은 심각하고 치명적인 합병증이 발생할 수 있다.올레자르센은 antisense RNA 기술을 활용해 간세포 내 APOC3 mRNA를 선택적으로 억제함으로써 apoC-III 단백질 생성량을 감소시키는 제제이다.그 결과 중성지방 분해를 저해하던 apoC-III 수준이 낮아지면서 LPL 매개 지질분해와 킬로미크론 제거가 촉진되고, 궁극적으로 중성지방 대사가 정상화된다. 즉, LPL 기능 저하로 TG가 축적되는 FCS 환자에서 apoC-III 감소를 통해 TG 제거 경로를 간접적으로 활성화하는 기전을 갖는다.이 약제의 허가는 3상 BALANCE 임상시험에서 확인된 유의한 효과와 안전성 결과를 근거로 이뤄졌다. 해당 연구 결과는 New England Journal of Medicine(NEJM)에 게재됐다.임상시험에서는 유전적으로 확진된 FCS 환자 66명을 대상으로 위약군 및 올레자르센 50mg, 80mg 피하 투여군(4주 간격)으로 무작위 배정하였다.그 결과, 6개월 시점에서 80mg군은 위약 대비 혈청 TG를 평균 42.5% 감소(P=0.0084)시켰으며, 급성 췌장염 발생 위험은 약 90% 감소했다. 또한 apoC-III 수치는 유의하게 감소했고, LDL-C는 용량 의존적으로 증가, apoB는 유의한 변화가 없었다.주요 이상반응으로는 주사 부위 반응, 혈소판 감소, 관절통, 경미한 혈당 및 간 효소 상승 등이 보고됐다.가족성 킬로미크론혈증 증후군(Familial Chylomicronemia Syndrome, FCS)은 무슨 질환인가?가족성 킬로미크론혈증 증후군(FCS)은 지단백분해효소(lipoprotein lipase, LPL) 또는 그 조절 단백의 유전적 결함으로 인해 발생하는 상염색체 열성 희귀 유전질환이다. 이로 인해 소장에서 흡수된 중성지방(triglyceride, TG)이 풍부한 킬로미크론(chylomicron, CM)이 적절히 분해되지 못하고 혈중에 병적으로 축적된다.정상 상태에서는 식후 림프계를 통해 혈중으로 유입된 CM이 LPL에 의해 TG가 유리지방산(non-esterified fatty acids)과 글리세롤(glycerol)로 가수분해되며, 약 3~4시간 내에 대부분 제거된다. 반면 FCS에서는 기능성 LPL이 거의 존재하지 않아, 공복 12시간 이상 경과해도 CM이 혈중에 잔류한다. 잔존 LPL의 미미한 활성이나 기타 혈장 리파아제의 보조 작용으로는 이를 보상할 수 없어, 지속적이며 중증의 고중성지방혈증이 발생한다.생화학적으로 FCS는 킬로미크론의 과도한 축적과 VLDL·LDL·HDL의 현저한 감소라는 독특한 지질 프로파일을 보인다. 외인성 TG 대사의 차단으로 CM 잔여입자 생성이 억제되고, 간에서 VLDL 합성에 필요한 지질 기질이 감소해 VLDL 및 LDL 수치가 낮거나 정상 수준에 머무른다. 또한 HDL은 CETP(cholesteryl ester transfer protein) 매개 지질 교환 증가와 불충분한 지질분해(lipolysis)로 인해 감소한다.FCS의 가장 심각한 합병증은 급성 췌장염(acute pancreatitis)으로, 혈중 TG가 1,000 mg/dL 이상에서 위험이 급격히 상승하며, FCS 환자에서는 보통 2,000–5,000 mg/dL 이상으로 유지되어 재발성 또는 만성 췌장염으로 진행할 수 있다. 병태생리적으로는 순환 중 CM이 췌장 모세혈관을 기계적으로 폐쇄하고, 제한적 LPL 작용으로 생성된 유리지방산(FFA)이 국소적으로 축적되어 세포 독성, 염증, 부종, 괴사를 유발한다.임상적으로는 극심한 상복부 통증, 구토, 발열, 혈청 아밀라아제·리파아제 상승이 특징이며, 반복적 염증은 췌장 섬유화와 외분비기능부전(exocrine insufficiency)으로 이어질 수 있다.또한, 간비대(hepatomegaly) 및 지방간(hepatic steatosis)이 흔히 동반된다. 이는 CM 및 TG의 만성 축적으로 인한 간세포 내 지방 침착이 원인으로, 장기간 지속 시 비알코올성 지방간염(NASH)으로 진행할 수 있으며, 이에 따른 간기능 저하 및 대사 합병증 위험도 보고되고 있다.더불어 혈중 지질입자 과잉은 비장비대(splenomegaly)와 다양한 조직 내 지질 침착(lipid deposition)을 초래할 수 있다. 특히 간, 비장, 망막, 피부 등에서 거품세포(foam cell) 형태의 축적이 관찰되며, 드물게 황색종(xanthomas) 등의 피부 병변으로 나타나기도 한다.킬로미크론(Chylomicrons. CM)이란 어떤 물질인가?음식을 통해 지방을 섭취하면, 소장에서 흡수된 지방은 장세포로 들어가 다시 중성지방(TG) 형태로 재합성된다. 이렇게 만들어진 TG는 일부는 세포 내에 저장되고, 일부는 킬로미크론(CM)이라는 지방 운반 입자를 형성하는 데 사용된다.CM은 처음에 아주 작은 씨앗 같은 형태의 전구체(pre-CM)로 만들어지며, 이때 핵심이 되는 구조 단백질이 바로 apoB-48이다. 이 apoB-48을 중심으로 TG가 차곡차곡 결합하면서 입자가 점차 커지고, 여기에 여러 지단백 관련 단백질이 더해지면 CM의 기본 골격이 완성된다.형성 초기의 CM은 골지체로 이동해 최종 가공을 거친다. 이 과정에서 필요한 단백질이 추가되고 구조가 정돈되며, 완성된 CM이 형성된다.완성된 CM은 장세포 밖으로 바로 혈액으로 들어가는 것이 아니라, 먼저 림프관으로 배출된다. 이후 림프 순환을 따라 이동해 흉관을 거쳐 쇄골하정맥(subclavian vein)으로 유입되면서 비로소 전신 혈액순환에 합류하게 된다.혈액 속으로 들어온 CM은 신체 여러 조직으로 이동해 지방을 전달한다. 근육에서는 에너지원으로 사용되고, 지방조직에서는 저장용으로 축적된다. 이 과정에서 CM 내 TG가 점점 빠져나가면서 입자는 작아지고, 결국 킬로미크론 잔여입자(CM remnant)라는 형태로 변한다.최종적으로 CM 잔여입자는 간으로 운반되어 제거된다. 간세포는 잔여입자 표면에 부착된 단백질 신호를 통해 이를 인식해 세포 내로 흡수하고, 분해하여 처리한다. 이 과정은 체내 지방의 운반과 분배가 효율적으로 이루어지도록 하는 중요한 생리적 단계다.Biogenesis of Lipoproteins(출처: Mass Spec Rev. 2023;42:1397–1423). 다시 정리하면, 섭취된 식이성 지방은 소장 내강에서 흡수된 후 장세포로 이동해 아포지질단백질 B-48(apoB-48)을 골격으로 CM을 형성한다. 형성된 CM은 림프계를 거쳐 혈액순환으로 유입되며, 순환계에 들어온 CM은 apoC-II에 의해 활성화된 지단백분해효소(LPL)에 의해 빠르게 가수분해된다.이 과정에서 방출된 유리지방산은 근육세포에서는 에너지원으로 산화되고, 지방조직에서는 다시 TG로 재합성되어 저장된다. TG가 제거되면서 입자는 점차 작아져 킬로미크론 잔여입자(CM remnant)가 되며, 이후 간세포 표면 수용체에 의해 인식되어 내재화(endocytosis)되고 분해됨으로써 순환계에서 제거된다.한편, TG는 간에서도 합성되며, 아포지질단백질 B-100(apoB-100)과 결합해 초저밀도지단백(VLDL, very low-density lipoprotein)을 형성한 뒤 혈액으로 분비된다. VLDL 역시 LPL의 작용을 받아 TG를 잃어가면서 중간밀도지단백(IDL, intermediate-density lipoprotein)로 전환되고, 이 과정에서도 유리지방산이 방출된다.생성된 IDL은 두 가지 경로를 따른다. 일부는 간에서 직접 제거되며, 나머지는 추가적인 LPL 및 hepatic lipase의 효소 작용을 통해 저밀도지단백(LDL, low-density lipoprotein)로 전환된다. LDL은 콜레스테롤이 풍부한 지단백으로, 말초 조직에 콜레스테롤을 공급하거나, 간으로 되돌아가 LDL 수용체에 의해 제거되는 등 체내 콜레스테롤 운반과 항상성 유지에 핵심적 역할을 한다.APOC3란 무엇인가APOC3는 간과 장에서 발현되는 유전자로, 이 유전자로부터 생성되는 단백질이 ApoC-III이다. 합성된 ApoC-III는 혈중 중성지방이 풍부한 지단백질(triglyceride-rich lipoproteins, TRLs)의 표면에 결합하여 지질 대사의 핵심 조절자로 기능한다.ApoC-III는 지단백분해효소(lipoprotein lipase, LPL)와 간 리파아제(hepatic lipase)의 활성을 억제하여 TRL의 분해(lipolysis)를 방해하고, 동시에 TRL 및 그 잔여입자의 간섭취(hepatic clearance)를 저해한다. 이러한 작용은 혈중 중성지방 상승과 TRL 잔여입자 축적을 초래하여, 죽상경화 발생 위험을 높이는 병태생리적 기반이 된다.유전역학적 연구는 APOC3/ApoC-III 축이 중성지방 대사 및 심혈관질환 위험에 인과적(causal) 역할을 한다는 명확한 근거를 제시한다. APOC3의 기능상실(loss-of-function, LOF) 변이를 보유한 개인은 ApoC-III 발현이 감소하여 혈중 중성지방 수치가 현저히 낮고, 관상동맥질환(ASCVD) 위험 또한 감소하는 것으로 보고된다.반대로 기능증가(gain-of-function, GOF) 변이나 APOC3의 과발현은 고중성지방혈증과 ASCVD 위험 증가와 밀접하게 연관되어 있다. 이러한 증거들은 APOC3가 단순한 지질 표지자를 넘어, 중성지방 대사를 조절하고 질환의 병태생리를 매개하는 핵심 인자임을 보여준다.APOC3는 주로 간세포(hepatocytes)에서 발현되며, 소장 상피세포(enterocytes)에서도 소량 발현된다. 이 유전자는 79개의 아미노산으로 구성된 소형 아포지단백질인 ApoC-III를 암호화한다.이러한 근거를 바탕으로 APOC3/ApoC-III 축은 고중성지방혈증, 죽상경화, TRL-관련 급성췌장염 등 다양한 대사·심혈관질환의 주요 치료 표적으로 부상하고 있다. 특히 기존 피브레이트나 오메가-3 지방산으로 조절되지 않는 난치성 고중성지방혈증 또는 가족성 킬로미크론혈증(FCS) 환자에서 APOC3 억제는 혈중 중성지방 및 ApoC-III 수치를 효과적으로 감소시키고, 췌장염 위험을 줄이는 잠재력을 보여주고 있다.Antisense oligonucleotide(ASO)는 무엇인가? ASO는 질병 관련 유전자의 발현을 RNA 단계에서 정밀하게 조절하도록 설계된 합성 핵산 치료제로, 표적 mRNA를 직접 억제함으로써 병태생리의 근본 원인을 교정하는 혁신적 치료 플랫폼이다.ASO는 일반적으로 뉴클레오타이드 15~25개로 구성되며, 표적 RNA와 상보적으로 결합하여 RNA 안정성, 스플라이싱, 번역 효율 등에 영향을 미친다. 이를 통해 단백질 생산 과정을 원천적으로 조절할 수 있다. 체내 투여된 ASO는 주로 간, 근육, 중추신경계 등 특정 장기에 분포한 뒤 세포 내로 유입되어 세포질과 핵에서 작용한다.ASO의 가장 대표적인 작용 기전은 RNase H1 매개 mRNA 절단(gene silencing)이다. ASO가 mRNA와 결합해 RNA–DNA hybrid를 형성하면 RNase H1이 이를 인식해 표적 mRNA를 절단하고, 절단된 mRNA는 신속히 분해된다. 그 결과 해당 단백질의 번역이 억제되며, 이는 과발현된 병적 단백질을 직접 감소시키는 데 매우 효과적이다(Figure 2). 이러한 기전은 대사질환, 염증질환, 신경·근육계 유전질환, 희귀질환 등 다양한 영역에서 임상적 효능이 입증되고 있다.RNase H1 ASO Mechanism of Action(출처: DNA AND CELL BIOLOGYVolume 39, Number 2, 2020).ASO는 스플라이싱 조절(splice modulation)을 통해 질환 원인 돌연변이를 교정하거나 기능적 단백질 아이소폼의 생성을 유도할 수도 있다. ASO가 pre-mRNA의 스플라이싱 조절 부위(exonic/intronic splicing enhancer 또는 silencer 등)에 결합하면, 스플라이싱 machinery의 접근 또는 조립을 선택적으로 억제·촉진하여 특정 엑손의 포함 또는 배제를 유도한다. 대표적 성공 사례로는 척수성 근위축증(SMA) 치료제 누시넨센(nusinersen, SpinrazaⓇ) 이 있다.이 외에도 ASO는 번역 억제, miRNA 기능 차단(antagomir-like effect), RNA 구조 변형을 통한 안정성 조절 등 다양한 분자적 경로로 작용한다. 이러한 약리 기전의 다양성은 ASO가 단일 기전에 국한되지 않고, RNA 수준에서 작동하는 정밀 유전자 조절 치료제임을 의미한다.ASO 기술 발전의 핵심은 화학적 구조 최적화였다. 초기에는 phosphorothioate(PS) 골격 변형을 통해 체내 안정성과 반감기를 연장했고, 이후 2’-O-methyl(2’-O-Me), 2’-O-methoxyethyl(2’-MOE) 및 locked nucleic acid(LNA) 등 2·3세대 핵산 변형 기술이 도입되어 결합 친화력, 선택성, 면역반응 감소, 독성 개선이 크게 진전됐다.최근에는 N-acetylgalactosamine(GalNAc) 결합 플랫폼의 도입으로 ASGPR 수용체를 통한 간세포 특이적 전달이 가능해지며, 효능 증대와 전신 부작용 최소화라는 중요한 기술적 도약이 이루어졌다.따라서 ASO는 DNA-단백질 축 사이의 핵심 매개 단계인 RNA를 직접 조절함으로써 유전자 발현을 분자 수준에서 교정하는 정밀 치료 전략이며, 기존의 단백질 표적 기반 치료제 또는 유전자 치료제와 차별화되는 혁신적 RNA 약물 플랫폼으로 자리매김하고 있다.가족성 킬로미크론혈증증후군(FCS) 기존 치료제에는 어떤 약제들이 있는가?FCS에서 약물치료로 시도되어 온 기존 약제에는 피브레이트, 오메가-3 지방산, 니아신 등이 있다. 그러나 이들 약제는 모두 LPL 의존적 경로를 기반으로 작용하기 때문에, LPL 또는 조절 단백의 유전적 결함을 특징으로 하는 FCS에서는 치료 효과가 제한적이다.피브레이트(fibrates)는 가장 오래된 고중성지방혈증 치료제로, 대표 약제로는 fenofibrate, gemfibrozil, bezafibrate 등이 있다.피브레이트는 PPAR-α(peroxisome proliferator–activated receptor-α)를 활성화하여 LPL 발현 증가, ApoC-III 발현 억제, 지방산 산화 촉진을 통해 TG를 감소시킨다. 이차성 고중성지방혈증에서는 의미 있는 TG 감소 효과가 있으나, FCS에서는 LPL 자체가 결핍되어 있어 치료 반응이 거의 나타나지 않는다. 또한 간효소 상승, 근육통, 신기능 저하 등의 부작용 가능성도 고려해야 한다.오메가-3 지방산(omega-3 fatty acids)은 EPA(eicosapentaenoic acid) 및 DHA(docosahexaenoic acid)를 기반으로 한 제제로, 간 내 TG 합성 억제 및 VLDL 분비 감소를 통해 TG 저하 효과를 보인다. 일반 고중성지방혈증에서는 20~30%의 TG 감소가 가능하나, 킬로미크론 축적이 근본 문제인 FCS에서는 LPL 비의존적 기전의 한계로 효과가 매우 제한적이며, 대개 10–20% 수준의 감소에 그친다. 이러한 수준의 감소는 급성 췌장염 위험 감소에는 불충분하다.니아신(niacin; 비타민 B3)은 과거 TG 감소와 HDL 상승 목적으로 사용되었으나, 혈당 상승, 간독성, 안면홍조(flushing) 등의 부작용으로 인해 현재는 임상적 사용이 거의 중단되었다. 특히 FCS 환자에서는 TG 감소 효과가 미미하고 안전성 문제가 커 실제 임상적 적용이 사실상 배제된 상태다.종합하면, 피브레이트, 오메가-3 지방산, 니아신 등 기존 약제들은 LPL 기능 강화 또는 지방 합성 억제에 의존하는 간접적 기전이므로, LPL 결핍이라는 FCS의 근본 병태를 해결하지 못한다. 이 때문에 FCS 치료의 핵심은 여전히 극단적 저지방 식이(< 20g/일)에 의존하고 있으며, 중증 환자에서는 충분한 예방 효과가 보장되지 않는다.최근 들어 ApoC-III 또는 ANGPTL3를 표적하는 RNA 기반 신약이 LPL 비의존적 기전을 통해 직접 병태생리를 교정하는 혁신적 치료 전략(mechanistic innovation)으로 주목받고 있다.APOC3 억제제는 어떤 약제인가?Apolipoprotein C-III(APOC3)는 단순한 지질 표지자를 넘어 중성지방(TG) 대사의 핵심 조절자로, 지단백 분해 억제, TRL 잔여입자 축적, 인슐린 저항성 및 염증 유도 등 다양한 병태생리 기전에 관여한다.특히 유전학적 근거에 따르면, APOC3 유전자의 기능 상실(loss-of-function) 변이 보유자는 중성지방 수치가 현저히 낮고, ASCVD 발생률 및 TRL-연관 급성 췌장염 위험이 감소하는 것으로 보고되었다. 이러한 결과는 APOC3가 질환의 병태생리에 직접적 역할을 한다는 점을 뒷받침하며, 유효한 치료 표적(targetable driver) 으로 확립되는 근거가 되었다.이러한 근거를 바탕으로, APOC3 발현을 선택적으로 억제하는 RNA 기반 치료제 개발이 활발히 진행되고 있다. 대표적인 플랫폼은 antisense oligonucleotide(ASO) 와 small interfering RNA(siRNA) 로, 모두 APOC3 mRNA를 직접 표적하여 ApoC-III 단백질 합성을 감소시키는 정밀 RNA치료 전략이다.초기 ASO 제제인 volanesorsen은 FCS 환자를 대상으로 ApoC-III와 중성지방 수치를 현저히 감소시키며 치료 잠재력을 입증했으나, 혈소판감소증(thrombocytopenia) 등 안전성 문제가 임상적 활용의 제약 요인으로 작용했다. 이러한 한계를 보완하기 위해 간 표적 GalNAc 결합 기술이 적용된 2세대 ASO인 olezarsen이 개발되었으며, 보다 우수한 안전성 프로파일과 강력한 TG 감소 효과가 관찰되고 있다.동시에 siRNA 플랫폼 기반의 plozasiran(ARO-APOC3) 역시 간세포 내 APOC3 발현을 억제하는 기전으로 개발 중이다.이 차세대 APOC3 억제제들은 기존 치료에 반응이 미흡한 난치성·중증 고중성지방혈증 환자군에게 새로운 치료 대안을 제공할 뿐 아니라, TRL-잔여 위험(residual risk) 감소를 통한 심혈관질환 예방 측면에서도 잠재적 가치를 보여주고 있다. 특히 TG 감소 외에도 간·췌장 합병증 개선 가능성, 심혈관 위험 지표 개선, 대사염증 경감 효과 등이 탐색되고 있어 적용 범위가 확장될 전망이다.결론적으로, APOC3 억제제는 중성지방 대사의 근본 조절축을 정밀하게 표적하는 혁신적 RNA 기반 치료 전략으로, 고중성지방혈증, 죽상경화성 심혈관질환, TRL-연관 급성 췌장염 등 다양한 대사 및 심혈관질환 영역에서 새로운 치료 패러다임을 제시하고 있다.올레자르센의 약리적 기전은 어떠한가? 올레자르센은 표적 mRNA와 상보적으로 결합하여 RNA–DNA hybrid를 형성하고, RNase H1을 활성화해 APOC3 mRNA를 절단·분해한다. 이로써 apoC-III 단백질 발현이 감소하고, LPL 활성이 회복되며, 간으로의 TRL 잔여입자 제거가 촉진되어 혈중 중성지방 농도가 유의하게 감소한다.간세포 선택성을 강화하기 위해 5’ 말단에는 삼지형(triantennary) N-아세틸갈락토사민(GalNAc) 리간드가 결합되어 있다. 이를 통해 asialoglycoprotein receptor(ASGPR)를 매개로 한 간세포 특이적 흡수가 가능해지며, 세포내섭취(endocytosis)를 거쳐 간세포 내로 이동한 후 표적 mRNA를 분해한다.The ASO Drug Olezarsen Targets Familial Chylomicronemia Syndrome[출처: https://www.cell.com/trends/pharmacological-sciences/abstract /S0165-6147(25) 00097-5]APOC3 억제를 통한 기전은 크게 세 가지로 정리된다. 첫째, 잔존 LPL 활성(residual LPL activity)을 강화하여 중성지방 분해를 촉진하고, 둘째, 중성지방이 풍부한 지단백(TG-rich lipoprotein)의 생성과 분비를 억제하며, 셋째, LPL 비의존적 대사 경로(alternative catabolic pathways)를 활성화하여 추가적인 중성지방 감소를 유도한다.올레자르센은 5–10–5 gapmer 구조로 설계되었으며, 2’-O-methoxyethyl(2’-MOE) 수식 염기와 phosphorothioate 골격을 적용해 안정성과 결합 친화도를 높였다. 내부 DNA 서열은 RNase H1 유도를 위한 구조적 요건을 유지하며, 5-methylcytosine과 5-methyluridine의 도입은 염기쌍 안정성과 표적 결합력을 강화한다.결과적으로, 올레자르센은 APOC3 mRNA 발현을 선택적으로 억제함으로써 혈중 중성지방을 효과적으로 감소시키는 정밀 RNA 기반 치료제로, 고중성지방혈증 및 가족성 킬로미크론혈증(FCS)의 병태생리를 표적하는 혁신적 치료 옵션으로서 임상적 의의가 크다.올레잘센(TRYNGOLZA)의 허가 임상 결과는 어떠한가?TRYNGOLZA의 효능은 유전적으로 FCS이 확인된 성인 환자 중, 공복 중성지방(TG) 수치가 880mg/dL 이상인 환자를 대상으로 실시된 무작위 배정, 위약 대조, 이중맹검 임상시험(Trial 1)을 통해 입증되었다.시험에 앞서 모든 환자는 1일 지방 섭취량을 20g 이하로 제한하는 저지방 식이요법을 최소 4주 이상 유지하는 준비(run-in) 기간을 거쳤다. 이후 환자들은 무작위로 배정되어, TRYNGOLZA 80mg(n=22) 또는 동일 용량의 위약(placebo, n=23)을 피하 주사 형태로 4주 간격으로 53주간 투여받았다.환자 인구학적 및 기저 특성은 두 치료군 간 전반적으로 유사하였다 등록 시 당뇨병을 동반한 환자 비율은 TRYNGOLZA 80mg 군 32%, 위약군 26%였다.연구 시작 시 TRYNGOLZA 80mg 군과 위약군 모두에서 스타틴(27%), 오메가-3 지방산(42%), 피브레이트(49%), 또는 기타 지질강하제(13%)가 병용 사용되었다.두 군을 합쳐 71%의 환자가 과거 10년 이내에 급성 췌장염(acute pancreatitis) 병력이 있었다. 기저 시점의 공복 중성지방 평균(SD) 수치는 2,604(1,364)mg/dL, 중앙값은 2,303mg/dL이었으며, 범위는 334–6,898mg/dL이었다.1차 평가변수(primary endpoint)는 기저치 대비 6개월차(23, 25, 27주차 평균)의 공복 중성지방 변화율(%)로, 위약군과 비교하여 분석되었다.그 결과, TRYNGOLZA 80mg 투여군은 위약군 대비 공복 중성지방 변화율이 -42.5%로 유의하게 감소하였다(95% 신뢰구간: -74.1% ~ -10.9%; p = 0.0084). 추가 결과는 Table 2를 참조. 기저치 대비 중앙값 변화율(Figure 1)과 중앙값 절대 중성지방(TG) 수치(Figure 2)는, 12개월 치료 기간 동안 일관된 중성지방 감소 효과를 보여주었다. 12개월의 치료 기간 동안, TRYNGOLZA 80mg을 투여받은 환자군에서 급성 췌장염(acute pancreatitis)의 발생률은 위약군보다 낮았다.TRYNGOLZA 80mg 투여군에서는 1명(5%), 위약군에서는 7명(30%의 환자에서 급성 췌장염이 보고되었다. 이들 모든 환자는 시험 등록 10년 이내에 췌장염 병력을 가지고 있었다.올레잘센의 쟁점이 될 수 있는 부분은?올레잘센은 FCS 최초이자 유일한 치료 옵션으로, 성인 FCS 환자에서 식이요법의 보조요법으로 중성지방(TG)을 유의하게 감소시킨다. 월 1회 80 mg 피하주사라는 단순한 용법 또한 장점으로 꼽힌다. 유사 기전 약물인 volanesorsen과 plozasiran은 아직 미국 FDA 승인을 받지 못했다.올레잘센의 허가 임상은 FCS 및 중증 고중성지방혈증 환자에서 유의미한 TG 감소 효과를 입증하며 치료적 진전을 보여주었으나, 해석 시 고려해야 할 중요한 한계가 존재한다.첫째, 대부분의 임상이 소수의 환자를 대상으로 수행되어 결과의 일반화 가능성에 제약이 있다. 희귀질환 특성상 환자 모집이 어렵지만, 연구 참여자의 인종적·임상적 다양성이 충분히 확보되지 않아 실제 진료 현장에 완전히 적용하기에는 한계가 있다. 또한 평가 기간이 주로 6~12개월에 그쳐 장기 투여 시 효과 지속성 및 누적 부작용에 대한 근거가 부족하다.둘째, 유효성 평가지표로 사용된 TG 감소는 대리결과(surrogate endpoint)에 해당한다. 급성 췌장염 발생 감소, 심혈관 사건 예방, 생존율 향상과 같은 최종 임상결과(hard outcomes)에 대한 근거는 충분히 축적되지 않았다. 이는 약물의 장기적 임상적 가치 평가 측면에서 중요한 한계다.셋째, 희귀질환 치료제 특성상 높은 치료비용과 접근성 제약 문제는 실제 임상 적용과 보건의료 자원 배분에서 중요한 고려 요소로 남아 있다.종합하면, 올레잘센은 고중성지방혈증 치료 영역에서 치료적 가치를 지닌 유망한 옵션으로 부상하고 있으나, 장기 안전성, 하드엔드포인트 근거, 비용-효과성 등 해결해야 할 과제가 여전히 존재한다. 향후 충분한 규모와 이질적 환자군을 포함한 장기 추적 연구가 수행되어, 실제 진료 환경에서의 임상적 유용성과 안전성이 확립되기를 기대한다.참고문헌 1. Erica Gianazza et al. “Proteomic studies on apoB‐containing lipoprotein in cardiovascular research: A comprehensive review” Mass Spec Rev. 2023;42:1397–1423. 2. Anne V. Smith1 and Sarah J. Tabrizi “Therapeutic Antisense Targeting of Huntingtin” DNA AND CELL BIOLOGYVolume 39, Number 2, 2020). 3. Fiza Javed et al. “Familial chylomicronemia syndrome: An expert clinical review from the National Lipid Association” Journal of Clinical Lipidology, Vol 19, No 3, May/June 2025 4. Kexin Wang et al. “Remnant cholesterol and atherosclerotic cardiovascular disease: Metabolism, mechanism, evidence, and treatment” Front. Cardiovasc. Med. 9:913869. 5. Erik S. et al “Olezarsen, Acute Pancreatitis, and Familial Chylomicronemia Syndrome” N Engl J Med 2024;390:1781-1792. 6. Jan Borén et al. “The Roles of ApoC-III on the Metabolism of Triglyceride-Rich Lipoproteins in Humans“ Humans. Front. Endocrinol. 11:474 2020. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).2025-11-06 21:18:18최병철 박사
첫 킬로미크론혈증 증후군 ASO 치료제 '올레자르센'아이오니스 파마슈티컬스(Ionis Pharmaceuticals)의 트린골자(TryngolzaⓇ, 성분명 올레자르센)는 APOC3 표적 antisense oligonucleotide(ASO) 제제로, 작년 미국 FDA, 올해 9월 유럽 EMA에서 성인 가족성 킬로미크론혈증 증후군(Familial Chylomicronemia Syndrome, FCS) 환자의 중성지방 감소를 위한 식이요법 보조 치료제로 최초 승인됐다.가족성 킬로미크론혈증 증후군(FCS)은 지단백분해효소(Lipoprotein Lipase, LPL) 또는 그 조절 인자의 결함으로 인해 소장에서 유래한 중성지방(TG) 풍부 지단백인 킬로미크론(chylomicron)이 적절히 분해되지 못하고 혈중에 병리적으로 축적되는 질환이다. 이로 인해 급성 췌장염(acute Pancreatitis)과 같은 심각하고 치명적인 합병증이 발생할 수 있다.올레자르센은 antisense RNA 기술을 활용해 간세포 내 APOC3 mRNA를 선택적으로 억제함으로써 apoC-III 단백질 생성량을 감소시키는 제제이다.그 결과 중성지방 분해를 저해하던 apoC-III 수준이 낮아지면서 LPL 매개 지질분해와 킬로미크론 제거가 촉진되고, 궁극적으로 중성지방 대사가 정상화된다. 즉, LPL 기능 저하로 TG가 축적되는 FCS 환자에서 apoC-III 감소를 통해 TG 제거 경로를 간접적으로 활성화하는 기전을 갖는다.이 약제의 허가는 3상 BALANCE 임상시험에서 확인된 유의한 효과와 안전성 결과를 근거로 이뤄졌다. 해당 연구 결과는 New England Journal of Medicine(NEJM)에 게재됐다.임상시험에서는 유전적으로 확진된 FCS 환자 66명을 대상으로 위약군 및 올레자르센 50mg, 80mg 피하 투여군(4주 간격)으로 무작위 배정하였다.그 결과, 6개월 시점에서 80mg군은 위약 대비 혈청 TG를 평균 42.5% 감소(P=0.0084)시켰으며, 급성 췌장염 발생 위험은 약 90% 감소했다. 또한 apoC-III 수치는 유의하게 감소했고, LDL-C는 용량 의존적으로 증가, apoB는 유의한 변화가 없었다.주요 이상반응으로는 주사 부위 반응, 혈소판 감소, 관절통, 경미한 혈당 및 간 효소 상승 등이 보고됐다.가족성 킬로미크론혈증 증후군(Familial Chylomicronemia Syndrome, FCS)은 무슨 질환인가?가족성 킬로미크론혈증 증후군(FCS)은 지단백분해효소(lipoprotein lipase, LPL) 또는 그 조절 단백의 유전적 결함으로 인해 발생하는 상염색체 열성 희귀 유전질환이다. 이로 인해 소장에서 흡수된 중성지방(triglyceride, TG)이 풍부한 킬로미크론(chylomicron, CM)이 적절히 분해되지 못하고 혈중에 병적으로 축적된다.정상 상태에서는 식후 림프계를 통해 혈중으로 유입된 CM이 LPL에 의해 TG가 유리지방산(non-esterified fatty acids)과 글리세롤(glycerol)로 가수분해되며, 약 3~4시간 내에 대부분 제거된다. 반면 FCS에서는 기능성 LPL이 거의 존재하지 않아, 공복 12시간 이상 경과해도 CM이 혈중에 잔류한다. 잔존 LPL의 미미한 활성이나 기타 혈장 리파아제의 보조 작용으로는 이를 보상할 수 없어, 지속적이며 중증의 고중성지방혈증이 발생한다.생화학적으로 FCS는 킬로미크론의 과도한 축적과 VLDL·LDL·HDL의 현저한 감소라는 독특한 지질 프로파일을 보인다. 외인성 TG 대사의 차단으로 CM 잔여입자 생성이 억제되고, 간에서 VLDL 합성에 필요한 지질 기질이 감소해 VLDL 및 LDL 수치가 낮거나 정상 수준에 머무른다. 또한 HDL은 CETP(cholesteryl ester transfer protein) 매개 지질 교환 증가와 불충분한 지질분해(lipolysis)로 인해 감소한다.FCS의 가장 심각한 합병증은 급성 췌장염(acute pancreatitis)으로, 혈중 TG가 1,000 mg/dL 이상에서 위험이 급격히 상승하며, FCS 환자에서는 보통 2,000–5,000 mg/dL 이상으로 유지되어 재발성 또는 만성 췌장염으로 진행할 수 있다. 병태생리적으로는 순환 중 CM이 췌장 모세혈관을 기계적으로 폐쇄하고, 제한적 LPL 작용으로 생성된 유리지방산(FFA)이 국소적으로 축적되어 세포 독성, 염증, 부종, 괴사를 유발한다.임상적으로는 극심한 상복부 통증, 구토, 발열, 혈청 아밀라아제·리파아제 상승이 특징이며, 반복적 염증은 췌장 섬유화와 외분비기능부전(exocrine insufficiency)으로 이어질 수 있다.또한, 간비대(hepatomegaly) 및 지방간(hepatic steatosis)이 흔히 동반된다. 이는 CM 및 TG의 만성 축적으로 인한 간세포 내 지방 침착이 원인으로, 장기간 지속 시 비알코올성 지방간염(NASH)으로 진행할 수 있으며, 이에 따른 간기능 저하 및 대사 합병증 위험도 보고되고 있다.더불어 혈중 지질입자 과잉은 비장비대(splenomegaly)와 다양한 조직 내 지질 침착(lipid deposition)을 초래할 수 있다. 특히 간, 비장, 망막, 피부 등에서 거품세포(foam cell) 형태의 축적이 관찰되며, 드물게 황색종(xanthomas) 등의 피부 병변으로 나타나기도 한다.킬로미크론(Chylomicrons. CM)이란 어떤 물질인가?음식을 통해 지방을 섭취하면, 소장에서 흡수된 지방은 장세포로 들어가 다시 중성지방(TG) 형태로 재합성된다. 이렇게 만들어진 TG는 일부는 세포 내에 저장되고, 일부는 킬로미크론(CM)이라는 지방 운반 입자를 형성하는 데 사용된다.CM은 처음에 아주 작은 씨앗 같은 형태의 전구체(pre-CM)로 만들어지며, 이때 핵심이 되는 구조 단백질이 바로 apoB-48이다. 이 apoB-48을 중심으로 TG가 차곡차곡 결합하면서 입자가 점차 커지고, 여기에 여러 지단백 관련 단백질이 더해지면 CM의 기본 골격이 완성된다.형성 초기의 CM은 골지체로 이동해 최종 가공을 거친다. 이 과정에서 필요한 단백질이 추가되고 구조가 정돈되며, 완성된 CM이 형성된다.완성된 CM은 장세포 밖으로 바로 혈액으로 들어가는 것이 아니라, 먼저 림프관으로 배출된다. 이후 림프 순환을 따라 이동해 흉관을 거쳐 쇄골하정맥(subclavian vein)으로 유입되면서 비로소 전신 혈액순환에 합류하게 된다.혈액 속으로 들어온 CM은 신체 여러 조직으로 이동해 지방을 전달한다. 근육에서는 에너지원으로 사용되고, 지방조직에서는 저장용으로 축적된다. 이 과정에서 CM 내 TG가 점점 빠져나가면서 입자는 작아지고, 결국 킬로미크론 잔여입자(CM remnant)라는 형태로 변한다.최종적으로 CM 잔여입자는 간으로 운반되어 제거된다. 간세포는 잔여입자 표면에 부착된 단백질 신호를 통해 이를 인식해 세포 내로 흡수하고, 분해하여 처리한다. 이 과정은 체내 지방의 운반과 분배가 효율적으로 이루어지도록 하는 중요한 생리적 단계다.Biogenesis of Lipoproteins(출처: Mass Spec Rev. 2023;42:1397–1423). 다시 정리하면, 섭취된 식이성 지방은 소장 내강에서 흡수된 후 장세포로 이동해 아포지질단백질 B-48(apoB-48)을 골격으로 CM을 형성한다. 형성된 CM은 림프계를 거쳐 혈액순환으로 유입되며, 순환계에 들어온 CM은 apoC-II에 의해 활성화된 지단백분해효소(LPL)에 의해 빠르게 가수분해된다.이 과정에서 방출된 유리지방산은 근육세포에서는 에너지원으로 산화되고, 지방조직에서는 다시 TG로 재합성되어 저장된다. TG가 제거되면서 입자는 점차 작아져 킬로미크론 잔여입자(CM remnant)가 되며, 이후 간세포 표면 수용체에 의해 인식되어 내재화(endocytosis)되고 분해됨으로써 순환계에서 제거된다.한편, TG는 간에서도 합성되며, 아포지질단백질 B-100(apoB-100)과 결합해 초저밀도지단백(VLDL, very low-density lipoprotein)을 형성한 뒤 혈액으로 분비된다. VLDL 역시 LPL의 작용을 받아 TG를 잃어가면서 중간밀도지단백(IDL, intermediate-density lipoprotein)로 전환되고, 이 과정에서도 유리지방산이 방출된다.생성된 IDL은 두 가지 경로를 따른다. 일부는 간에서 직접 제거되며, 나머지는 추가적인 LPL 및 hepatic lipase의 효소 작용을 통해 저밀도지단백(LDL, low-density lipoprotein)로 전환된다. LDL은 콜레스테롤이 풍부한 지단백으로, 말초 조직에 콜레스테롤을 공급하거나, 간으로 되돌아가 LDL 수용체에 의해 제거되는 등 체내 콜레스테롤 운반과 항상성 유지에 핵심적 역할을 한다.APOC3란 무엇인가APOC3는 간과 장에서 발현되는 유전자로, 이 유전자로부터 생성되는 단백질이 ApoC-III이다. 합성된 ApoC-III는 혈중 중성지방이 풍부한 지단백질(triglyceride-rich lipoproteins, TRLs)의 표면에 결합하여 지질 대사의 핵심 조절자로 기능한다.ApoC-III는 지단백분해효소(lipoprotein lipase, LPL)와 간 리파아제(hepatic lipase)의 활성을 억제하여 TRL의 분해(lipolysis)를 방해하고, 동시에 TRL 및 그 잔여입자의 간섭취(hepatic clearance)를 저해한다. 이러한 작용은 혈중 중성지방 상승과 TRL 잔여입자 축적을 초래하여, 죽상경화 발생 위험을 높이는 병태생리적 기반이 된다.유전역학적 연구는 APOC3/ApoC-III 축이 중성지방 대사 및 심혈관질환 위험에 인과적(causal) 역할을 한다는 명확한 근거를 제시한다. APOC3의 기능상실(loss-of-function, LOF) 변이를 보유한 개인은 ApoC-III 발현이 감소하여 혈중 중성지방 수치가 현저히 낮고, 관상동맥질환(ASCVD) 위험 또한 감소하는 것으로 보고된다.반대로 기능증가(gain-of-function, GOF) 변이나 APOC3의 과발현은 고중성지방혈증과 ASCVD 위험 증가와 밀접하게 연관되어 있다. 이러한 증거들은 APOC3가 단순한 지질 표지자를 넘어, 중성지방 대사를 조절하고 질환의 병태생리를 매개하는 핵심 인자임을 보여준다.APOC3는 주로 간세포(hepatocytes)에서 발현되며, 소장 상피세포(enterocytes)에서도 소량 발현된다. 이 유전자는 79개의 아미노산으로 구성된 소형 아포지단백질인 ApoC-III를 암호화한다.이러한 근거를 바탕으로 APOC3/ApoC-III 축은 고중성지방혈증, 죽상경화, TRL-관련 급성췌장염 등 다양한 대사·심혈관질환의 주요 치료 표적으로 부상하고 있다. 특히 기존 피브레이트나 오메가-3 지방산으로 조절되지 않는 난치성 고중성지방혈증 또는 가족성 킬로미크론혈증(FCS) 환자에서 APOC3 억제는 혈중 중성지방 및 ApoC-III 수치를 효과적으로 감소시키고, 췌장염 위험을 줄이는 잠재력을 보여주고 있다.Antisense oligonucleotide(ASO)는 무엇인가? ASO는 질병 관련 유전자의 발현을 RNA 단계에서 정밀하게 조절하도록 설계된 합성 핵산 치료제로, 표적 mRNA를 직접 억제함으로써 병태생리의 근본 원인을 교정하는 혁신적 치료 플랫폼이다.ASO는 일반적으로 뉴클레오타이드 15~25개로 구성되며, 표적 RNA와 상보적으로 결합하여 RNA 안정성, 스플라이싱, 번역 효율 등에 영향을 미친다. 이를 통해 단백질 생산 과정을 원천적으로 조절할 수 있다. 체내 투여된 ASO는 주로 간, 근육, 중추신경계 등 특정 장기에 분포한 뒤 세포 내로 유입되어 세포질과 핵에서 작용한다.ASO의 가장 대표적인 작용 기전은 RNase H1 매개 mRNA 절단(gene silencing)이다. ASO가 mRNA와 결합해 RNA–DNA hybrid를 형성하면 RNase H1이 이를 인식해 표적 mRNA를 절단하고, 절단된 mRNA는 신속히 분해된다. 그 결과 해당 단백질의 번역이 억제되며, 이는 과발현된 병적 단백질을 직접 감소시키는 데 매우 효과적이다(Figure 2). 이러한 기전은 대사질환, 염증질환, 신경·근육계 유전질환, 희귀질환 등 다양한 영역에서 임상적 효능이 입증되고 있다.RNase H1 ASO Mechanism of Action(출처: DNA AND CELL BIOLOGYVolume 39, Number 2, 2020).ASO는 스플라이싱 조절(splice modulation)을 통해 질환 원인 돌연변이를 교정하거나 기능적 단백질 아이소폼의 생성을 유도할 수도 있다. ASO가 pre-mRNA의 스플라이싱 조절 부위(exonic/intronic splicing enhancer 또는 silencer 등)에 결합하면, 스플라이싱 machinery의 접근 또는 조립을 선택적으로 억제·촉진하여 특정 엑손의 포함 또는 배제를 유도한다. 대표적 성공 사례로는 척수성 근위축증(SMA) 치료제 누시넨센(nusinersen, SpinrazaⓇ) 이 있다.이 외에도 ASO는 번역 억제, miRNA 기능 차단(antagomir-like effect), RNA 구조 변형을 통한 안정성 조절 등 다양한 분자적 경로로 작용한다. 이러한 약리 기전의 다양성은 ASO가 단일 기전에 국한되지 않고, RNA 수준에서 작동하는 정밀 유전자 조절 치료제임을 의미한다.ASO 기술 발전의 핵심은 화학적 구조 최적화였다. 초기에는 phosphorothioate(PS) 골격 변형을 통해 체내 안정성과 반감기를 연장했고, 이후 2’-O-methyl(2’-O-Me), 2’-O-methoxyethyl(2’-MOE) 및 locked nucleic acid(LNA) 등 2·3세대 핵산 변형 기술이 도입되어 결합 친화력, 선택성, 면역반응 감소, 독성 개선이 크게 진전됐다.최근에는 N-acetylgalactosamine(GalNAc) 결합 플랫폼의 도입으로 ASGPR 수용체를 통한 간세포 특이적 전달이 가능해지며, 효능 증대와 전신 부작용 최소화라는 중요한 기술적 도약이 이루어졌다.따라서 ASO는 DNA-단백질 축 사이의 핵심 매개 단계인 RNA를 직접 조절함으로써 유전자 발현을 분자 수준에서 교정하는 정밀 치료 전략이며, 기존의 단백질 표적 기반 치료제 또는 유전자 치료제와 차별화되는 혁신적 RNA 약물 플랫폼으로 자리매김하고 있다.가족성 킬로미크론혈증증후군(FCS) 기존 치료제에는 어떤 약제들이 있는가?FCS에서 약물치료로 시도되어 온 기존 약제에는 피브레이트, 오메가-3 지방산, 니아신 등이 있다. 그러나 이들 약제는 모두 LPL 의존적 경로를 기반으로 작용하기 때문에, LPL 또는 조절 단백의 유전적 결함을 특징으로 하는 FCS에서는 치료 효과가 제한적이다.피브레이트(fibrates)는 가장 오래된 고중성지방혈증 치료제로, 대표 약제로는 fenofibrate, gemfibrozil, bezafibrate 등이 있다.피브레이트는 PPAR-α(peroxisome proliferator–activated receptor-α)를 활성화하여 LPL 발현 증가, ApoC-III 발현 억제, 지방산 산화 촉진을 통해 TG를 감소시킨다. 이차성 고중성지방혈증에서는 의미 있는 TG 감소 효과가 있으나, FCS에서는 LPL 자체가 결핍되어 있어 치료 반응이 거의 나타나지 않는다. 또한 간효소 상승, 근육통, 신기능 저하 등의 부작용 가능성도 고려해야 한다.오메가-3 지방산(omega-3 fatty acids)은 EPA(eicosapentaenoic acid) 및 DHA(docosahexaenoic acid)를 기반으로 한 제제로, 간 내 TG 합성 억제 및 VLDL 분비 감소를 통해 TG 저하 효과를 보인다. 일반 고중성지방혈증에서는 20~30%의 TG 감소가 가능하나, 킬로미크론 축적이 근본 문제인 FCS에서는 LPL 비의존적 기전의 한계로 효과가 매우 제한적이며, 대개 10–20% 수준의 감소에 그친다. 이러한 수준의 감소는 급성 췌장염 위험 감소에는 불충분하다.니아신(niacin; 비타민 B3)은 과거 TG 감소와 HDL 상승 목적으로 사용되었으나, 혈당 상승, 간독성, 안면홍조(flushing) 등의 부작용으로 인해 현재는 임상적 사용이 거의 중단되었다. 특히 FCS 환자에서는 TG 감소 효과가 미미하고 안전성 문제가 커 실제 임상적 적용이 사실상 배제된 상태다.종합하면, 피브레이트, 오메가-3 지방산, 니아신 등 기존 약제들은 LPL 기능 강화 또는 지방 합성 억제에 의존하는 간접적 기전이므로, LPL 결핍이라는 FCS의 근본 병태를 해결하지 못한다. 이 때문에 FCS 치료의 핵심은 여전히 극단적 저지방 식이(< 20g/일)에 의존하고 있으며, 중증 환자에서는 충분한 예방 효과가 보장되지 않는다.최근 들어 ApoC-III 또는 ANGPTL3를 표적하는 RNA 기반 신약이 LPL 비의존적 기전을 통해 직접 병태생리를 교정하는 혁신적 치료 전략(mechanistic innovation)으로 주목받고 있다.APOC3 억제제는 어떤 약제인가?Apolipoprotein C-III(APOC3)는 단순한 지질 표지자를 넘어 중성지방(TG) 대사의 핵심 조절자로, 지단백 분해 억제, TRL 잔여입자 축적, 인슐린 저항성 및 염증 유도 등 다양한 병태생리 기전에 관여한다.특히 유전학적 근거에 따르면, APOC3 유전자의 기능 상실(loss-of-function) 변이 보유자는 중성지방 수치가 현저히 낮고, ASCVD 발생률 및 TRL-연관 급성 췌장염 위험이 감소하는 것으로 보고되었다. 이러한 결과는 APOC3가 질환의 병태생리에 직접적 역할을 한다는 점을 뒷받침하며, 유효한 치료 표적(targetable driver) 으로 확립되는 근거가 되었다.이러한 근거를 바탕으로, APOC3 발현을 선택적으로 억제하는 RNA 기반 치료제 개발이 활발히 진행되고 있다. 대표적인 플랫폼은 antisense oligonucleotide(ASO) 와 small interfering RNA(siRNA) 로, 모두 APOC3 mRNA를 직접 표적하여 ApoC-III 단백질 합성을 감소시키는 정밀 RNA치료 전략이다.초기 ASO 제제인 volanesorsen은 FCS 환자를 대상으로 ApoC-III와 중성지방 수치를 현저히 감소시키며 치료 잠재력을 입증했으나, 혈소판감소증(thrombocytopenia) 등 안전성 문제가 임상적 활용의 제약 요인으로 작용했다. 이러한 한계를 보완하기 위해 간 표적 GalNAc 결합 기술이 적용된 2세대 ASO인 olezarsen이 개발되었으며, 보다 우수한 안전성 프로파일과 강력한 TG 감소 효과가 관찰되고 있다.동시에 siRNA 플랫폼 기반의 plozasiran(ARO-APOC3) 역시 간세포 내 APOC3 발현을 억제하는 기전으로 개발 중이다.이 차세대 APOC3 억제제들은 기존 치료에 반응이 미흡한 난치성·중증 고중성지방혈증 환자군에게 새로운 치료 대안을 제공할 뿐 아니라, TRL-잔여 위험(residual risk) 감소를 통한 심혈관질환 예방 측면에서도 잠재적 가치를 보여주고 있다. 특히 TG 감소 외에도 간·췌장 합병증 개선 가능성, 심혈관 위험 지표 개선, 대사염증 경감 효과 등이 탐색되고 있어 적용 범위가 확장될 전망이다.결론적으로, APOC3 억제제는 중성지방 대사의 근본 조절축을 정밀하게 표적하는 혁신적 RNA 기반 치료 전략으로, 고중성지방혈증, 죽상경화성 심혈관질환, TRL-연관 급성 췌장염 등 다양한 대사 및 심혈관질환 영역에서 새로운 치료 패러다임을 제시하고 있다.올레자르센의 약리적 기전은 어떠한가? 올레자르센은 표적 mRNA와 상보적으로 결합하여 RNA–DNA hybrid를 형성하고, RNase H1을 활성화해 APOC3 mRNA를 절단·분해한다. 이로써 apoC-III 단백질 발현이 감소하고, LPL 활성이 회복되며, 간으로의 TRL 잔여입자 제거가 촉진되어 혈중 중성지방 농도가 유의하게 감소한다.간세포 선택성을 강화하기 위해 5’ 말단에는 삼지형(triantennary) N-아세틸갈락토사민(GalNAc) 리간드가 결합되어 있다. 이를 통해 asialoglycoprotein receptor(ASGPR)를 매개로 한 간세포 특이적 흡수가 가능해지며, 세포내섭취(endocytosis)를 거쳐 간세포 내로 이동한 후 표적 mRNA를 분해한다.The ASO Drug Olezarsen Targets Familial Chylomicronemia Syndrome[출처: https://www.cell.com/trends/pharmacological-sciences/abstract /S0165-6147(25) 00097-5]APOC3 억제를 통한 기전은 크게 세 가지로 정리된다. 첫째, 잔존 LPL 활성(residual LPL activity)을 강화하여 중성지방 분해를 촉진하고, 둘째, 중성지방이 풍부한 지단백(TG-rich lipoprotein)의 생성과 분비를 억제하며, 셋째, LPL 비의존적 대사 경로(alternative catabolic pathways)를 활성화하여 추가적인 중성지방 감소를 유도한다.올레자르센은 5–10–5 gapmer 구조로 설계되었으며, 2’-O-methoxyethyl(2’-MOE) 수식 염기와 phosphorothioate 골격을 적용해 안정성과 결합 친화도를 높였다. 내부 DNA 서열은 RNase H1 유도를 위한 구조적 요건을 유지하며, 5-methylcytosine과 5-methyluridine의 도입은 염기쌍 안정성과 표적 결합력을 강화한다.결과적으로, 올레자르센은 APOC3 mRNA 발현을 선택적으로 억제함으로써 혈중 중성지방을 효과적으로 감소시키는 정밀 RNA 기반 치료제로, 고중성지방혈증 및 가족성 킬로미크론혈증(FCS)의 병태생리를 표적하는 혁신적 치료 옵션으로서 임상적 의의가 크다.올레잘센(TRYNGOLZA)의 허가 임상 결과는 어떠한가?TRYNGOLZA의 효능은 유전적으로 FCS이 확인된 성인 환자 중, 공복 중성지방(TG) 수치가 880mg/dL 이상인 환자를 대상으로 실시된 무작위 배정, 위약 대조, 이중맹검 임상시험(Trial 1)을 통해 입증되었다.시험에 앞서 모든 환자는 1일 지방 섭취량을 20g 이하로 제한하는 저지방 식이요법을 최소 4주 이상 유지하는 준비(run-in) 기간을 거쳤다. 이후 환자들은 무작위로 배정되어, TRYNGOLZA 80mg(n=22) 또는 동일 용량의 위약(placebo, n=23)을 피하 주사 형태로 4주 간격으로 53주간 투여받았다.환자 인구학적 및 기저 특성은 두 치료군 간 전반적으로 유사하였다 등록 시 당뇨병을 동반한 환자 비율은 TRYNGOLZA 80mg 군 32%, 위약군 26%였다.연구 시작 시 TRYNGOLZA 80mg 군과 위약군 모두에서 스타틴(27%), 오메가-3 지방산(42%), 피브레이트(49%), 또는 기타 지질강하제(13%)가 병용 사용되었다.두 군을 합쳐 71%의 환자가 과거 10년 이내에 급성 췌장염(acute pancreatitis) 병력이 있었다. 기저 시점의 공복 중성지방 평균(SD) 수치는 2,604(1,364)mg/dL, 중앙값은 2,303mg/dL이었으며, 범위는 334–6,898mg/dL이었다.1차 평가변수(primary endpoint)는 기저치 대비 6개월차(23, 25, 27주차 평균)의 공복 중성지방 변화율(%)로, 위약군과 비교하여 분석되었다.그 결과, TRYNGOLZA 80mg 투여군은 위약군 대비 공복 중성지방 변화율이 -42.5%로 유의하게 감소하였다(95% 신뢰구간: -74.1% ~ -10.9%; p = 0.0084). 추가 결과는 Table 2를 참조. 기저치 대비 중앙값 변화율(Figure 1)과 중앙값 절대 중성지방(TG) 수치(Figure 2)는, 12개월 치료 기간 동안 일관된 중성지방 감소 효과를 보여주었다. 12개월의 치료 기간 동안, TRYNGOLZA 80mg을 투여받은 환자군에서 급성 췌장염(acute pancreatitis)의 발생률은 위약군보다 낮았다.TRYNGOLZA 80mg 투여군에서는 1명(5%), 위약군에서는 7명(30%의 환자에서 급성 췌장염이 보고되었다. 이들 모든 환자는 시험 등록 10년 이내에 췌장염 병력을 가지고 있었다.올레잘센의 쟁점이 될 수 있는 부분은?올레잘센은 FCS 최초이자 유일한 치료 옵션으로, 성인 FCS 환자에서 식이요법의 보조요법으로 중성지방(TG)을 유의하게 감소시킨다. 월 1회 80 mg 피하주사라는 단순한 용법 또한 장점으로 꼽힌다. 유사 기전 약물인 volanesorsen과 plozasiran은 아직 미국 FDA 승인을 받지 못했다.올레잘센의 허가 임상은 FCS 및 중증 고중성지방혈증 환자에서 유의미한 TG 감소 효과를 입증하며 치료적 진전을 보여주었으나, 해석 시 고려해야 할 중요한 한계가 존재한다.첫째, 대부분의 임상이 소수의 환자를 대상으로 수행되어 결과의 일반화 가능성에 제약이 있다. 희귀질환 특성상 환자 모집이 어렵지만, 연구 참여자의 인종적·임상적 다양성이 충분히 확보되지 않아 실제 진료 현장에 완전히 적용하기에는 한계가 있다. 또한 평가 기간이 주로 6~12개월에 그쳐 장기 투여 시 효과 지속성 및 누적 부작용에 대한 근거가 부족하다.둘째, 유효성 평가지표로 사용된 TG 감소는 대리결과(surrogate endpoint)에 해당한다. 급성 췌장염 발생 감소, 심혈관 사건 예방, 생존율 향상과 같은 최종 임상결과(hard outcomes)에 대한 근거는 충분히 축적되지 않았다. 이는 약물의 장기적 임상적 가치 평가 측면에서 중요한 한계다.셋째, 희귀질환 치료제 특성상 높은 치료비용과 접근성 제약 문제는 실제 임상 적용과 보건의료 자원 배분에서 중요한 고려 요소로 남아 있다.종합하면, 올레잘센은 고중성지방혈증 치료 영역에서 치료적 가치를 지닌 유망한 옵션으로 부상하고 있으나, 장기 안전성, 하드엔드포인트 근거, 비용-효과성 등 해결해야 할 과제가 여전히 존재한다. 향후 충분한 규모와 이질적 환자군을 포함한 장기 추적 연구가 수행되어, 실제 진료 환경에서의 임상적 유용성과 안전성이 확립되기를 기대한다.참고문헌 1. Erica Gianazza et al. “Proteomic studies on apoB‐containing lipoprotein in cardiovascular research: A comprehensive review” Mass Spec Rev. 2023;42:1397–1423. 2. Anne V. Smith1 and Sarah J. Tabrizi “Therapeutic Antisense Targeting of Huntingtin” DNA AND CELL BIOLOGYVolume 39, Number 2, 2020). 3. Fiza Javed et al. “Familial chylomicronemia syndrome: An expert clinical review from the National Lipid Association” Journal of Clinical Lipidology, Vol 19, No 3, May/June 2025 4. Kexin Wang et al. “Remnant cholesterol and atherosclerotic cardiovascular disease: Metabolism, mechanism, evidence, and treatment” Front. Cardiovasc. Med. 9:913869. 5. Erik S. et al “Olezarsen, Acute Pancreatitis, and Familial Chylomicronemia Syndrome” N Engl J Med 2024;390:1781-1792. 6. Jan Borén et al. “The Roles of ApoC-III on the Metabolism of Triglyceride-Rich Lipoproteins in Humans“ Humans. Front. Endocrinol. 11:474 2020. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).2025-11-06 21:18:18최병철 박사 -
 향정 식욕억제제 무차별 처방한 의사 9명 적발[데일리팜=강신국 기자] 향정 식욕억제제를 무차별한 처방한 의사들과 환자들이 경찰에 적발됐다.부산경찰청은 마약류 관리에 관한 법률 위반 혐의로 의사 9명과 환자 26명 등 모두 35명을 불구속 송치했다고 6일 밝혔다.경찰에 따르면 적발된 의사들은 2023년 1월부터 2024년 10월까지 식약처의 안전사용 기준을 따르지 않고 식욕억제제 등을 체중 감량을 원하는 환자들에게 장기간에 걸쳐 처방한 혐의를 받고 있다. 의사들은 진료기록부에 명확한 진단명(진료 코드명)을 기록하지 않은 상태에서 같은 패턴으로 펜디메트라진 등의 식욕억제제를 처방해왔다.식욕억제제는 비만 치료제이기에 체질량 지수(BMI)가 30 이상이거나 고지혈증 등이 있으면서 BMI가 27 이상인 환자에게 사용하게 돼 있는데 검사도 없이 환자의 말만으로 처방전이 발급됐다. 최대 3개월 이내인 허가 용량도 지켜지지 않았다 것으로 나타났다.경찰은 식약처부터 수사를 의뢰받아 부산지역 정신건강의학과와 내과 등 병원과 의원 8곳을 상대로 압수수색을 진행한 뒤 이런 사실을 밝혀냈다.2025-11-06 10:21:23강신국
향정 식욕억제제 무차별 처방한 의사 9명 적발[데일리팜=강신국 기자] 향정 식욕억제제를 무차별한 처방한 의사들과 환자들이 경찰에 적발됐다.부산경찰청은 마약류 관리에 관한 법률 위반 혐의로 의사 9명과 환자 26명 등 모두 35명을 불구속 송치했다고 6일 밝혔다.경찰에 따르면 적발된 의사들은 2023년 1월부터 2024년 10월까지 식약처의 안전사용 기준을 따르지 않고 식욕억제제 등을 체중 감량을 원하는 환자들에게 장기간에 걸쳐 처방한 혐의를 받고 있다. 의사들은 진료기록부에 명확한 진단명(진료 코드명)을 기록하지 않은 상태에서 같은 패턴으로 펜디메트라진 등의 식욕억제제를 처방해왔다.식욕억제제는 비만 치료제이기에 체질량 지수(BMI)가 30 이상이거나 고지혈증 등이 있으면서 BMI가 27 이상인 환자에게 사용하게 돼 있는데 검사도 없이 환자의 말만으로 처방전이 발급됐다. 최대 3개월 이내인 허가 용량도 지켜지지 않았다 것으로 나타났다.경찰은 식약처부터 수사를 의뢰받아 부산지역 정신건강의학과와 내과 등 병원과 의원 8곳을 상대로 압수수색을 진행한 뒤 이런 사실을 밝혀냈다.2025-11-06 10:21:23강신국 -
 HER2 변이 비소세포폐암 경구제 '존거티닙', 희귀약 지정베링거인겔하임 [데일리팜=이탁순 기자] HER2 변이 진행성 비소세포폐암 환자 대상 최초의 경구용 표적치료제로 관심을 모으고 있는 베링거인겔하임의 '존거티닙'이 식품의약품안전처로부터 희귀의약품으로 지정됐다.희귀의약품으로 지정되면 허가 지원, 수수료 면제, 독점권 연장 등 혜택이 부여되기 때문에 정식 허가에 속도를 높일 것으로 보인다.식약처는 4일 존거티닙을 'HER2 돌연변이가 있는 진행성, 절제불가능 또는 전이성 비편평 비소세포폐암 환자의 치료' 희귀의약품으로 지정 공고했다.희귀의약품은 국내 환자 수가 2만명 이하이며, 적절한 치료 방법이나 의약품이 개발되지 않은 질환 조건을 만족해야 한다. 희귀의약품으로 지정되면 신속 상담 등 허가 지원, 제출서류 간소화, 수수료 면제, 자료보호권 10년 혜택 등이 부여된다.존거티닙은 지난 8월 '헤넥시오스'라는 제품명으로 미국FDA로부터 가속 승인을 받았다. 이전 치료 경험이 있는 HER2 변이 진행성 비소세포폐암 환자를 위한 최초의 경구용 표적치료제가 탄생한 것이다.같은 질환에 사용되는 표적치료제로는 항체약물접합체(ADC) '엔허투주(트라스투주맙 데룩스테칸, AZ-다이이찌산쿄)'가 있다. 하지만 엔허투주는 정맥주사제로, 편의성이 떨어진다는 단점이 있다. 알테오젠이 엔허투를 피하주사로 개량해 임상 연구를 진행하는 것도 이 때문이다.존거티닙은 1b상 임상시험(Beamion-LUNG 1)에서 백금착제 기반 화학항암치료를 받았으나 HER-2 표적치료제로는 치료받지 않은 71명에서 객관적반응률(ORR) 75%를 나타냈다. 또한 환자의 6%는 완전관해, 환자의 69%는 부분관해를 보였다. 반응지속기간(DOR) 중앙값이 6개월 이상인 환자 비율은 58%였다.이를 통해 FDA 패스트트랙 심사를 통해 가속 승인을 받을 수 있었다.한편, 개발단계 희귀의약품에는 한국아스트라제네카의 저인산효소증 치료제 후보 에프짐포타제알파 주사제가 추가 지정됐다.2025-11-04 18:47:47이탁순
HER2 변이 비소세포폐암 경구제 '존거티닙', 희귀약 지정베링거인겔하임 [데일리팜=이탁순 기자] HER2 변이 진행성 비소세포폐암 환자 대상 최초의 경구용 표적치료제로 관심을 모으고 있는 베링거인겔하임의 '존거티닙'이 식품의약품안전처로부터 희귀의약품으로 지정됐다.희귀의약품으로 지정되면 허가 지원, 수수료 면제, 독점권 연장 등 혜택이 부여되기 때문에 정식 허가에 속도를 높일 것으로 보인다.식약처는 4일 존거티닙을 'HER2 돌연변이가 있는 진행성, 절제불가능 또는 전이성 비편평 비소세포폐암 환자의 치료' 희귀의약품으로 지정 공고했다.희귀의약품은 국내 환자 수가 2만명 이하이며, 적절한 치료 방법이나 의약품이 개발되지 않은 질환 조건을 만족해야 한다. 희귀의약품으로 지정되면 신속 상담 등 허가 지원, 제출서류 간소화, 수수료 면제, 자료보호권 10년 혜택 등이 부여된다.존거티닙은 지난 8월 '헤넥시오스'라는 제품명으로 미국FDA로부터 가속 승인을 받았다. 이전 치료 경험이 있는 HER2 변이 진행성 비소세포폐암 환자를 위한 최초의 경구용 표적치료제가 탄생한 것이다.같은 질환에 사용되는 표적치료제로는 항체약물접합체(ADC) '엔허투주(트라스투주맙 데룩스테칸, AZ-다이이찌산쿄)'가 있다. 하지만 엔허투주는 정맥주사제로, 편의성이 떨어진다는 단점이 있다. 알테오젠이 엔허투를 피하주사로 개량해 임상 연구를 진행하는 것도 이 때문이다.존거티닙은 1b상 임상시험(Beamion-LUNG 1)에서 백금착제 기반 화학항암치료를 받았으나 HER-2 표적치료제로는 치료받지 않은 71명에서 객관적반응률(ORR) 75%를 나타냈다. 또한 환자의 6%는 완전관해, 환자의 69%는 부분관해를 보였다. 반응지속기간(DOR) 중앙값이 6개월 이상인 환자 비율은 58%였다.이를 통해 FDA 패스트트랙 심사를 통해 가속 승인을 받을 수 있었다.한편, 개발단계 희귀의약품에는 한국아스트라제네카의 저인산효소증 치료제 후보 에프짐포타제알파 주사제가 추가 지정됐다.2025-11-04 18:47:47이탁순 -
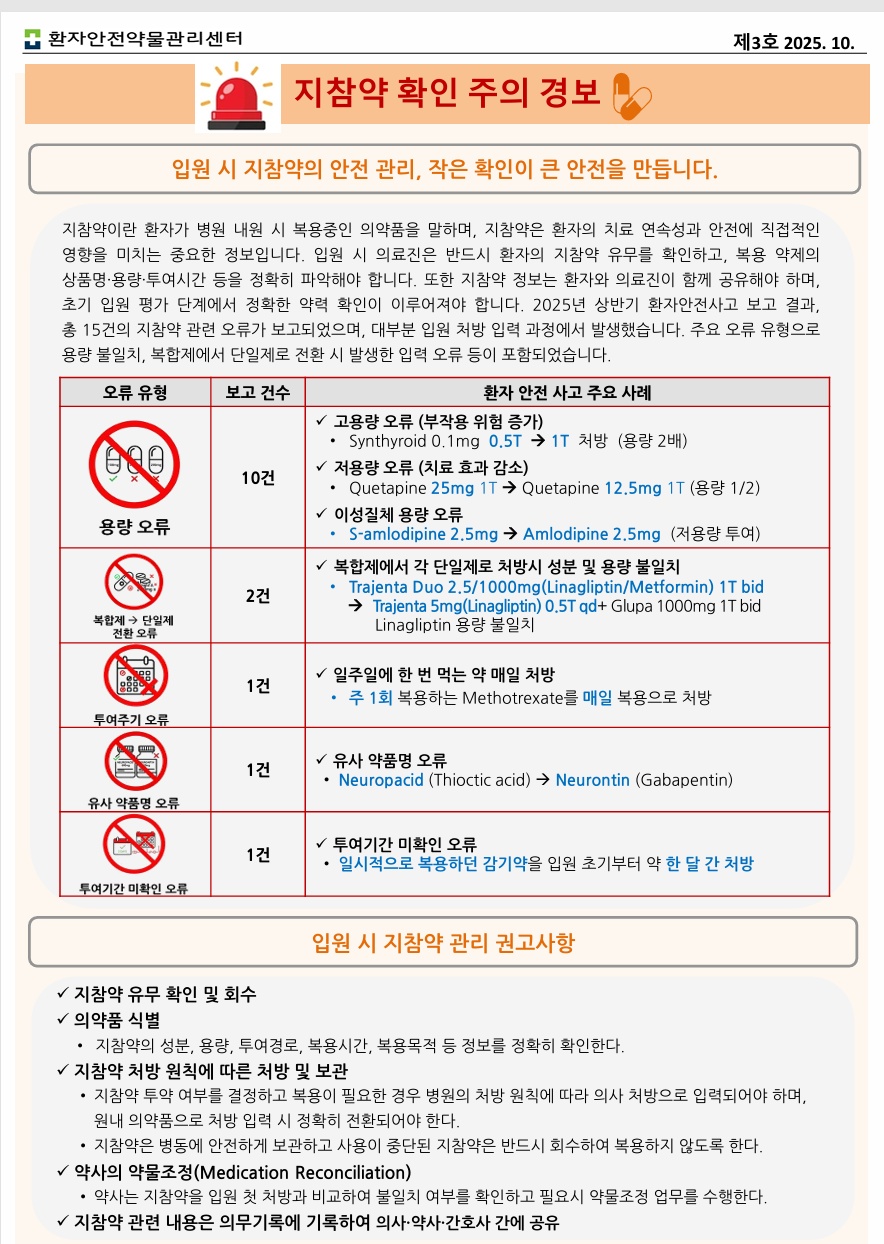 병원약사회, 환자안전약물관리센터 소식지 3호 발간[데일리팜=김지은 기자] 한국병원약사회(회장 정경주)는 4일 환자안전약물관리센터(센터장 윤정이)에서 발행한 제3호 소식지를 회원 약사들에 배포했다고 밝혔다.병원약사회는 증가하는 의약품 관련 환자안전사고 예방을 위해 지난 2023년 환자안전약물관리센터를 설립했다.센터에서는 대외적 환자안전 관련 정책 대응과 유관기관과 협력을 통해 환자 안전 활동을 강화하고, 의약품 오류 예방을 위해 제약회사와의 소통 채널 역할을 수행해 오고 있다. 작년부터는 센터 홈페이지(https://safe.kshp.or.kr)를 오픈해 소식지를 발간하는 한편 항생제 Speak Up 캠페인 포스터를 제작해 회원 약사들의 병원에 배포하는 등 전담인력배치, 환자안전활동 수행이 어려운 중소·요양병원을 비롯해 전체 회원병원들의 환자안전사고 정보공유와 홍보, 예방활동에 앞장서고 있다.센터 홈페이지의 주요 메뉴인 ‘환자안전사고 보고프로그램’은 각 병원에서 발생한 사고와 관련해 발생단계와 처방구분, 사고내용 및 원인, 개선방안 등을 제출하면 월별 보고건수와 발생단계, 사고유형의 동향을 확인할 수 있는 프로그램이다. 이번에 발행한 소식지 3호는 지난 3월부터 8월까지 6개월 간의 보고 데이터를 취합해 발간된 것이다.이번 소식지에 따르면 환자안전사고 보고 중 절반 이상인 58.6%가 조제 단계에서 발생했다. 사고유형 별 오류 빈도를 살펴보면 조제 시 약품명 오류(25%), 처방 입력 시 용법용량 오류(21.4%), 투약 및 기타에서는 누락오류(39.2%)가 제일 높은 것으로 나타났다.조치 내용으로는 재조제(50%), 처방중재(36.1%), 교육(9.3%), 주치의 보고 및 약품명 변경 등(4.6%) 순이었다.한편 이번 소식지 내 ‘지참약 확인 주의 경보’ 코너에서는 2025년 상반기 환자안전사고 보고 결과 드러난 총 15건의 지참약 관련 오류 사례가 담겼다. 주로 지참약을 확인하고 입원처방으로 입력 과정에서 처방 불일치 오류가 발생했으며 주요 오류 유형은 용량 불일치, 복합제에서 단일제로 전환시 불일치 등이었다. 권고사항으로는 ▲지참약 유무 확인 및 회수 ▲의약품 식별 ▲지참약 처방 원칙에 따른 처방 및 보관 ▲약사의 약물조정 등이 제시됐다.이어 조선대병원과 서울대병원의 지참약 처방 입력 오류 예방을 위한 병원 업무 사례도 실렸다.윤정이 센터장은 “센터에서 발간되는 소식지를 통해 환자안전사고의 예방과 재발 방지에 도움이 될 수 있길 바란다”며 “센터에서는 주사 마약류 포장개선, 의약품 포장개선을 비롯해 현재 추진중인 수액/TPN(고영양수액) 유효기한 표기 개선 등 회원 병원의 공통적인 개선사항을 제약사에 요구해 개선해 나가고 있다”고 말했다.2025-11-04 10:24:07김지은
병원약사회, 환자안전약물관리센터 소식지 3호 발간[데일리팜=김지은 기자] 한국병원약사회(회장 정경주)는 4일 환자안전약물관리센터(센터장 윤정이)에서 발행한 제3호 소식지를 회원 약사들에 배포했다고 밝혔다.병원약사회는 증가하는 의약품 관련 환자안전사고 예방을 위해 지난 2023년 환자안전약물관리센터를 설립했다.센터에서는 대외적 환자안전 관련 정책 대응과 유관기관과 협력을 통해 환자 안전 활동을 강화하고, 의약품 오류 예방을 위해 제약회사와의 소통 채널 역할을 수행해 오고 있다. 작년부터는 센터 홈페이지(https://safe.kshp.or.kr)를 오픈해 소식지를 발간하는 한편 항생제 Speak Up 캠페인 포스터를 제작해 회원 약사들의 병원에 배포하는 등 전담인력배치, 환자안전활동 수행이 어려운 중소·요양병원을 비롯해 전체 회원병원들의 환자안전사고 정보공유와 홍보, 예방활동에 앞장서고 있다.센터 홈페이지의 주요 메뉴인 ‘환자안전사고 보고프로그램’은 각 병원에서 발생한 사고와 관련해 발생단계와 처방구분, 사고내용 및 원인, 개선방안 등을 제출하면 월별 보고건수와 발생단계, 사고유형의 동향을 확인할 수 있는 프로그램이다. 이번에 발행한 소식지 3호는 지난 3월부터 8월까지 6개월 간의 보고 데이터를 취합해 발간된 것이다.이번 소식지에 따르면 환자안전사고 보고 중 절반 이상인 58.6%가 조제 단계에서 발생했다. 사고유형 별 오류 빈도를 살펴보면 조제 시 약품명 오류(25%), 처방 입력 시 용법용량 오류(21.4%), 투약 및 기타에서는 누락오류(39.2%)가 제일 높은 것으로 나타났다.조치 내용으로는 재조제(50%), 처방중재(36.1%), 교육(9.3%), 주치의 보고 및 약품명 변경 등(4.6%) 순이었다.한편 이번 소식지 내 ‘지참약 확인 주의 경보’ 코너에서는 2025년 상반기 환자안전사고 보고 결과 드러난 총 15건의 지참약 관련 오류 사례가 담겼다. 주로 지참약을 확인하고 입원처방으로 입력 과정에서 처방 불일치 오류가 발생했으며 주요 오류 유형은 용량 불일치, 복합제에서 단일제로 전환시 불일치 등이었다. 권고사항으로는 ▲지참약 유무 확인 및 회수 ▲의약품 식별 ▲지참약 처방 원칙에 따른 처방 및 보관 ▲약사의 약물조정 등이 제시됐다.이어 조선대병원과 서울대병원의 지참약 처방 입력 오류 예방을 위한 병원 업무 사례도 실렸다.윤정이 센터장은 “센터에서 발간되는 소식지를 통해 환자안전사고의 예방과 재발 방지에 도움이 될 수 있길 바란다”며 “센터에서는 주사 마약류 포장개선, 의약품 포장개선을 비롯해 현재 추진중인 수액/TPN(고영양수액) 유효기한 표기 개선 등 회원 병원의 공통적인 개선사항을 제약사에 요구해 개선해 나가고 있다”고 말했다.2025-11-04 10:24:07김지은 -
 K-바이오 호재일까…FDA, 시밀러 진입 장벽 완화 추진[데일리팜=차지현 기자] 미국 규제당국이 바이오시밀러를 더 빠르고 저렴하게 개발할 수 있도록 하는 대규모 제도 개편에 착수했다. 비교 임상을 줄이거나 면제하고, 약국 단계에서 바이오시밀러 대체 처방을 가능하도록 허용하는 게 핵심이다.31일 바이오 업계에 따르면 미국 식품의약국(FDA)은 29일(현지 시각) 바이오시밀러 승인 절차를 대폭 간소화한다고 발표했다. 해당 지침은 2015년 첫 바이오시밀러 승인 이후 축적된 데이터와 경험을 반영해 불필요한 임상시험을 줄이고 개발 효율성을 높이는 게 골자다.새 지침에 따르면 바이오시밀러 개발사는 사람 대상 임상시험 대신, 세포 실험으로도 약효 차이를 입증할 수 있다. 기존에는 오리지널 약과 번갈아 투여해 동등성을 확인하는 교차 투여 시험을 진행해야 했으나 앞으로는 이런 절차가 대부분 생략될 예정이다.동물 독성시험이나 면역 반응 시험, 효능 시험 등도 대부분 폐지되거나 면제된다. 다른 국가의 기준으로 만든 의약품이라도 동일성만 입증되면 미국에서도 인허가를 받을 수 있다. FDA의 최종 지침은 3개월~6개월 후에 발표될 것으로 점쳐진다.FDA는 "새로운 지침 초안에서 FDA는 바이오시밀러의 유사성 입증 연구를 단순화하고 불필요한 임상 시험을 줄이는 주요 개정안을 제안했다"면서 "별도 이니셔티브를 통해 바이오시밀러가 오리지널 의약품과 상호대체 가능한 형태로 개발되도록 절차를 간소화할 계획"이라고 했다.이번 조치는 도널드트럼프 미국 대통령이 추진한 약가 인하 정책의 일환이다. 앞서 트럼프 대통령은 지난 4월 제네릭 의약품과 바이오시밀러 승인 절차를 간소화하는 행정명령에 서명한 바 있다. 오리지널 의약품의 복제약 도입을 확대해 국민의 약값 부담을 낮추겠다는 얘기다. FDA는 이번 지침 개편으로 환자와 약사가 보다 쉽게 저비용 대체 의약품을 선택할 수 있도록 돕겠다는 구상이다.FDA는 "고가 생물학적 의약품이 미국 전체 처방의 5%에 불과하지만 전체 의약품 지출의 51%(2024년 기준)를 차지한다"면서도 "반면 FDA가 승인한 바이오시밀러는 오리지널 의약품과 동일한 수준의 안전성과 효능을 지니고 있음에도 시장 점유율은 여전히 20% 미만에 머물러 있다"고 했다.FDA에 따르면 지금까지 76개의 바이오시밀러가 품목허가를 획득했다. 그러나 특허 만료를 앞둔 오리지널 의약품 중 실제 바이오시밀러로 개발이 진행 중인 건 10%에 불과하다. 매출 5억 달러 이상인 고부가 바이오의약품의 27% 수준의 바이오시밀러도 개발이 진행되고 있지 않다는 게 FDA 측 설명이다.특히 FDA는 시장 진입을 막는 복잡한 승인 절차를 간소화함으로써 개발비를 최대 90%까지 줄일 수 있을 것으로 내다봤다. 기존에는 비교 임상시험에만 평균 1~3년, 약 2400만 달러의 시간과 비용이 들었다. 그러나 실제로는 약효 차이를 가려내는 정확도가 낮아 비효율적이었다는 지적이 있었다.마티 마카리 FDA 국장은 "바이오시밀러 개발 프로세스를 간소화하고 호환성을 발전시킴으로써 수백만 명의 미국인에게 영향을 미치는 암, 자가면역 질환과 희귀 질환에 대한 첨단 치료제에 대한 비용을 크게 절감할 수 있다"라고 했다.업계에서는 이 같은 정책 변화가 국내 기업에게도 호재로 작용할 것이라는 전망도 나온다. 승인 절차가 단축되면 삼성바이오에피스와 셀트리온 등 미국 시장에 바이오시밀러를 출시, 판매 중인 국내사의 임상 부담이 줄고 제품 개발 속도를 높일 수 있을 것이라는 기대다.일각에서는 진입장벽이 낮아지면서 바이오시밀러 시장의 경쟁이 더욱 심화할 것이라는 우려도 제기된다. 높은 임상 비용 등 부담으로 시장에 진입하지 못했던 신규 플레이어가 대거 증가하면서 시장 내 가격 경쟁을 가속화할 수 있다는 시각이다.2025-10-31 12:00:23차지현
K-바이오 호재일까…FDA, 시밀러 진입 장벽 완화 추진[데일리팜=차지현 기자] 미국 규제당국이 바이오시밀러를 더 빠르고 저렴하게 개발할 수 있도록 하는 대규모 제도 개편에 착수했다. 비교 임상을 줄이거나 면제하고, 약국 단계에서 바이오시밀러 대체 처방을 가능하도록 허용하는 게 핵심이다.31일 바이오 업계에 따르면 미국 식품의약국(FDA)은 29일(현지 시각) 바이오시밀러 승인 절차를 대폭 간소화한다고 발표했다. 해당 지침은 2015년 첫 바이오시밀러 승인 이후 축적된 데이터와 경험을 반영해 불필요한 임상시험을 줄이고 개발 효율성을 높이는 게 골자다.새 지침에 따르면 바이오시밀러 개발사는 사람 대상 임상시험 대신, 세포 실험으로도 약효 차이를 입증할 수 있다. 기존에는 오리지널 약과 번갈아 투여해 동등성을 확인하는 교차 투여 시험을 진행해야 했으나 앞으로는 이런 절차가 대부분 생략될 예정이다.동물 독성시험이나 면역 반응 시험, 효능 시험 등도 대부분 폐지되거나 면제된다. 다른 국가의 기준으로 만든 의약품이라도 동일성만 입증되면 미국에서도 인허가를 받을 수 있다. FDA의 최종 지침은 3개월~6개월 후에 발표될 것으로 점쳐진다.FDA는 "새로운 지침 초안에서 FDA는 바이오시밀러의 유사성 입증 연구를 단순화하고 불필요한 임상 시험을 줄이는 주요 개정안을 제안했다"면서 "별도 이니셔티브를 통해 바이오시밀러가 오리지널 의약품과 상호대체 가능한 형태로 개발되도록 절차를 간소화할 계획"이라고 했다.이번 조치는 도널드트럼프 미국 대통령이 추진한 약가 인하 정책의 일환이다. 앞서 트럼프 대통령은 지난 4월 제네릭 의약품과 바이오시밀러 승인 절차를 간소화하는 행정명령에 서명한 바 있다. 오리지널 의약품의 복제약 도입을 확대해 국민의 약값 부담을 낮추겠다는 얘기다. FDA는 이번 지침 개편으로 환자와 약사가 보다 쉽게 저비용 대체 의약품을 선택할 수 있도록 돕겠다는 구상이다.FDA는 "고가 생물학적 의약품이 미국 전체 처방의 5%에 불과하지만 전체 의약품 지출의 51%(2024년 기준)를 차지한다"면서도 "반면 FDA가 승인한 바이오시밀러는 오리지널 의약품과 동일한 수준의 안전성과 효능을 지니고 있음에도 시장 점유율은 여전히 20% 미만에 머물러 있다"고 했다.FDA에 따르면 지금까지 76개의 바이오시밀러가 품목허가를 획득했다. 그러나 특허 만료를 앞둔 오리지널 의약품 중 실제 바이오시밀러로 개발이 진행 중인 건 10%에 불과하다. 매출 5억 달러 이상인 고부가 바이오의약품의 27% 수준의 바이오시밀러도 개발이 진행되고 있지 않다는 게 FDA 측 설명이다.특히 FDA는 시장 진입을 막는 복잡한 승인 절차를 간소화함으로써 개발비를 최대 90%까지 줄일 수 있을 것으로 내다봤다. 기존에는 비교 임상시험에만 평균 1~3년, 약 2400만 달러의 시간과 비용이 들었다. 그러나 실제로는 약효 차이를 가려내는 정확도가 낮아 비효율적이었다는 지적이 있었다.마티 마카리 FDA 국장은 "바이오시밀러 개발 프로세스를 간소화하고 호환성을 발전시킴으로써 수백만 명의 미국인에게 영향을 미치는 암, 자가면역 질환과 희귀 질환에 대한 첨단 치료제에 대한 비용을 크게 절감할 수 있다"라고 했다.업계에서는 이 같은 정책 변화가 국내 기업에게도 호재로 작용할 것이라는 전망도 나온다. 승인 절차가 단축되면 삼성바이오에피스와 셀트리온 등 미국 시장에 바이오시밀러를 출시, 판매 중인 국내사의 임상 부담이 줄고 제품 개발 속도를 높일 수 있을 것이라는 기대다.일각에서는 진입장벽이 낮아지면서 바이오시밀러 시장의 경쟁이 더욱 심화할 것이라는 우려도 제기된다. 높은 임상 비용 등 부담으로 시장에 진입하지 못했던 신규 플레이어가 대거 증가하면서 시장 내 가격 경쟁을 가속화할 수 있다는 시각이다.2025-10-31 12:00:23차지현 -
 자누비아 제네릭 점유율 23%…경보·한미만 두각[데일리팜=김진구 기자] DPP-4 억제제 계열 당뇨병 치료제 ‘자누비아(시타글립틴)’ 시리즈의 제네릭 제품들이 발매 2년 만에 점유율을 23%로 확대했다. 다만 시장 침투 속도는 기존 테넬리아(테네리글립틴)·가브스(빌다글립틴) 사례와 비교해 더디다는 분석이다.제네릭 제품간 희비가 교차하는 것으로 나타났다. 대부분 제네릭이 분기처방액 1억원 미만 처방액을 기록 중인 가운데, 경보제약과 한미약품은 10억원 이상의 실적을 내며 입지를 다지고 있다.자누비아 제네릭 발매 2년 점유율 23%…시장 침투 속도↓29일 의약품 시장조사기관 유비스트에 따르면 올해 3분기 시타글립틴 단일제와 시타글립틴·메트포르민 복합제의 원외처방 규모는 283억원이다. 작년 3분기 302억원 대비 6% 감소했다.오리지널은 감소한 반면 제네릭은 증가했다. 오리지널 제품인 자누비아·자누메트·자누메트엑스알의 처방실적은 작년 3분기 251억원에서 올해 3분기 217억원으로 14% 감소했다. 자누비아는 58억원에서 45억원으로, 자누메트와 자누메트엑스알은 193억원에서 172억원으로 각각 줄었다.제네릭 발매 이후론 꾸준히 하락세다. 특허 만료 직전인 2023년 2분기 375억원이던 자누비아 시리즈의 처방실적은 제네릭이 본격 가세한 2023년 4분기 266억원으로 줄었고, 올해 3분기엔 이보다 18% 더 감소했다. 반면 제네릭 제품들은 1년 새 합산 처방실적이 51억원에서 66억원으로 30% 증가했다. 자누비아 제네릭은 16억원에서 19억원으로, 자누메트·자누메트엑스알 제네릭은 35억원에서 47억원으로 각각 늘었다.자누비아 제네릭은 2023년 9월 발매됐다. 연 6000억원 규모의 DPP-4 억제제 시장에서 처방 선두를 오랜 기간 유지한 제품의 특허 만료에 많은 제네릭사가 도전장을 냈다. 총 89개 업체가 제네릭을 허가받았고, 이 가운데 60개 업체가 제품을 발매했다.전체 시장에서의 제네릭 점유율은 1년 새 17%에서 23%로 확대됐다. 다만 시장 침투 속도는 테넬리아·가브스 등 다른 DPP-4 억제제 제네릭의 사례와 비교해 다소 더디다는 평가다.가브스·가브스메트 제네릭의 경우 발매 1년차에 점유율 42%를 기록한 바 있다. 2년차에는 47%로 오리지널과 비슷한 수준으로 점유율을 더욱 확대했다. 테넬리아·테넬리아엠 제네릭의 경우 발매 1년차에 54%의 점유율로 이미 오리지널을 넘어섰다. 2년차엔 58%로 더욱 높아졌다.한미·경보 껑충…나머지 업체는 대부분 분기처방액 3억원 미만제네릭 업체간 희비가 교차하는 모습이다. 분기 처방액 10억원 이상인 업체는 2곳뿐이고, 나머지 대부분 업체는 1억원에도 못 미치는 실적을 기록했다.경보제약은 ‘자누스틴메트’와 ‘자누스틴엑스알’ 등 복합제 제네릭 2개로 올해 3분기 11억원의 처방실적을 냈다. 작년 3분기 6억원 대비 약 2배 증가했다. 두 제품의 누적 처방실적은 49억원이다.한미약품의 ‘시타’와 ‘시타메트엑스알’은 전년대비 25% 증가한 10억원의 처방실적을 기록했다. 발매 이후 누적 처방액은 58억원에 달한다.반면 대부분 제네릭 제품은 저조한 성적을 내고 있다. 제품을 발매한 60개 업체 가운데 41개 업체(68%)의 3분기 처방실적이 1억원에 못 미친다. 또한 15개 업체(25%)는 분기 처방실적이 3억원 미만이다. 3분기 기준 업체 1곳당 평균 처방실적은 1.1억원 수준이다. 자누비아 제네릭 제품들이 영향력 확대에 어려움을 겪는 이유로 이미 DPP-4 억제제 계열 당뇨병 치료제 시장이 포화 상태라는 점이 꼽힌다.이 시장에선 자누비아 시리즈 외에도 제미글로, 트라젠타, 테넬리아, 슈가논, 가브스, 온글라이자, 네시나, 가드렛 등 오리지널 제품이 경쟁 중이다. 이 가운데 가브스와 테넬리아, 트라젠타의 경우 특허 만료 이후로 제네릭까지 경쟁에 합류한 상태다.또한 DPP-4 억제제 시장은 포시가·자디앙 등 SGLT-2 억제제 계열 당뇨병 치료제가 등장한 이후로 전체 처방실적이 감소세다. 이런 상황에서 무더기로 등장한 자누비아·자누메트 제네릭이 치열한 경쟁을 펼치면서 기대에 미치지 못하는 성적을 내고 있다는 분석이다.DPP-4 억제제 시장 분석2025-10-30 06:20:10김진구
자누비아 제네릭 점유율 23%…경보·한미만 두각[데일리팜=김진구 기자] DPP-4 억제제 계열 당뇨병 치료제 ‘자누비아(시타글립틴)’ 시리즈의 제네릭 제품들이 발매 2년 만에 점유율을 23%로 확대했다. 다만 시장 침투 속도는 기존 테넬리아(테네리글립틴)·가브스(빌다글립틴) 사례와 비교해 더디다는 분석이다.제네릭 제품간 희비가 교차하는 것으로 나타났다. 대부분 제네릭이 분기처방액 1억원 미만 처방액을 기록 중인 가운데, 경보제약과 한미약품은 10억원 이상의 실적을 내며 입지를 다지고 있다.자누비아 제네릭 발매 2년 점유율 23%…시장 침투 속도↓29일 의약품 시장조사기관 유비스트에 따르면 올해 3분기 시타글립틴 단일제와 시타글립틴·메트포르민 복합제의 원외처방 규모는 283억원이다. 작년 3분기 302억원 대비 6% 감소했다.오리지널은 감소한 반면 제네릭은 증가했다. 오리지널 제품인 자누비아·자누메트·자누메트엑스알의 처방실적은 작년 3분기 251억원에서 올해 3분기 217억원으로 14% 감소했다. 자누비아는 58억원에서 45억원으로, 자누메트와 자누메트엑스알은 193억원에서 172억원으로 각각 줄었다.제네릭 발매 이후론 꾸준히 하락세다. 특허 만료 직전인 2023년 2분기 375억원이던 자누비아 시리즈의 처방실적은 제네릭이 본격 가세한 2023년 4분기 266억원으로 줄었고, 올해 3분기엔 이보다 18% 더 감소했다. 반면 제네릭 제품들은 1년 새 합산 처방실적이 51억원에서 66억원으로 30% 증가했다. 자누비아 제네릭은 16억원에서 19억원으로, 자누메트·자누메트엑스알 제네릭은 35억원에서 47억원으로 각각 늘었다.자누비아 제네릭은 2023년 9월 발매됐다. 연 6000억원 규모의 DPP-4 억제제 시장에서 처방 선두를 오랜 기간 유지한 제품의 특허 만료에 많은 제네릭사가 도전장을 냈다. 총 89개 업체가 제네릭을 허가받았고, 이 가운데 60개 업체가 제품을 발매했다.전체 시장에서의 제네릭 점유율은 1년 새 17%에서 23%로 확대됐다. 다만 시장 침투 속도는 테넬리아·가브스 등 다른 DPP-4 억제제 제네릭의 사례와 비교해 다소 더디다는 평가다.가브스·가브스메트 제네릭의 경우 발매 1년차에 점유율 42%를 기록한 바 있다. 2년차에는 47%로 오리지널과 비슷한 수준으로 점유율을 더욱 확대했다. 테넬리아·테넬리아엠 제네릭의 경우 발매 1년차에 54%의 점유율로 이미 오리지널을 넘어섰다. 2년차엔 58%로 더욱 높아졌다.한미·경보 껑충…나머지 업체는 대부분 분기처방액 3억원 미만제네릭 업체간 희비가 교차하는 모습이다. 분기 처방액 10억원 이상인 업체는 2곳뿐이고, 나머지 대부분 업체는 1억원에도 못 미치는 실적을 기록했다.경보제약은 ‘자누스틴메트’와 ‘자누스틴엑스알’ 등 복합제 제네릭 2개로 올해 3분기 11억원의 처방실적을 냈다. 작년 3분기 6억원 대비 약 2배 증가했다. 두 제품의 누적 처방실적은 49억원이다.한미약품의 ‘시타’와 ‘시타메트엑스알’은 전년대비 25% 증가한 10억원의 처방실적을 기록했다. 발매 이후 누적 처방액은 58억원에 달한다.반면 대부분 제네릭 제품은 저조한 성적을 내고 있다. 제품을 발매한 60개 업체 가운데 41개 업체(68%)의 3분기 처방실적이 1억원에 못 미친다. 또한 15개 업체(25%)는 분기 처방실적이 3억원 미만이다. 3분기 기준 업체 1곳당 평균 처방실적은 1.1억원 수준이다. 자누비아 제네릭 제품들이 영향력 확대에 어려움을 겪는 이유로 이미 DPP-4 억제제 계열 당뇨병 치료제 시장이 포화 상태라는 점이 꼽힌다.이 시장에선 자누비아 시리즈 외에도 제미글로, 트라젠타, 테넬리아, 슈가논, 가브스, 온글라이자, 네시나, 가드렛 등 오리지널 제품이 경쟁 중이다. 이 가운데 가브스와 테넬리아, 트라젠타의 경우 특허 만료 이후로 제네릭까지 경쟁에 합류한 상태다.또한 DPP-4 억제제 시장은 포시가·자디앙 등 SGLT-2 억제제 계열 당뇨병 치료제가 등장한 이후로 전체 처방실적이 감소세다. 이런 상황에서 무더기로 등장한 자누비아·자누메트 제네릭이 치열한 경쟁을 펼치면서 기대에 미치지 못하는 성적을 내고 있다는 분석이다.DPP-4 억제제 시장 분석2025-10-30 06:20:10김진구













![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
