㉖ 최초 원발성 lgA 신병증 항체치료제 '시베프렌리맙'
- 최병철 박사
- 2026-04-17 06:00:53
-
가
- 가
- 가
- 가
- 가
- 가
- 최병철 박사의 노벨드럭 인사이트
- 최초의 APRIL 표적치료제로서 전환점 제시
- 장기적 신기능 보존 근거 제한적...추적 연구 입증 필요
- PR
- 전국 지역별 의원·약국 매출&상권&입지를 무료로 검색하세요!!
- 데일리팜맵 바로가기

보이작트(VoyxactⓇ, 성분명: 시베프렌리맙, sibeprenlimab-szsi, 오츠카)는 출혈 및 염증을 유발할 수 있는 자가항체 생성을 촉진하는 APRIL(A proliferation-inducing ligand)을 차단하는 약제다. 2025년 11월 미국 FDA로부터 성인 1차성 면역글로불린 A 신병증(IgA nephropathy, IgAN) 환자에서 요단백 감소 적응증으로 승인되었다.
IgAN은 면역글로불린 A(IgA)가 신장에 축적되는 진행성 면역매개성 만성 신질환이다. IgA는 정상적으로 면역 체계의 구성 요소이나, 과도하게 축적될 경우 신장 염증을 유발하고 시간이 경과함에 따라 신장 조직의 섬유화를 초래한다. 이 질환은 주로 20~40세 성인에서 발병하며, 상당수 환자에서 평생에 걸쳐 말기 신부전(end-stage kidney disease, ESKD)으로 진행할 수 있다.
최근 IgAN 치료 옵션으로는 부데소나이드(budesonide) 성분의 타르페요(TarpeyoⓇ), endothelin type A receptor와 angiotensin II receptor를 동시에 차단하는 필스파리(FilspariⓇ, sparsentan), 보체 alternative pathway의 핵심 구성 요소인 factor B를 선택적으로 억제하는 경구용 소분자 약제 파브할타(FabhaltaⓇ, iptacopan), 그리고 선택적 endothelin A receptor antagonist인 반라피아(VanrafiaⓇ, atrasentan) 등이 있다.
시베프렌리맙은 IgAN 발병 기전의 4단계 과정에서 핵심적인 역할을 하는 APRIL에 선택적으로 결합하여 그 생물학적 활성을 차단하는 인간화 IgG2 단클론 항체이다.
시베프렌리맙의 허가 임상시험인 VISIONARY는 다국가, 무작위배정, 이중눈가림, 위약대조 3상 연구로 설계되었다. 생검으로 확진된 성인 IgAN 환자를 대상으로 시베프렌리맙 400 mg을 4주 간격으로 피하 투여하였으며, 대조군에는 동일한 방식으로 위약을 투여하였다.
모든 환자는 최대 내약 용량의 ACE 억제제(ACEi) 또는 안지오텐신 수용체 차단제(ARB)를 기반으로 한 표준 치료를 유지하였고, 일부 환자에서는 SGLT2 억제제를 병용하였다. 1차 평가변수는 9개월 시점에서 24시간 요단백/크레아티닌 비(uPCR)의 기저치 대비 변화였으며, 주요 2차 평가변수는 24개월 동안의 연간 추정 사구체여과율(eGFR) 감소 기울기였다.
9개월 시점에서 24시간 uPCR은 시베프렌리맙군에서 기저 대비 50.2% 감소한 반면, 위약군에서는 2.1% 증가하였다. 이에 따른 위약 보정 치료 효과는 51.2% 감소였으며, 96.5% 신뢰구간은 42.9%~58.2%로 나타났고, 통계적으로 유의한 결과를 보여(P<0.0001) 1차 평가변수를 충족하였다.
NEJM 초록 및 학회 발표 자료에 따르면, 시베프렌리맙은 단백뇨 감소뿐 아니라 혈뇨 개선, 단백뇨 관해, Gd-IgA1 및 APRIL 관련 생체지표에서도 긍정적인 경향을 보였다. 추가 분석에서는 단백뇨 관해(<0.5 g/day)가 시베프렌리맙군 34.3%, 위약군 12.7%로 나타났으며, 혈뇨 소실은 각각 80%와 31%로 보고되었다.
전반적인 안전성 프로파일은 양호하였다. 치료 중 이상반응(treatment-emergent adverse events, TEAE)은 시베프렌리맙군에서 76.3%, 위약군에서 84.5% 발생하였으며, 중대한 이상반응은 각각 3.9%와 5.4%였다. 이상반응으로 인한 치료 중단은 각각 0.7%와 2.4%에서 발생하였고, 사망 사례는 보고되지 않았다.
가장 흔한 이상반응은 상기도 감염, 주사부위 통증 및 홍반, COVID-19, 비인두염 등이었다. 회사 발표에 따르면, 10% 이상 발생하면서 위약군보다 빈도가 높았던 이상반응은 감염(49% vs 45%)과 주사부위 반응(24% vs 23%)이었다.
면역글로불린 A 신병증(IgA nephropathy, IgAN)은 무엇인가?
면역글로불린 A 신병증(IgAN)은 갈락토스 결핍 IgA1(galactose-deficient IgA1, Gd-IgA1)과 이에 대한 자가항체를 포함하는 면역복합체가 사구체 간질에 침착되는 것을 특징으로 하는, 전 세계적으로 가장 흔한 원발성 사구체신염이다. 그러나 실제 유병률은 의료 접근성, 데이터 수집의 질, 선별 검사 방식, 신장 생검 시행 기준의 차이 등으로 인해 정확히 규명되지 않았으며, 이러한 요인들로 인해 추정치에 편차가 존재한다.
유전적 요인은 지역 및 민족 간 유병률 차이에 중요한 영향을 미치는 것으로 알려져 있다. 북미에서는 IgAN이 생검으로 확진된 원발성 사구체신염의 약 10~20%를 차지하는 반면, 유럽에서는 20~30%, 동아시아에서는 40~50%까지 보고된다. 다국가 연구에 따르면 성인의 연간 발생률은 인구 10만 명당 최소 2.5건으로 추정된다.
IgAN은 수년에 걸쳐 신기능이 점진적으로 저하되는 만성 질환으로, 상당한 이환율과 사망률을 동반한다. 전체 환자의 약 25~50%는 진단 후 10~20년 이내에 신부전으로 진행한다. 특히 이 질환은 주로 젊은 성인에서 발병하기 때문에, 최적의 보존적 치료에도 불구하고 상당수 환자가 생애 동안 신부전을 경험하게 되며, 이에 따른 노동력 손실과 사회경제적 부담이 증가한다.
고령 환자의 경우 고혈압, 당뇨병, 심혈관 질환 등의 동반 질환을 동반할 가능성이 높으며, 이는 IgAN에 의한 신장 손상을 악화시키고 치료를 복잡하게 만든다. 또한 이러한 동반 질환이 있는 환자에서 진단이 지연될 경우 신장 예후가 악화되고 심혈관 사건의 위험도 증가한다. IgAN 환자의 기대 수명은 일반 인구 대비 평균 약 6년 감소하는 것으로 보고되며, 이는 주로 신부전 관련 합병증에 기인한다.
임상적으로 IgAN은 미세혈뇨에서 육안적 혈뇨에 이르기까지 다양한 양상을 보이며, 단백뇨의 정도는 신기능 저하의 중요한 결정 인자로 작용한다. 일부 환자에서는 급속 진행성 사구체신염과 같은 중증 형태로 나타나기도 한다.
확진을 위해서는 신장 생검이 필요하며, 사구체 내 IgA의 우세한 침착이 관찰되고, 흔히 IgG 및/또는 IgM이 동반된다. 또한 90% 이상의 환자에서 보체 C3가 IgA와 함께 검출되어 보체 활성화를 시사한다. 이러한 보체 활성화는 주로 대체 경로 또는 렉틴 경로를 통해 매개되며, 사구체 염증 및 손상의 핵심 기전으로 작용한다.
옥스퍼드 분류(Oxford classification)는 질환 진행 위험과 독립적으로 연관된 조직학적 지표를 제시하며, 여기에는 사구체간세포 증식(mesangial hypercellularity), 내피세포 증식(endocapillary hypercellularity), 분절성 사구체경화증(segmental glomerulosclerosis), 세뇨관 위축 및 간질 섬유증(tubular atrophy/interstitial fibrosis), 초승달 모양 병변(crescents)이 포함된다.
Gd-IgA1의 침착, 보체 활성화, 사구체 손상 간의 상호작용에 대한 이해는 IgAN의 병태생리를 규명하고 새로운 치료 표적을 개발하는 데 중요한 근거를 제공한다. 단백뇨는 신기능 저하를 예측하는 가장 중요한 조절 가능한 위험 인자이며, 순환하는 Gd-IgA1 및 항 Gd-IgA1 자가항체의 농도가 높을수록 신기능 저하 속도가 빠르고 말기 신부전으로 진행할 위험이 증가한다.
갈락토스 결핍 IgA1(Galactose-deficient IgA1, Gd-IgA1)는 무엇인가?
IgA는 IgA1과 IgA2의 두 가지 아형으로 구성되며, 이 중 IgA 신병증(IgAN)의 병인에는 주로 IgA1이 관여한다. 특히 IgA1은 hinge region에 존재하는 당쇄(glycosylation)에 이상이 발생한 형태로 생성되며, 이러한 비정상 IgA1은 자가항체와 결합하여 면역복합체를 형성한다. 형성된 면역복합체는 사구체 내 모세혈관을 지지하는 구조인 메산지움(mesangium)에 선택적으로 침착되어 염증 반응과 신장 손상을 유도한다.
반면 IgA2는 주로 장 점막에서 생성되며, 구조적으로 hinge region이 짧아 당쇄 이상이 발생할 가능성이 상대적으로 낮다. 이에 따라 IgAN의 병인에는 거의 관여하지 않는 것으로 알려져 있다.
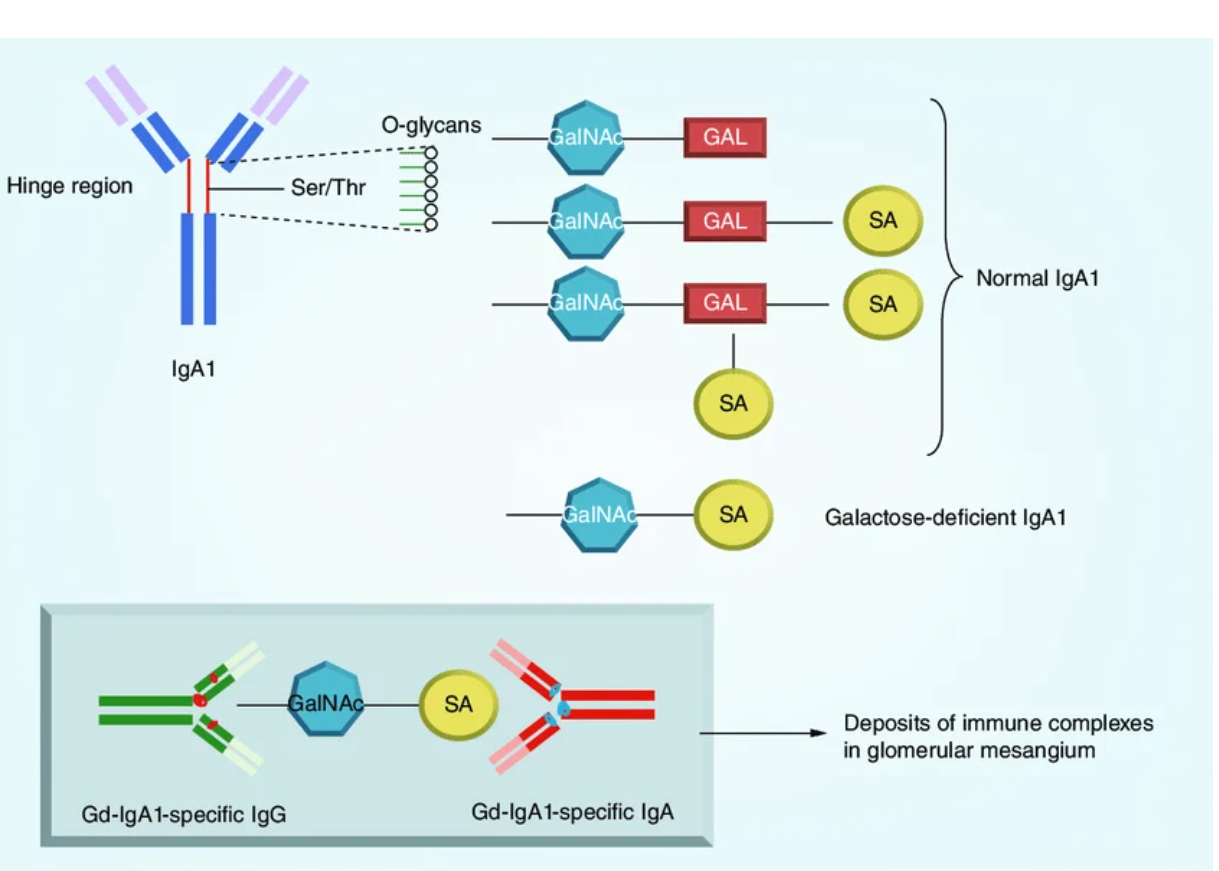
IgA1의 hinge region은 세린(serine)과 트레오닌(threonine) 잔기로 구성되어 있으며, 이들 아미노산의 수산기(-OH)에 O-당화(O-glycosylation)가 일어난다. 정상적인 당화 과정에서는 먼저 N-아세틸갈락토사민(N-acetylgalactosamine, GalNAc)이 결합한 후 갈락토스(galactose, Gal)가 순차적으로 추가된다. 이후 시알산(sialic acid, SA)은 갈락토스 또는 GalNAc에 결합할 수 있으며, 이러한 과정은 IgA1의 구조적 안정성과 기능 유지에 필수적이다.
그러나 IgAN 환자에서는 IgA1의 당화 과정에서 갈락토스 결핍이 발생하며, 이로 인해 시알산이 갈락토스 대신 GalNAc에 결합하게 된다. 그 결과 갈락토스 결핍 IgA1(galactose-deficient IgA1, Gd-IgA1)이 형성된다. 혈중 Gd-IgA1이 증가하면 이에 대한 자가항체(IgA 또는 IgG)가 생성되고, 이들이 결합하여 순환 면역복합체를 형성한다(Figure 1).
이러한 면역복합체는 사구체 메산지움에 축적되며, 보체 시스템의 활성화, 사이토카인 분비 증가, 메산지움 세포 증식을 유도한다. 이러한 일련의 반응은 사구체 손상으로 이어지며, 결과적으로 만성 신질환(chronic kidney disease, CKD), 사구체 여과율(glomerular filtration rate, GFR) 감소, 단핵구 화학유인 단백질(monocyte chemoattractant protein, MCP)의 증가와 같은 병태생리적 변화를 초래한다.
IgA 신병증(IgAN) 병인 발생과 4단계 가설은?
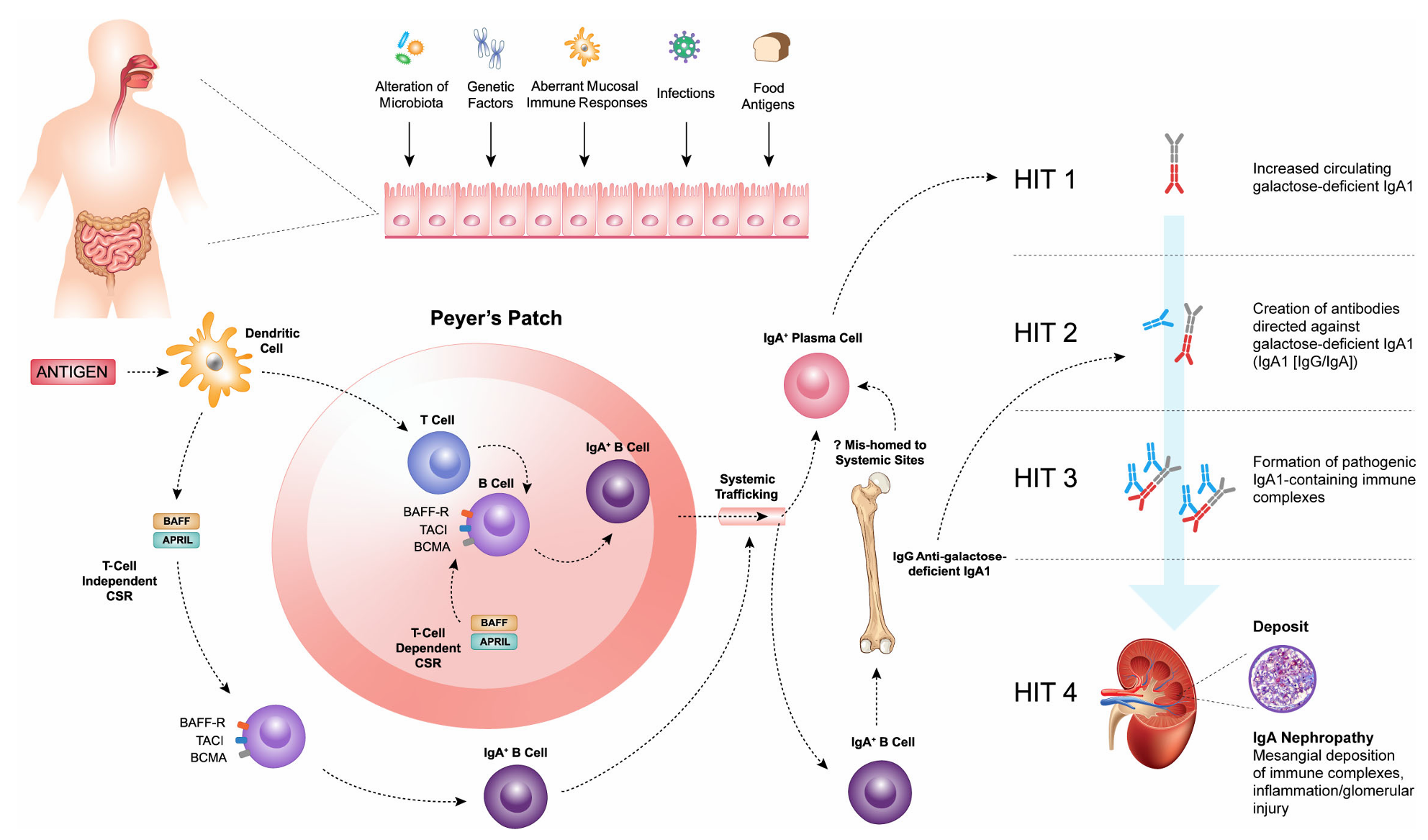
IgA 신병증(IgAN)에서 증가된 갈락토스 결핍 IgA1(Gd-IgA1)의 주요 기원은 점막으로 제시되고 있다. 인체 IgA의 대부분은 점막 관련 림프조직(mucosal-associated lymphoid tissue, MALT)에 존재하는 형질세포에서 생성되며, 특히 장관 관련 림프조직(gut-associated lymphoid tissue, GALT)과 비인두 관련 림프조직(nasopharynx-associated lymphoid tissue, NALT)이 핵심적인 역할을 한다. 실제로 IgAN 환자에서는 편도염, 상기도 감염 또는 위장관 감염과 같은 점막 감염과 연관된 시기에 혈뇨가 발생하는 경우가 흔히 관찰되며, 이는 점막–신장 축(mucosa–kidney axis)의 연관성을 시사한다.
GALT, 특히 페이어 패치(Peyer’s patches, PPs) 내 면역 반응은 T 세포 의존성 및 비의존성 경로를 모두 포함한다. 해당 조직에서는 수지상세포와 같은 항원제시세포가 항원을 포획하고, 이를 통해 미성숙 B 세포가 활성화되어 IgA⁺ B 세포로의 계열 전환(class switch recombination, CSR)이 유도된다. 이러한 과정은 T 세포 의존성 또는 비의존성 공자극 신호에 의해 조절된다.
정상적인 점막 면역에서 IgA 생성으로의 전환은 필수적인 방어 기전으로, IgA는 점막 표면에서 병원체를 중화하고 공생 미생물과의 항상성을 유지하는 역할을 한다. 그러나 IgAN에서는 B 세포 활성화 및 CSR 과정의 이상으로 인해 Gd-IgA1이 과도하게 생성된다.
종양괴사인자(Tumor Necrosis Factor, TNF) 계열에 속하는 B 세포 활성화 인자(B-cell activating factor, BAFF)와 증식 유도 리간드(a proliferation-inducing ligand, APRIL)는 T 세포 의존성 및 비의존성 CSR을 모두 촉진하며, IgA⁺ B 세포의 생성과 생존에 핵심적인 역할을 한다. 생성된 IgA⁺ B 세포는 림프계 및 혈류를 통해 점막을 벗어나 다양한 조직으로 이동한다.
특히 B 세포 표면에 발현되는 TACI(transmembrane activator and CAML interactor), BCMA(B-cell maturation antigen), BAFF-R(B-cell activating factor receptor)는 BAFF 및 APRIL과 결합함으로써 B 세포의 생존, 증식, 그리고 IgA 생성 세포로의 분화를 촉진한다. 이러한 사이토카인–수용체 상호작용은 면역 반응을 증폭시키고 IgAN의 병태생리에 중요한 기여를 한다.
IgAN 환자에서는 이러한 세포 이동이 비정상적으로 조절되어, 점막 유래 IgA⁺ 형질세포가 골수와 같은 전신 조직으로 이소성 이동(homing)하는 것으로 추정된다. 그 결과 “점막형” Gd-IgA1이 혈중에서 지속적으로 생성된다. 또한 최근 연구에서는 장 내강으로부터 Gd-IgA1의 역수송 또는 IgA⁺ B 세포의 신장 직접 이동 기전 역시 IgAN 병인에 기여할 가능성이 제시되고 있다.
한편, Gd-IgA1 수치의 증가만으로는 IgAN이 발생하지 않는다. 실제로 일부 1차 가족 구성원에서도 유사하게 높은 Gd-IgA1 수치가 관찰되지만, 임상적 신장 질환으로 진행하지 않는 경우가 존재한다. IgAN에서 신장 손상이 발생하기 위해서는 Gd-IgA1을 포함하는 면역복합체의 형성이 필수적이다.
이러한 개념은 IgAN의 병인을 설명하는 ‘4단계 타격 가설(four-hit hypothesis)’로 정리된다. 이 가설에 따르면, 순환 Gd-IgA1의 증가(Hit 1)가 항 Gd-IgA1 자가항체(IgA 또는 IgG)의 생성을 유도하고(Hit 2), 이어 면역복합체가 형성되며(Hit 3), 최종적으로 이러한 복합체가 사구체에 침착되어 염증과 신장 손상을 유발한다(Hit 4). 따라서 IgAN은 자가면역 기전을 포함하는 면역매개 질환으로 이해될 수 있다(Figure 2).
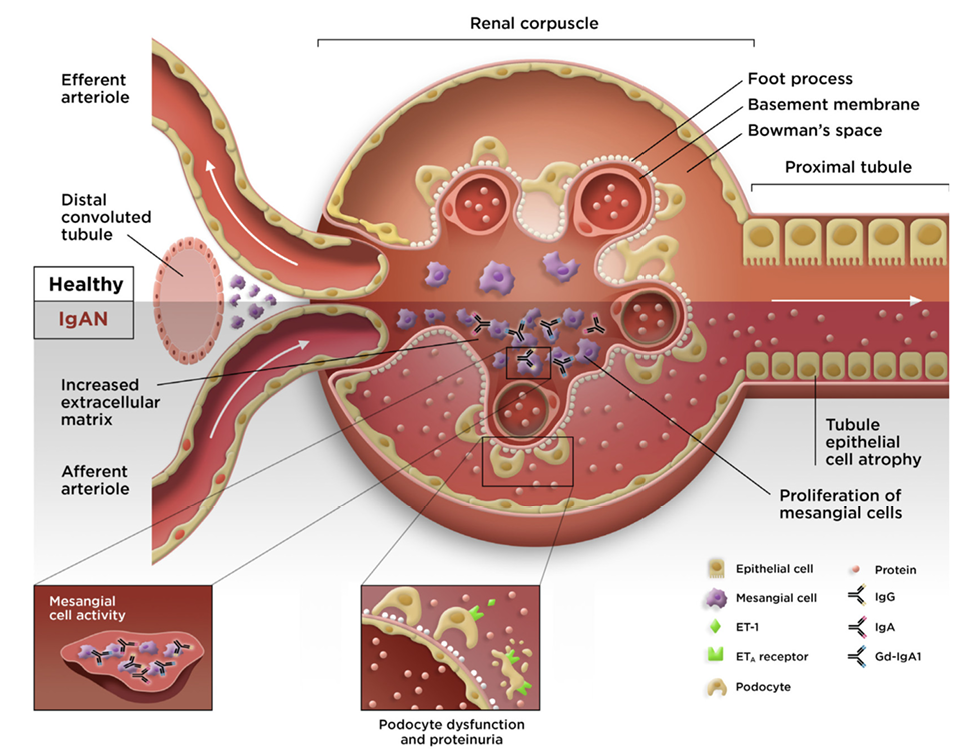
정상 사구체에서는 IgA의 침착이나 면역복합체 형성이 관찰되지 않으며, 메산지움 세포와 기질은 항상성 상태를 유지한다. 또한 보체 활성화 및 염증 반응이 유발되지 않아 사구체의 구조적·기능적 안정성이 보존된다.
반면 IgAN은 비정상적으로 당화된 IgA1의 생성에서 시작된다. 이러한 IgA1은 자가항체(IgG 또는 IgA)의 표적이 되어 순환 면역복합체를 형성하고, 이후 사구체 메산지움에 선택적으로 침착된다. 침착된 면역복합체는 메산지움 세포를 활성화시키며, 보체계(특히 C3 중심 경로)의 활성화를 유도하여 염증 반응과 세포 증식을 촉진한다. 그 결과 메산지움 기질의 확장과 세포 증식이 발생하고, 사구체의 구조적 변화와 여과 기능의 손상이 초래된다.
이와 함께 사구체 메산지움 세포의 활성화는 세포외기질(extracellular matrix) 생성 증가, 보체계 활성화, 그리고 다양한 사이토카인 및 케모카인의 분비를 유도한다. 이러한 반응은 국소 염증과 섬유화를 증폭시키며, 사구체 손상과 여과 장벽의 파괴로 이어진다. 결과적으로 혈뇨, 단백뇨, 그리고 진행성 신기능 저하가 나타나며, 이는 IgAN의 대표적인 임상적 특징이다(Figure 3).
현재 개발 중인 다양한 치료제는 면역복합체를 생성하는 상위 단계의 형질세포부터 하위 단계의 보체계 구성요소에 이르기까지 IgAN 병태생리의 다양한 경로를 표적으로 하고 있다.
원발성 면역글로불린 A 신병증(IgAN) 사용하는 약제는?
IgA 신병증(IgAN)의 치료는 KDIGO 가이드라인에 따라 보존적 치료를 기본으로 하며, 질병 활성도와 진행 위험도에 따라 단계적으로 치료 전략을 적용한다.
모든 IgAN 환자에서는 단백뇨 감소와 신기능 보존을 목표로 한 최적화된 지지 치료가 우선적으로 권장된다. 그 중심에는 레닌–안지오텐신–알도스테론계(renin–angiotensin–aldosterone system, RAAS) 억제제가 있으며, angiotensin-converting enzyme inhibitor(ACEi) 또는 angiotensin receptor blocker(ARB)를 사용하여 사구체 내 압력을 감소시키고 단백뇨를 효과적으로 줄인다. 이러한 약제는 단순한 혈압 조절을 넘어 사구체 과여과를 완화하고, 단백뇨 감소를 통해 신손상의 진행을 지연시키는 핵심적인 신보호 효과를 나타낸다.
혈압 조절은 IgAN 치료에서 중요한 요소로, 일반적으로 수축기 혈압을 120mmHg 이하로 유지하는 것이 권장된다(개별 환자의 상태에 따라 조정 가능). 특히 단백뇨가 동반된 환자에서는 보다 엄격한 혈압 조절이 신기능 보존에 유리한 것으로 알려져 있다. 또한 RAAS 억제제는 가능한 최대 내약 용량까지 점진적으로 증량하여 단백뇨 감소 효과를 극대화하는 것이 권장된다.
비약물적 중재 또한 중요한 치료 축을 구성한다. 염분 섭취 제한(일반적으로 하루 2g 미만의 나트륨 섭취 권장)은 RAAS 억제제의 항단백뇨 효과를 증강시키며, 체중 조절과 규칙적인 신체 활동은 전반적인 심혈관 위험 감소와 신기능 보존에 기여한다. 더불어 금연, 과도한 단백질 섭취 제한, 그리고 대사 이상(예: 이상지질혈증, 인슐린 저항성)에 대한 관리 역시 병행되어야 한다.
지지 치료에도 불구하고 의미 있는 단백뇨가 지속되거나 질병 진행 위험이 높은 환자에서는 면역조절 치료가 고려된다. 선택된 환자에서 전신 코르티코스테로이드 사용이 제안될 수 있으나, 감염, 대사 이상, 골다공증 등 잠재적 부작용 위험을 고려하여 신중한 환자 선별이 필요하다.
최근에는 질환의 병태생리를 직접 표적으로 하는 치료 전략이 개발되고 있다. 장관 점막 면역을 조절하는 표적 방출 부데소니드 제제인 Tarpeyo는 Peyer’s patches를 통해 점막 유래 IgA 생성을 감소시키는 기전으로 활용되고 있다. 또한 B 세포 활성화 경로를 조절하는 BAFF/APRIL 축을 표적으로 하는 치료제와 보체 경로 억제제 등 다양한 기전 기반 치료제가 임상 개발 단계에서 연구되고 있다.
따라서 IgAN 치료는 기존의 비특이적 신보호 중심 접근에서 점차 질환의 면역학적 기전을 직접 조절하는 정밀 치료 전략으로 확장되고 있으며, 환자의 위험도에 기반한 단계적 치료 접근이 중요하다.
면역글로불린 A 신병증(IgA nephropathy, IgAN)에 최근 마국 FDA에서 승인돤 신약은?
IgA 신병증(IgAN)의 치료는 최근 병태생리에 기반한 다양한 표적 치료 전략으로 확장되고 있으며, 승인된 약제들은 점막 면역, 혈역학, 보체, endothelin 경로, 그리고 B 세포–면역글로불린 생성 축을 순차적으로 표적으로 하는 양상을 보인다.
가장 먼저 승인된 약제는 Tarpeyo(성분명: budesonide)로, 2021년 FDA 가속 승인 이후 2023년 최종 승인을 받았다. 이 약제는 장관의 Peyer’s patches를 표적으로 하는 지연 방출형 스테로이드로, 점막 면역계를 선택적으로 조절하여 IgA 생성 감소를 유도한다. 특히 병인 물질인 갈락토스 결핍 IgA1(Gd-IgA1)의 생성을 상위 단계에서 억제함으로써, IgAN의 점막–신장 축(mucosa–kidney axis)을 직접적으로 조절하는 기전을 가진다.
이후 2023년에 승인된 Filspari(성분명: sparsentan)은 endothelin type A receptor와 angiotensin II receptor를 동시에 차단하는 이중 수용체 길항제이다. 이를 통해 사구체 내 혈역학적 부담을 감소시키고 단백뇨를 효과적으로 억제하며, 기존 RAAS 억제제 대비 강화된 단백뇨 감소 효과를 보이는 것이 특징이다.
2024년에는 Fabhalta(성분명: iptacopan)가 승인되었으며, 이는 보체 alternative pathway의 핵심 구성 요소인 factor B를 선택적으로 억제하는 경구용 소분자 약제이다. 해당 약제는 보체 활성화를 차단하여 사구체 내 염증 반응을 감소시키며, IgAN에서 보체 매개 손상이 중요한 병태생리 기전임을 반영한 치료 전략으로 평가된다.
2025년에는 Vanrafia(성분명: atrasentan)가 승인되었으며, 선택적 endothelin A receptor 길항제로 작용한다. 이 약제는 사구체 내 혈관 수축, 염증 및 섬유화를 억제함으로써 단백뇨 감소와 신기능 보존 효과를 나타내며, endothelin 경로의 병태생리적 중요성을 반영한 치료 접근이다.
가장 최근에는 Voyxact(성분명: sibeprenlimab)가 2025년 승인되었다. 이 약제는 APRIL(a proliferation-inducing ligand)을 선택적으로 차단하는 인간화 단클론 항체로, B 세포의 class switch recombination과 형질세포 생존을 억제함으로써 IgA 생성 감소를 유도한다. 그 결과 Gd-IgA1 생성 감소, 자가항체 형성 억제, 그리고 면역복합체 형성 감소로 이어지는 상위 단계(upstream)의 면역 조절 효과를 나타낸다.
이와 같이 IgAN 치료는 비특이적 신보호 중심 접근에서 벗어나, 질환의 병태생리를 직접 표적으로 하는 정밀 치료 전략으로 빠르게 전환되고 있으며, 각 치료제는 서로 다른 병인 경로를 보완적으로 조절하는 특징을 가진다.
APRIL(A-Proliferation-Inducing-Ligand) 차단제는 무엇인가?
BAFF(B-cell activating factor)와 APRIL(a proliferation-inducing ligand)은 모두 TNF 계열 리간드로서 B 세포의 생존과 분화를 조절하는 공통된 기능을 가지지만, 작용 범위와 생물학적 특이성에서 차이를 보인다.
BAFF는 주로 BAFF-R을 통해 미성숙 및 성숙 B 세포의 생존을 유지하는 데 중요한 역할을 하며, 전반적인 B 세포 항상성 유지에 필수적인 신호로 작용한다.
반면 APRIL은 TACI(transmembrane activator and CAML interactor)와 BCMA(B-cell maturation antigen)를 통해 주로 class switch recombination(CSR)과 형질세포 생존을 촉진하며, 특히 IgA 생성과 밀접하게 연관된 신호를 전달한다.
IgAN에서는 점막 유래 IgA, 특히 Gd-IgA1의 과도한 생성이 병인의 핵심 기전으로 작용한다. 이에 따라 IgA 생성에 직접적으로 관여하는 APRIL 경로가 중요한 치료 표적으로 제시된다. APRIL을 선택적으로 차단할 경우 IgA 생성과 형질세포 유지가 억제되어, 병인 물질인 Gd-IgA1의 감소를 유도할 수 있다.
반면 BAFF는 전체 B 세포 생존에 필수적인 역할을 수행하므로, 이를 광범위하게 억제할 경우 면역억제에 따른 감염 위험 증가 등 비특이적 부작용이 발생할 가능성이 있다. 따라서 IgAN에서는 보다 선택적으로 IgA 생성 경로를 조절할 수 있는 APRIL 차단 전략이 치료적으로 유리한 접근으로 평가된다.
APRIL을 표적으로 하는 단클론 항체는 APRIL에 선택적으로 결합하여 TACI 및 BCMA 수용체로 전달되는 신호를 차단함으로써, B 세포의 분화와 형질세포 생존을 억제한다. 그 결과 IgA, 특히 병인적 역할을 하는 Gd-IgA1의 생성이 감소한다.
특히 APRIL은 점막 면역에서 IgA class switching과 형질세포 유지에 핵심적인 역할을 수행하므로, 이를 억제함으로써 점막 유래 IgA 생성 자체를 상위 단계에서 감소시키는 효과를 나타낸다. 이러한 작용은 Gd-IgA1 감소 → 자가항체 생성 감소 → 면역복합체 형성 감소 → 사구체 침착 및 염증 반응 감소로 이어지는 병태생리적 연쇄를 차단하는 결과로 이어진다.
시베프렌리맙은 어떤 약제인가?
시베프렌리맙은 IgAN의 발병 기전을 설명하는 4단계 과정에서 핵심적인 역할을 하는 APRIL에 선택적으로 결합하여 그 생물학적 활성을 차단하는 인간화 IgG2 단클론 항체이다(Figure 4).
APRIL은 병원성 Gd-IgA1의 생성과 형질세포 생존을 촉진함으로써 IgAN의 발생 및 진행에 중요한 역할을 한다. APRIL을 억제함으로써 시베프렌리맙은 혈중 Gd-IgA1 수치를 감소시키고, 이어 자가항체 형성 및 면역복합체 생성 감소를 통해 질환의 핵심 병태생리 과정을 상위 단계에서 조절한다. 이 약제는 4주 간격으로 피하 투여하는 자가 주사 제형으로 개발되었다.
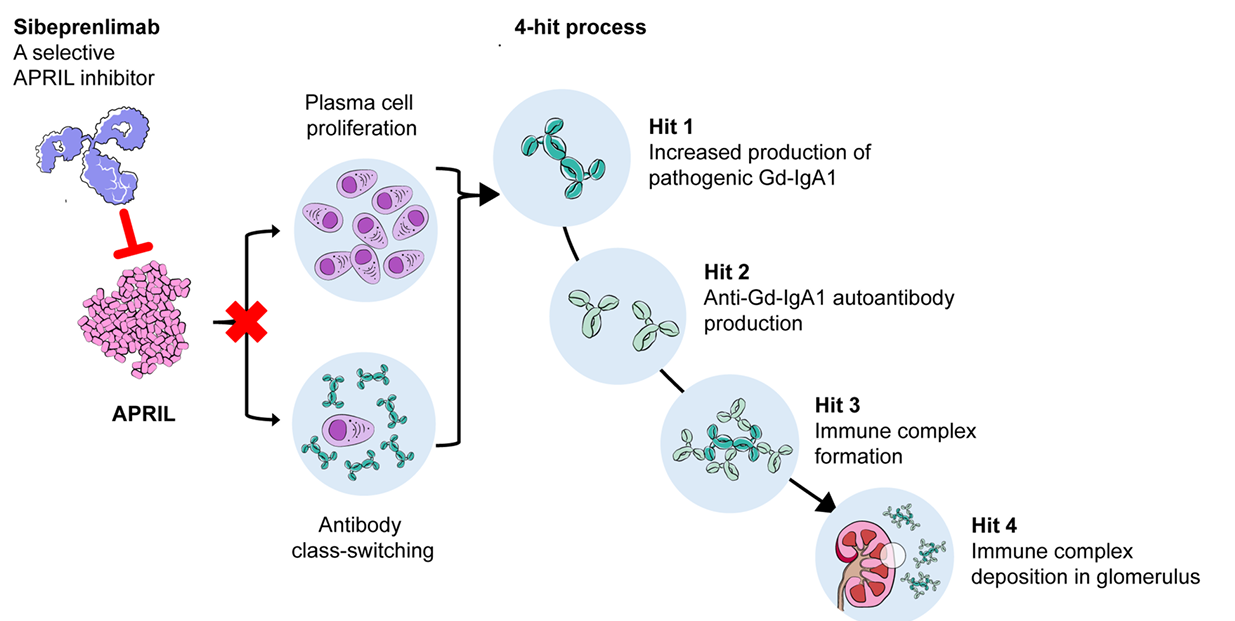
2018년 이후 IgAN 성인 환자를 대상으로 시베프렌리맙의 유효성과 안전성을 평가하기 위한 총 6개의 임상시험으로 구성된 포괄적인 임상 개발 프로그램이 진행되어 왔다. 전임상 및 1상 연구에서는 시베프렌리맙이 혈청 APRIL 농도와 병원성 Gd-IgA1 생성을 감소시키고, 그 결과 면역복합체 형성을 억제함이 확인되었다.
ENVISION 연구에서는 시베프렌리맙의 신장 보호 효과를 평가하였으며, 2상 시험의 약동학 및 IgA 모델링 결과를 통해 시베프렌리맙 400mg 피하 투여가 4mg/kg 정맥 투여와 유사한 약물 노출 및 IgA 감소 효과를 나타낼 수 있음이 시사되었다.
2상 ENVISION 임상시험에서는 생검으로 확진된 IgAN 환자를 대상으로 체중 기반 월 1회 정맥 투여를 시행하였으며, 주요 평가변수인 12개월 시점 24시간 요단백/크레아티닌 비(uPCR-24h)의 변화에서 용량 의존적인 치료 효과가 확인되었다. 특히 4mg/kg 투여군에서는 약 59% 감소를 보인 반면, 위약군에서는 약 20% 감소에 그쳤다.
또한 시베프렌리맙 치료는 혈청 Gd-IgA1(약 65%), 총 IgA(약 65%), IgG(약 35%), IgM(약 75%) 농도를 감소시켰으며, 혈청 APRIL을 거의 완전하고 지속적으로 억제하는 효과를 나타냈다.
기저 시점부터 12개월까지의 연간 사구체여과율(eGFR) 감소율 또한 시베프렌리맙 4mg/kg 투여군에서 유의하게 억제된 것으로 나타났으며(0.2 ± 1.8mL/min/1.73 m²), 위약군에서는 더 큰 감소가 관찰되었다(−7.4 ± 1.8mL/min/1.73 m²). 한편 이상반응 발생률은 두 군 간 유사한 수준으로 보고되었다.
IgAN 임상시험에서 단백뇨 감소와 eGFR 감소 억제는 치료 효과를 평가하는 대표적인 대리지표로 널리 인정되고 있으며, 이러한 결과는 APRIL 억제가 IgAN 치료에서 임상적으로 의미 있는 효과를 가질 수 있음을 뒷받침한다.
시베프렌리맙은 치료적 위치는?
IgA 신병증의 치료는 KDIGO 가이드라인에 따른 단계적 접근을 기반으로 하며, 초기에는 레닌–안지오텐신–알도스테론계(RAAS) 억제제를 중심으로 한 지지요법을 통해 단백뇨 감소와 신기능 보존을 목표로 한다. 그러나 일부 환자에서는 이러한 치료에도 불구하고 질병이 지속적으로 진행하며, 고위험군에서는 스테로이드 또는 면역억제제 사용이 고려된다. 다만 감염 및 전신 부작용의 위험이 치료 적용에 있어 중요한 제한 요인으로 작용한다.
최근에는 IgAN의 병태생리를 반영한 다양한 표적 치료제가 도입되면서 치료 전략이 확장되고 있다. 점막 면역을 조절하는 탈페이요(budesonide), 혈역학적 조절을 기반으로 하는 필스파리(sparsentan) 및 반라피아(atrasentan), 그리고 보체 경로를 억제하는 파발타(iptacopan) 등 다양한 기전의 치료제가 임상에서 활용되고 있다.
이들 약제는 각각 점막 면역, 사구체 혈역학, 보체 매개 염증 등 질환의 하위 병태생리 단계를 조절하는 전략으로 작용한다. 반면 시베프렌리맙은 Gd-IgA1을 중심으로 하는 병인의 상위 단계에 직접 개입하는 치료 전략으로 개발된 약제로, 기존 치료와 차별화된 임상적 위치를 가진다.
IgAN은 Gd-IgA1 생성 증가, 이에 대한 자가항체 형성, 면역복합체 형성 및 사구체 침착, 그리고 보체 활성화를 통한 염증 반응으로 이어지는 다단계 병인 과정을 특징으로 한다.
시벤프렌리맙은 APRIL을 선택적으로 차단함으로써 B 세포의 면역글로불린 계열 전환(class switch recombination)과 형질세포 생존을 억제하고, 결과적으로 Gd-IgA1 생성 자체를 감소시키는 상위(upstream) 기전을 가진다. 이러한 작용은 단순한 단백뇨 감소를 넘어 질환의 근본 병인에 직접 작용하는 disease-modifying 접근으로 해석될 수 있다.
또한 순환 Gd-IgA1 및 항 Gd-IgA1 자가항체 수치 감소와 연계된 생물학적 효과는 질병 활성도 조절과 예후 개선에 기여할 수 있는 바이오마커 기반 치료 전략의 가능성을 시사한다.
임상적으로는 초기 단계에서 지지요법을 우선 적용하되, 지속적인 단백뇨 또는 질병 진행 위험이 높은 환자군에서는 시벤프렌리맙과 같은 표적 치료를 조기에 병용하거나 단계적으로 도입하는 전략이 고려될 수 있다. 이는 장기적인 신기능 보존과 말기 신부전 진행 지연을 목표로 하는 치료 패러다임의 변화를 반영한다.
따라서 시벤프렌리맙은 기존 치료가 주로 하위 병태생리 단계에 작용하는 것과 달리 IgA 생성 단계 자체를 조절하는 상위 표적 치료제로서, IgAN 치료 전략에서 중요한 위치를 차지하며 향후 정밀의학 기반 치료 접근의 핵심 축으로 자리잡을 가능성이 있다.
시벤프렌리맙(voyxact)의 허가임상은 어떠한가?
VOYXACT의 단백뇨에 대한 효과는 생검으로 IgA 신병증이 확인된 성인 환자를 대상으로 한 무작위 배정, 이중눈가림, 위약 대조, 다기관 글로벌 임상시험(VISIONARY)에서 평가되었다.
연구 대상은 사구체 여과율(eGFR)이 30mL/min/1.73 m² 이상이고 단백뇨가 존재하는 환자로 정의되었으며 단백뇨 기준은 24시간 소변 단백/크레아티닌 비(uPCR-24h) ≥0.75g/g 또는 하루 소변 단백 ≥1.0g/day였다. 또한 모든 환자는 최대 허용 용량의 ACEi 및/또는 ARB를 안정적으로 투여받고 있었으며 일부 환자에서는 sodium-glucose co-transporter 2 inhibitor(SGLT2i)가 병용되었다.
다른 사구체 질환이 있는 환자 또는 스크리닝 이전 16주 이내에 전신 면역억제제를 사용한 환자는 연구에서 제외되었다. 환자는 1:1 비율로 무작위 배정되어 VOYXACT 또는 위약을 4주 간격으로 피하 주사로 투여받았다.
총 510명의 환자가 등록되었으며 이 중 9개월 시점 방문에 도달할 수 있었던 최초 320명(63%)을 대상으로 중간 효능 분석이 수행되었다. 이 중 152명은 VOYXACT를 투여받았고 168명은 위약군에 배정되었다. 치료군 간 기저 인구학적 특성과 질병 특성은 전반적으로 균형을 이루었다. 기저 시점에서 중앙 연령은 42세(범위 18–83세)였으며 남성이 63%를 차지하였다.
기저 시점에서 평균 uPCR-24h는 1.5g/g였고 평균 eGFR은 63mL/min/1.73 m²였으며 74%의 환자에서 혈뇨가 관찰되었다. 약 67%의 환자는 고혈압 병력이 있었고 7%는 제2형 당뇨병 병력을 가지고 있었다. 또한 98%의 환자가 ACEi 및/또는 ARB를 투여받고 있었으며 약 40%는 SGLT2i를 병용하고 있었다.
주요 평가 변수는 9개월 시점에서 기저 대비 uPCR-24h의 상대적 변화였다. uPCR-24h의 기저 대비 평균 추정 변화율은 Figure 1에 제시되어 있으며 아침 첫 소변을 이용한 spot urine에서 측정된 uPCR의 기하평균 변화율 추이는 Figure 2에 제시되어 있다.
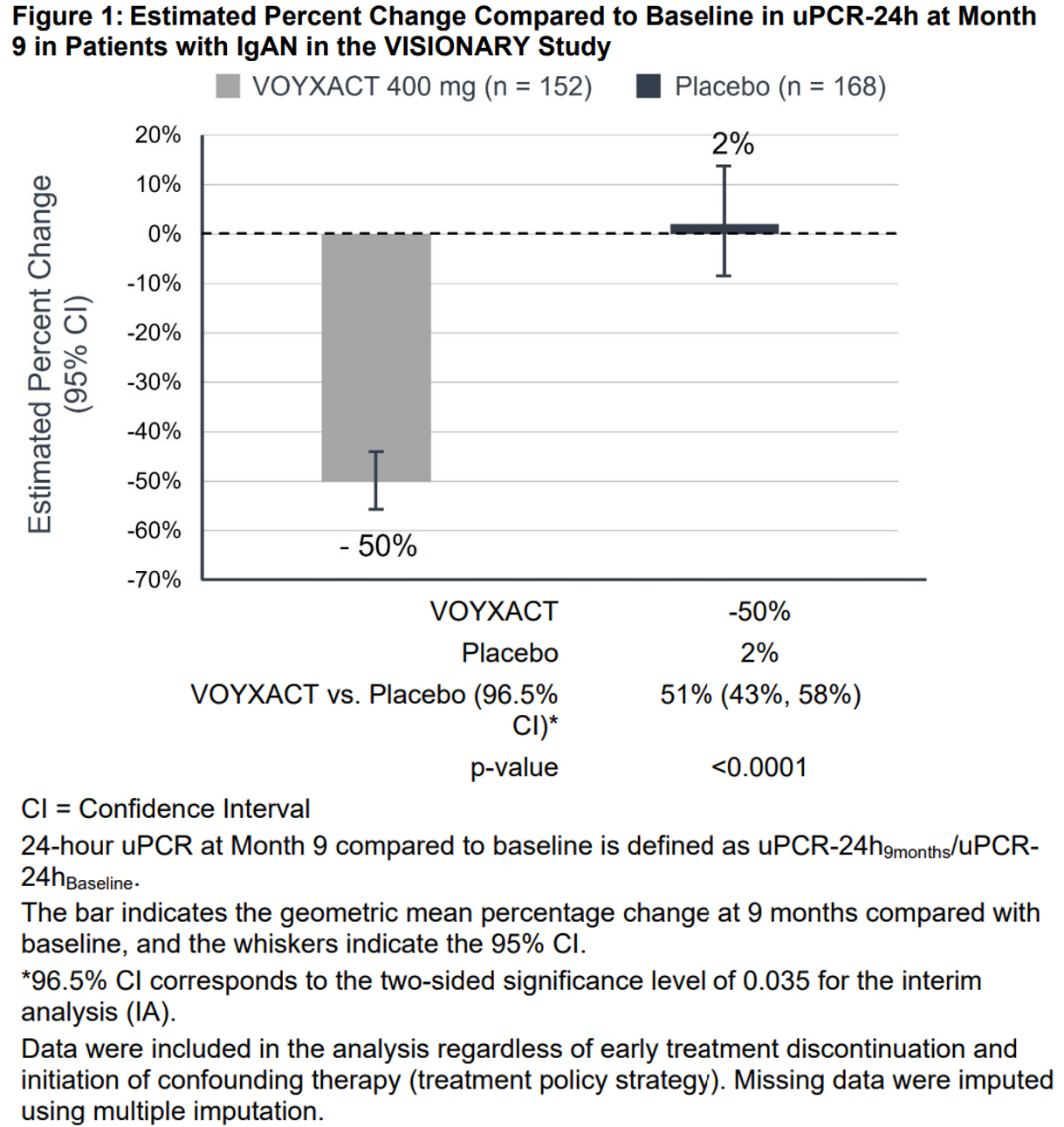
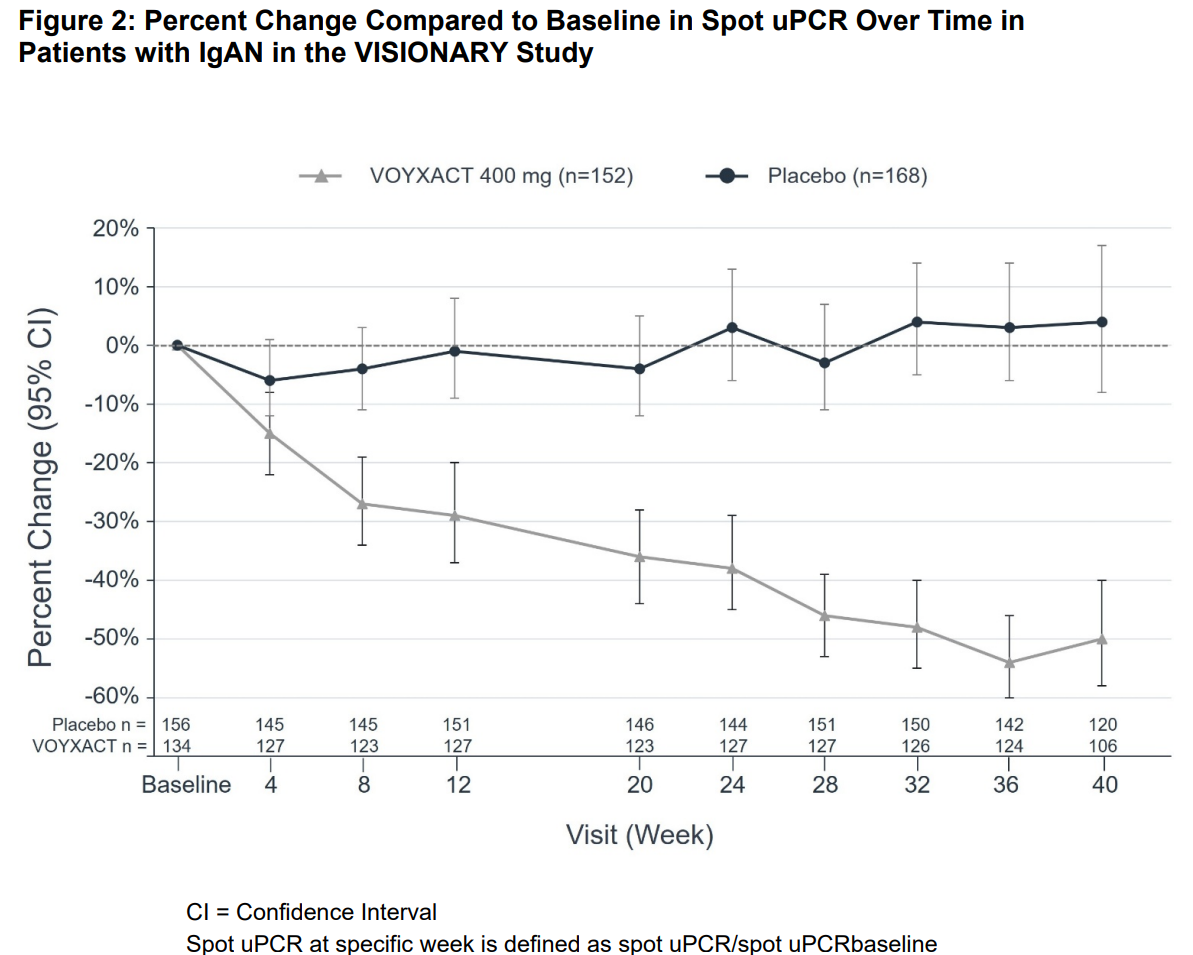
VOYXACT의 치료 효과(VOYXACT와 위약 간 uPCR-24h 감소율)는 성별, 연령, 인종, 민족, 지역과 같은 인구학적 요인뿐 아니라 기저 단백뇨 수준(uPCR-24h), 기저 사구체 여과율(eGFR), 그리고 SGLT2i 사용 여부를 포함한 사전 정의된 층화 변수 전반에서 일관되게 나타났다.
시베프렌리맙의 임상적 의의, 허가 근거 및 향후 과제는
시벤프렌리맙은 APRIL을 선택적으로 억제하는 단클론 항체로서 IgAN의 병태생리에서 핵심적인 상위 단계인 Gd-IgA1 생성 경로에 직접 개입하는 치료제이다. 기존 치료가 주로 단백뇨 감소 및 사구체 혈역학 조절과 같은 하위 병태생리 단계에 작용하는 것과 달리 시벤프렌리맙은 B 세포의 class switch recombination과 형질세포 생존을 억제함으로써 Gd-IgA1 생성 자체를 감소시키는 upstream 기전을 가진다. 이러한 특성은 질병의 근본 원인에 작용하는 disease-modifying therapy로서의 가능성을 시사한다.
시벤프렌리맙의 허가는 VISIONARY 임상시험을 근거로 이루어졌으며 해당 연구에서 시벤프렌리맙은 표준 치료(ACEi/ARB ± SGLT2i)를 유지하는 환자군에서 단백뇨(uPCR-24h)의 유의한 감소를 나타내었다. 특히 치료 효과는 성별, 연령, 인종, 기저 단백뇨 수준, eGFR 및 SGLT2 억제제 사용 여부 등 다양한 하위군에서 일관되게 나타나 환자군 전반에서 재현성을 보였다. 이러한 결과는 시벤프렌리맙이 기존 지지요법 위에 추가되는 치료 옵션으로서 임상적 유용성을 가질 수 있음을 뒷받침한다.
그러나 시벤프렌리맙의 임상 적용에는 몇 가지 한계점이 존재한다. 첫째, 허가 근거가 주로 단백뇨 감소와 같은 surrogate endpoint에 기반하고 있어 장기적인 신기능 보존(eGFR decline 감소 또는 ESRD 진행 억제)에 대한 확정적 근거는 아직 제한적이다. 둘째, APRIL 억제에 따른 장기 면역학적 영향, 특히 점막 면역 저하 및 감염 위험 증가 가능성에 대한 충분한 장기 안전성 데이터가 확보되지 않았다. 셋째, IgAN의 병태생리가 이질적인 점을 고려할 때 모든 환자에서 동일한 치료 반응을 기대하기 어려우며 환자 선택 기준의 정립이 필요하다.
향후 치료 전략으로는 첫째, 장기 추적 연구를 통해 eGFR 감소율 및 말기 신부전 진행 억제와 같은 hard endpoint에 대한 효과를 입증하는 것이 필요하다. 둘째, Gd-IgA1 및 항 Gd-IgA1 항체와 같은 바이오마커를 활용한 반응 예측 및 환자 선별이 필요하다. 셋째, RAAS 억제제, SGLT2 억제제, endothelin receptor antagonist, 보체 억제제 등과의 병용 요법을 통해 다중 병태생리 경로를 동시에 조절하는 병합 치료가 고려될 수 있다. 넷째, BAFF/APRIL 축 외에도 점막 면역 및 장-신장 축을 표적으로 하는 치료와의 통합적 접근이 필요하다.
따라서 시벤프렌리맙은 IgAN 치료에서 기존의 보존적 치료를 넘어 질병의 면역학적 근본 기전에 직접 개입하는 최초의 APRIL 표적 치료제로서 중요한 치료적 전환점을 제시하며 향후 바이오마커 기반 환자 맞춤 치료와 병용 요법 전략을 통해 그 임상적 가치가 더욱 확대될 것으로 예상된다.
참고문헌
1. Vicki J Hwang et al. “Biomarkers in IgA nephropathy” Biomark. Med. (2014) 8(10), 1263–1277.
2. Cheung CK et al. “The roleof BAFF and APRIL in IgA nephropathy:pathogenic mechanisms andtargeted therapies” Front. Nephrol. 3:1346769 (2024).
3. Mohit Mathur et al. “APRoliferation-Inducing Ligand (APRIL) in the Pathogenesisof Immunoglobulin A Nephropathy: A Review of the Evidence” J. Clin. Med. 2023, 12, 6927.
4. Vlado Perkovic et al. “Evaluating Sibeprenlimab in IgA Nephropathy - Rationale and Baseline Data from the VISIONARY Trial” Kidney International Reports (2025) 10, 4207–4218.
5. Yitao Fan et al. “Advancements in understanding the roleof intestinal dysbacteriosis mediated mucosalimmunity in IgA nephropathy” BMC Nephrology (2024) 25:203.
6. Loreto Gesualdo et al. “The mucosal immune system and IgA nephropathy” Seminars in Immunopathology (2021) 43:657–668.
7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).
- 익명 댓글
- 실명 댓글
- 댓글 0
- 최신순
- 찬성순
- 반대순











































![[유한양행] 마그비 시리즈](https://cdn.platpharm.co.kr/2024/03/2403261023280000193.jpg)
![[일양약품] 프로엑스피](https://cdn.platpharm.co.kr/2026/01/2601221008450010125.webp)
![[신신제약] 아렉스마일드](https://cdn.platpharm.co.kr/2023/11/2311300927130000133.jpg)
![[신신제약] 모스키토 밀크](https://cdn.platpharm.co.kr/2025/10/2510150733400004067.webp)
![[삼진제약] 게보핏 시리즈](https://cdn.platpharm.co.kr/2024/07/2407100728250000386.png)
![[유한양행] 안티푸라민 파스 시리즈](https://cdn.platpharm.co.kr/2024/05/2405280631070000069.png)
![[노보노디스크] 위고비](https://cdn.platpharm.co.kr/static/dailypharm/Wigobi.png)
![[리쥬올] PDLLA 퍼밍 크림 30ml](https://cdn.platpharm.co.kr/2026/04/2604070229110000386.webp)
![[옵투스] 오에수 시리즈](https://cdn.platpharm.co.kr/2026/02/2602130209000031633.webp)
![[종근당] 브레이닝캡슐](https://cdn.platpharm.co.kr/2025/06/2506040708450012544.png)
![[경방신약] 방콜브이산](https://cdn.platpharm.co.kr/2025/12/2512310630020002495.webp)
![[일양약품] 도담도담 시리즈](https://cdn.platpharm.co.kr/2024/02/2402020935180000240.jpg)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202604/1776750298620.png)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[레비온] PDRN+EGF, 레비온RX PDRN EGF 크림](https://i.baropharm.com/products/202512/1765949426601.png)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/partner/products/3f39593e-6318-4dd9-a778-c008c868b5c8.png)
![[쥬베룩] 진짜 쥬베룩을 담은 약국전용 PDLLA 크림](https://i.baropharm.com/products/202604/1775343960671.png?label=바뷰페로고)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
![[경동제약] 인태반 자양강장제, 파워콤프](https://i.baropharm.com/partner/products/0a2cbb4c-96c5-40a5-aec2-8beeae11682c.png)
![[CHD제약] 50년 전통의 천혜당 식염포도당](https://i.baropharm.com/products/202604/1775095858899.png)
![[알엑스미] 알엑스미 리쥬영 울트라 PDRN 10000 딥리페어 크림](https://i.baropharm.com/partner/products/70c72dd0-cfd3-4d80-87e4-dc4f8de6658b.png?label=바뷰페로고)
![[리쥬올] 닥터 리쥬올 어드밴스드 PDRN 리쥬비네이팅 크림 30ml](https://i.baropharm.com/partner/products/a201d2b4-f21e-4b13-957c-846d286b3d21.jpg?label=바뷰페로고)
![[정제수0%] 물 한방울 없이 콜라겐 60% 꽉 채운 PDRN](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/0a838fb804879.png)
![[신규매출/펫] 라이프펫 강아지 유산균 동물약국 필수템](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/94f80101539a8.jpg)
![[마진2배/1+1] 편한가몰 매주 업데이트되는 1+1 특가관](https://gi.esmplus.com/pyunhanga/timesale.jpg)
![[약사님복지템] 풀리오 종아리 마사지기 피로회복 필수품](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/024771c0a3d5f.png)
![[초저가더마] 약국 화장품 매대 필수! 비타민 크림](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/9dddfbfed16c2.jpg)
![[복약대효자템] 코빵에어 페퍼민트 코막힘 답답할때 필수](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/0c57b4a3f02b9.png)
![[2030유입템] 럽티 호박차 티백 V라인 이너뷰티 핫템](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/70d5f9c5baba8.jpg)
![[여성재구매1위] 오니스트 트리플 콜라겐 액상 프리미엄](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/e47b9791e6f11.jpg)
![[소아과문전픽] 야미얼스 유기농 젤리 엄마들이 찾는 간식](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/ac4a307e0a63e.png)
![[요즘대세/수면] 젤라토닌 식물성 멜라토닌 1mg 구미](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/8fb2533d57de4.png)
![[객단가수직상승] 파스찾는 환자가 같이 사가는 프리미엄 안마기](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/8cb1830429122.jpg)
![[16차 완판 신화] 환자들이 먼저 알아보는 1위 콜라겐 마스크](https://cdn.imweb.me/upload/S2025060969b2a2d28fb0a/18cc54913f205.jpg)



